Bei den ungesättigten KW gibt es z.B. folgende Stoffgruppen: Alkene (mit einer C=C-Bindung), Alkine (mit einer C≡C-Dreifachbindung) und Alkadiene (mit zwei C=C-Doppelbindungen).
1 Ein aromatischer KW (Aromat) ist eine Verbindung, die ringförmige (zyklische) Kohlenwasserstoffmoleküle mit delokalisierten (4n+2)-Elektronen enthält (z.B. Benzol C6H6).
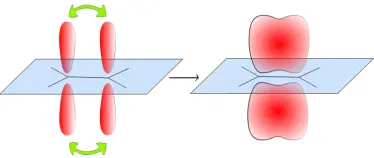
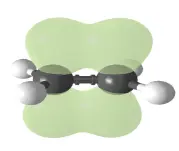
Beispiel: Der Stoff Benzol weist die Summenformel C 6H 6 auf. Er reagiert weder wie ein gesättigter noch wie ein ungesättigter KW, da die jeweils ober- und unterhalb der Molekülebene liegende „Zweitbindung“ der C-Atome (das bei der sp 2 -Hybridisierung übrigbleibende p-Orbital) zu einem Ringsystem „verschmiert“ (Delokalisierung):
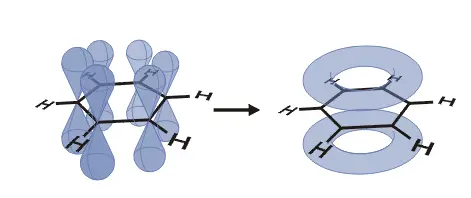 Bildquelle: CC BY-SA 1.0, https://commons.wikimedia.org/w/index.php?curid=515162
Bildquelle: CC BY-SA 1.0, https://commons.wikimedia.org/w/index.php?curid=515162
Als Strukturformeln für das C 6 H 6 -Molekül existieren folgende Varianten: (mesomere Grenzstrukturen des Benzols und sein Kalottemodell)
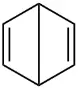 , , allgemein vereinfacht als
, , allgemein vereinfacht als
Hinweis: Weitere Beispiele für aromatische Verbindungen neben dem B enzol sind das T oluol (links) und die drei X ylole (zusammen auch “ BTX-Aromaten ” genannt):
Toluol: Xylole: Links: Toluol C 6 H 5 -CH 3 ist ein Methylbenzol – eines der H-Atome wurde durch eine CH 3 -Gruppe ersetzt. Xylole weisen je zwei CH 3 -Substituenten auf und es gibt drei Isomere. Man vergibt bei deren Benennung zur Unterscheidung Positiosziffern: Links das 1,2-Dimethylbenzol (auch ortho-Xylol genannt), mittig das 1,3-Dimethylbenzol (auch meta-Xylol) und rechts 1,4-Dimethylbenzol (auch: para-Xylol).
1 Isomerie ist das Vorhandensein verschiedener Verbindungen unterschiedlicher Struktur(formeln) mit gleicher Summenformel.
Beispiele: Vom Butan C 4 H 10 gibt es zwei Isomere, ein geradkettiges Molekül (n-Butan, im folgenden Bild links) und ein verzweigtes Molekül (Isobutan, im folgenden Bild rechts). Beim Pentan C 5 H 12 gibt es schon drei Isomere (geradkettiges n-Pentan, einfach verzweigt das Methylbutan und doppelt verzweigt das bereits genannte Neopentan, auch 2,2-Dimethylpropan genannt. Je mehr C-Atome es im KW gibt, desto mehr Isomere sind möglich: Beim Hexan C 6 H 14 gibt es bereits 5 Isomere, beim Decan C 10 H 22 schon 75 und beim Dodecan C 20 H 42 insgesamt 366319 Isomere.Auch ringförmige KW wie z.B. die Aromaten weisen Isomere auf. Vom Xylol gibt es z.B. drei Isomere (vgl. Abb oben zu Merksatz 162).
Die folgende Abbildung zeigt die beiden Butan-Isomere:

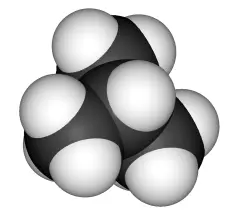
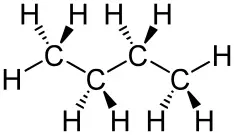

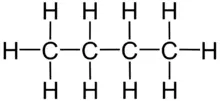
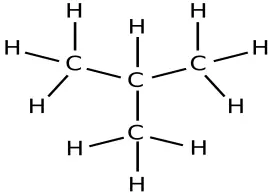
CH 3 CH 3CH 2CH 2CH 3CH 3 C CH 3 H
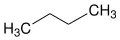 n -Butan / Isobutan (2-Methyl-propan)
n -Butan / Isobutan (2-Methyl-propan) 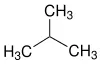
Hinweis: Neben der Positionsisomerie gibt es bei größeren Molekülen z.B. auch eine Spiegebildisomerie : Das Heptanisomer, das 3-Methyl-hexan, weist z.B. bei * ein C-Atom auf, das 4 verschiedene Reste trägt: Ein H-Atom, eine Methylgruppe –CH 3 , eine Ethylgruppe –C 2 H 5 und eine Propylgruppe –C 3 H 7 :
CH 3 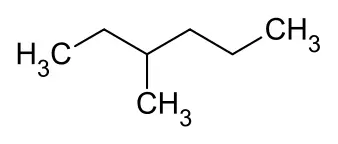 H C*C 2H 5 3-Methyl-hexan vereinfachte Strukturformel: C 3H 7(CH 3)HC*(C 2H 5)(C 3H 7)
H C*C 2H 5 3-Methyl-hexan vereinfachte Strukturformel: C 3H 7(CH 3)HC*(C 2H 5)(C 3H 7)
Beim 3-Methyl-hexan existieren zwei zueinander spiegelbildliche Isomere:
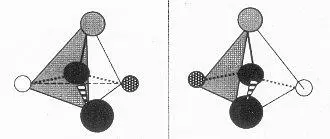
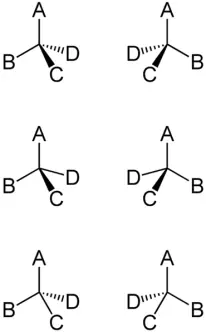
Eine Verbindung C*(ABCD) mit einem C*-Atom, das vier verschiedene Reste ( Substituenten A bis D ) aufweist, ist optisch aktiv . Sie existiert in zwei zueinander spiegelbildlichen Strukturen ( Chiralität , Enantiomeren-Paare). Solche optisch aktiven C-Atome werden als Stereo- oder Chiralitätszentren bezeichnet und in Formel oft mit einem Sternchen * markiert.
Chirale Verbindungen sind in der Biochemie von großer Bedeutung. Sie kommen in Kohlenhydraten und Proteinen vor („linksdrehende Aminosäuren“ im Joghurt), aber auch in Seitenketten des Chlorophylls oder im Vitamin E (Tocopherol).
1 Mesomerie ist das Vorhandensein mehrerer möglicher Struktur(formel)n in einem Molekül (mesomere Grenzstrukturen, z.B. Keto-Enol-Tautomerie).
Beispiele für Mesomerie (mesomere Grenzstrukturen):
Benzol:
Carbonylgruppe C=O:
Merksätze Stoffgruppenorganischer Verbindungen
1 Halogenalkane sind Kohlenwasserstoffe, in deren Moleküle in oder mehrere H-Atome durch Halogenatome ausgetauscht worden sind (Halogene als Substituenten, Mehrfachsubstitution: Di-, Tri-, Tetrahalogenalkane bis hin zu Polyhalogenalkanen). Sie sind in der Regel nicht wasserlöslich, reagieren z.T. explosionsartig mit Alkalimetallen und setzen bei Verbrennung Halogenwasserstoffe frei.
Beispiele: Der Fluorchlorkohlenwasserstoff (FCKW) Dichlordifluormethan und das Insektizid Lindan (Hexachlorcyclohexan, HCCH) sind Halogen-KW.
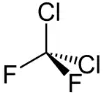 CF 2 Cl 2 Lindan, C 6 H 6 Cl 6 :
CF 2 Cl 2 Lindan, C 6 H 6 Cl 6 :
Читать дальше


 Bildquelle: CC BY-SA 1.0, https://commons.wikimedia.org/w/index.php?curid=515162
Bildquelle: CC BY-SA 1.0, https://commons.wikimedia.org/w/index.php?curid=515162 , , allgemein vereinfacht als
, , allgemein vereinfacht als





 n -Butan / Isobutan (2-Methyl-propan)
n -Butan / Isobutan (2-Methyl-propan) 
 H C*C 2H 5 3-Methyl-hexan vereinfachte Strukturformel: C 3H 7(CH 3)HC*(C 2H 5)(C 3H 7)
H C*C 2H 5 3-Methyl-hexan vereinfachte Strukturformel: C 3H 7(CH 3)HC*(C 2H 5)(C 3H 7)

 CF 2 Cl 2 Lindan, C 6 H 6 Cl 6 :
CF 2 Cl 2 Lindan, C 6 H 6 Cl 6 :










