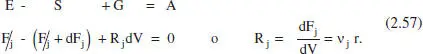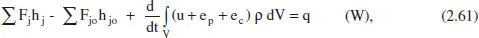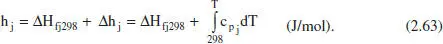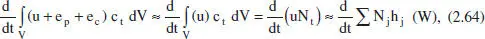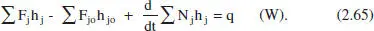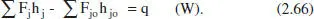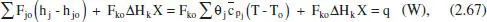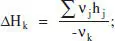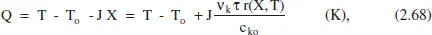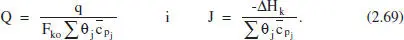Nota . La massa de catalitzador i el volum del reactor poden relacionar-se per l’equació M cat= ρ bV, en la qual ρ bés la densitat global del llit catalític i val 500 kg/m 3.
Solució :
En el cas de l’apartat b de l’exemple 2.6, la velocitat de reacció és negativa, la qual cosa indica que correspon a una situació fora del nostre abast, per tant, com que no es pot assolir, no té cap sentit físic. Per al cas c , aplicant l’equació dels gasos ideals, tenim c ko= 0.002 mol/L, c To= 0.02 mol/L, per la qual cosa Q vo= 2520 m 3/h.
Del balanç de matèria en un RCTA, eq. (2.56) tenim:

La velocitat de reacció és molt menuda, per la qual cosa el volum de reacció necessari és molt gran. Modificant les condicions d’operació es podria millorar considerablement el procés. Cal assenyalar que es tracta d’una reacció catalítica, i aquestes reaccions es duen a terme normalment en un reactor tipus RFP, i no en un RCTA.
• RFP o RCT
En la figura 2.15 es mostra un esquema d’un RFP. A més de l’aspecte de conducció i del funcionament continu (reactor continu tubular, RCT), aquest reactor ideal requereix que es complisca una hipòtesi: la circulació del fluid és francament turbulenta, a açò es refereix el nom de reactor de flux de pistó (RFP). El perfil de velocitat és pla, la qual cosa implica que totes les molècules tenen el mateix temps de residència en el reactor.
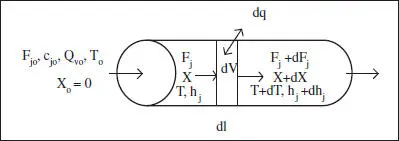
Figura 2.15. Esquema d’un RFP.
Com a conseqüència de la hipòtesi anterior, la composició canviarà únicament a la direcció axial. Atès que la composició varia d’uns punts a uns altres del sistema (la temperatura variarà o no d’acord amb el sistema d’intercanvi de calor), la velocitat de reacció també variarà. Per això, no serveix l’anàlisi macroscòpica realitzada en els anteriors reactors. Plantejant un balanç de matèria en el component j en l’element de volum d V , en estat estacionari, es té
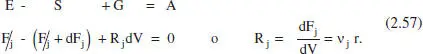
I si es tracta d’un sistema de densitat constant,
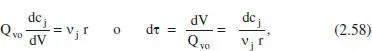
i en funció de X:

Les equacions anteriors es poden transcriure de forma gràfica tal com es pot veure en la figura 2.12, en aquest cas la variable temps, t , cal entendre-la com a temps espacial τ. La similitud entre les equacions del model del RDTA i del RFP és el resultat d’un funcionament semblant, encara que un discontinu i l’altre continu.
La forma no estacionària del balanc. de matèria en aquest reactor quedaria

D’aquesta manera s’han escrit les equacions del balanc. de matèria per als diferents reactors ideals. La utilització d’aquestes equacions estarà relacionada amb l’objectiu que es plantege. Així, en problemes de disseny, Fobjectiu és determinar les característiques del reactor (generalment el temps, que en els reactors continus es tradueix en el volum o en el cabal) que permeten obtenir una certa conversió o una producció determinada. En els problemes d’anàlisi s’estudia l’efecte d’alguna variable sobre el comportament del reactor.
2.6.2 Balang d’energia
Del mddul «Operacions Bàsiques de FEnginyeria Química» per al balanc. d’energia en sistemes amb reacció química (Aucejo i altres, 1999):
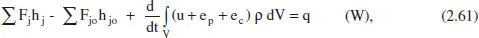
on s’han menyspreat les variations de Fenergia potential, Fenergia cinètica i la contribució del treball.
El terme q representa el flux de calor intercanviada, que es pot correspondre amb un valor donat (en el cas de calefactió elèctrica, per exemple), o en el cas que s’utilitze un fluid bescanviador pot venir donat per una equació com:

on T . és la temperatura del fluid bescanviador.
L’entalpia de l’espècie A en les condicions del corrent considerat es pot calcular amb l’equació (2.63), en el cas que no hi haja canvi de fase entre les dues temperatures considerades (la de referènda 298 K i la del corrent). En cas contrari, es modificarà adequadament aquesta equació:
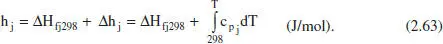
De nou resulta molt senzill aplicar l’equació (2.61) als reactors de tanc agitat, ja que la concentració i la temperatura són uniformes. No obstant això, aquesta aplicació requereix alguna simplificació, ja que en la mateixa equació s’utilitza energia interna i entalpia. Analitzant el terme d’acumulació, menyspreant de nou els termes d’energia potencial i cinètica enfront del de l’energia interna i aproximant aquesta per l’entalpia es té
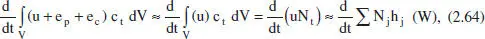
amb la qual cosa la (2.61) quedarà
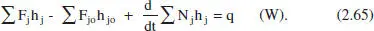
2.6.2.1 RCTA en estat estacionari
De la (2.65):
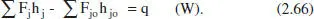
Escrivint aquesta equació en funció del grau de conversió per al cas en què hi haja una sola reacció:
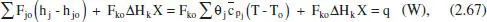
on s ha considerat que:
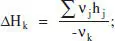
reordenant (2.67) i recordant (2.56):
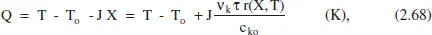
on
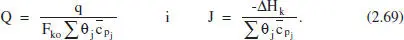
Si hi haguera diverses reaccions es tindria
Читать дальше