14. L’espècie A en dissolució amb una concentració de 2 mol/L es converteix en R en un RDTA isoterm, segons una cinètica de primer ordre. En cada cicle d’operació s’aconsegueix la conversió del 95 %. Aquest cicle d’operació dura 4 h, distribuïdes en 3 h de l’etapa de reacció i 1 h de les etapes de càrrega, descàrrega i neteja. El mercat per al producte R ha crescut, per la qual cosa es vol duplicar la capacitat de producció.
a ) Quina és la producció original (mol de R/h m 3de reactor) que es vol duplicar?
b ) Funciona el reactor en les condicions de màxima producció? En el cas que la resposta siga negativa, quina seria la producció màxima?
c ) Quin és el temps de reacció que condueix al màxim benefici?
La continuació d’aquest problema es troba en el 4.8.
Dades i Notes . El cost del reactiu A és 0.30 €/mol, el valor del producte R és de 0.90 €/mol. El cost del reactor és 120 €/ h m 3de reactor. La temperatura d’operació és 363 K.
15. La reacció de descomposició de l’acetona en fase gas és CH 3COCH 3→ CH 2CO + CH 4. Aquesta reacció es desenvoluparà en un RFP encamisat. Per la camisa del reactor circula vapor d’aigua a una temperatura prou elevada perquè el funcionament del reactor siga isoterm. El corrent aliment, que consta d’acetona pura, s’introdueix amb un cabal de 8000 kg/h a 1035 K i 1.6 atm. La conversió a l’eixida s’ha fixat en el 20 %, a causa del caràcter inestable del cetè. Determineu el volum (longitud) de reactor necessari per a aconseguir aquest grau de conversió. Determineu, així mateix, el perfil de temperatura del gas calefactor al llarg del reactor (almenys quatre punts dins de l’interval d’interès) necessari per a mantenir constant la temperatura de la mescla reactiva. Justifiqueu la variació trobada. Dades i Notes . La reacció és de primer ordre i la constant de velocitat ve donada per k = exp(34.33 - 34222/T) s -1. La calor de reacció a 1035 K és 78758 J/mol i les calors específiques dels components (J/mol K) són: 166.9 (acetona), 84.7 (cetè) i 73.0 (metà). El RFP està format, en realitat, per un banc de 1000 tubs (1.000 reactors RFP iguals funcionant en paral·lel) d’1" nominal (diàmetre = 0.0266 m). Es pot considerar que el sistema funciona a P constant. El coeficient de transferència de calor per a aquest sistema val 110 W/m 2K.
16. L’òxid d’etilè és un dels principals compostos químics per volum de producció. El 1997, als EUA, se’n van produir uns 3 milions de tones, amb un preu de 1.3 $/kg. Un 60 % de l'òxid d’etilè produït es va dedicar a la fabricació d’etilenglicol.
Calculeu el volum d’un RFP necessari per a produir òxid d’etilè a partir de l’oxidació catalítica d’etilè amb aire. L’esquema de reacció és
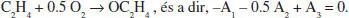
Es vol assolir un 60 % de conversió. Els reactius s’alimenten en la proporció estequiomètrica, el cabal d’alimentació de l’etilè és de 0.14 kmol/s, i la pressió de l’aliment és 10 atm. El reactor conté el catalitzador com un rebliment i opera de forma isoterma a 260 °C.
Si el reactor es constraint amb 10 bancs de tubs del tipus 40 (diàmetre intern 1.5"), amb 100 tubs per banc, quina serà la longitud d’aquests tubs?
Pot suposar-se en primera aproximació menyspreable la caiguda de pressió en el reactor. Repetiu el càlcul considerant la pèrdua de pressió en el reactor. Dades i Notes. Es pot aproximar que les propietats de la mescla reactiva són les de l’aire a les mateixes condicions de pressió i temperatura (a 10 atm i 260 °C, ρ = 6.6 kg/m 3i μ = 2.78 10 5kg/m s). La densitat aparent de les partícules de catalitzador (diàmetre 0.25”) és de 1922 kg/m 3, i la fracció buida del Hit de partícules és 0.45. La cinètica de la reacció ve donada per:
r = k P 1 1/3P 2 2/3mol de A 1/g cat. h.
Constant de la velocitat de la reacció a 260°C:
k = 0.0141 mol de A 1/atm g cat. h.
La solució d’aquest problema es dóna en l’Apèndix II (exemple II.2.4).
17. S’està dissenyant un esterilitzador de flux (continu) que operant a 121 °C per a tractar un cabal de líquid de 1 L/s. La mort de C. botulinum pot considerarse de primer ordre i la constant cinètica a la temperatura d’operació val 0.192 s 1. Determineu el volum d’un RCTA i d’un RFP necessaris per a reduir la concentració d’aquest microorganisme en sis ordres de magnitud. Repetiu el càlcul per a 12 ordres de magnitud.
Lectures d’ampliació
ABU-KHALAF, A. M. (1994): «Mathematical modeling of an experimental reaction system», Chemical Engineering Education , 28 (1), pp. 48-51.
— (1996): «Dynamic and steady-state behavior of a CSTR», Chemical Engineering Education , 30 (2), pp. 132-134.
DICKEY, D. J. (1991): «Succeed at Stirred-Tank-Reactor Design», Chemical Engineering Progress , 87 (12), pp. 22-31.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «ЛитРес».
Прочитайте эту книгу целиком, купив полную легальную версию на ЛитРес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.