Bisher haben Sie qualitativ gelernt, wie sich ein ideales Gas verhält, wenn Sie Druck, Temperatur und Volumen variieren. Der Verfahrenstechniker möchte das aber quantitativ berechnen. Er will genau wissen, wie hoch wird der Druck in einem konstanten Volumen, wenn die Temperatur erhöht wird. Hier kommt das ideale Gasgesetz ins Spiel. Es beschreibt den Zusammenhang zwischen den drei Größen Druck, Temperatur und Volumen. Das ideale Gasgesetz lautet:
(2.3) 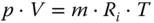
oder
(2.4) 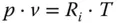
mit
p : Druck in Pa,
T : Temperatur in K,
m : Masse in kg,
R i: individuelle oder spezifische Gaskonstante in J · kg–1 · K–1 sowie dem
spezifischen Volumen v in m3/kg:(2.5)
Die individuelle oder spezifische Gaskonstante R iist eine Funktion des betrachteten Stoffs i.
Das ideale Gasgesetz ist eine der wichtigsten Gleichungen in der Verfahrenstechnik. Sind drei der vier Größen p , V , m (oder n ) sowie T bekannt, lässt sich der Zustand eines Gases vollständig beschreiben. Wird nicht mit der Masse m , sondern der Stoffmenge n als Zustandsgröße gearbeitet, ergibt sich für das ideale Gasgesetz:
(2.6) 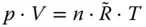
mit
n : Stoffmenge in mol,
allgemeine oder universelle Gaskonstante in J · mol–1 · K–1.
Die allgemeine Gaskonstante hat den Wert
(2.7) 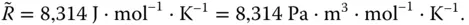
 Abbildung 2.8zeigt anhand eines einfachen Beispiels, wie das ideale Gasgesetz angewendet werden kann. In ein mit Wasser gefülltes Gefäß werden 5 mol Luft mit 20 °C (Temperatur des gesamten Systems aus Wasser und Luft) bei einem Druck 1,013 · 10 5Pa geleitet. Gesucht ist das Volumen, das die Luft einnimmt.
Abbildung 2.8zeigt anhand eines einfachen Beispiels, wie das ideale Gasgesetz angewendet werden kann. In ein mit Wasser gefülltes Gefäß werden 5 mol Luft mit 20 °C (Temperatur des gesamten Systems aus Wasser und Luft) bei einem Druck 1,013 · 10 5Pa geleitet. Gesucht ist das Volumen, das die Luft einnimmt.
Bei den gegebenen Bedingungen kann das ideale Gasgesetz verwendet werden. Formel 2.6wird nach dem Volumen V aufgelöst:
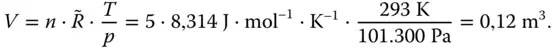
Die Luft nimmt bei diesen Bedingungen ein Volumen von 0,12 m 3oder 120 l ein.
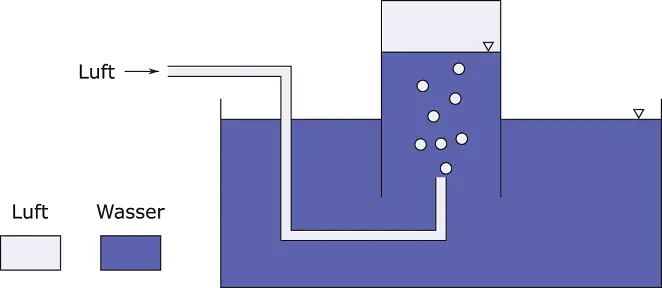
Abbildung 2.8Beispiel für das ideale Gasgesetz
Was ist jetzt eigentlich ein Mol?
Lassen Sie uns kurz über das Mol diskutieren, das Nichtchemikern immer irgendwie suspekt erscheint. Eine Masse lässt sich wiegen, da haben Sie etwas in der Hand. Sie kennen vielleicht noch die Standardfrage aus Kindestagen: »Was ist schwerer, 1 kg Blei oder 1 kg Federn?« Die Antwort war häufig: 1 kg Blei natürlich. Heute wissen Sie, dass diese Antwort nicht wirklich richtig ist. Dennoch, die Masse ist uns geläufig, wir wiegen uns (manchmal lassen wir das auch lieber), wir kaufen Waren in Masseeinheiten und schauen hier auf den spezifischen Preis, der in €/kg angegeben ist, um Warenpreise miteinander vergleichen zu können. Nirgendwo finden Sie €/mol!
Schauen Sie sich zuerst die Definition des Mols an.
 1 mol ist die Stoffmenge eines Systems, das aus ebenso vielen Einzelteilchen besteht, wie Atome in 0,012 kg des Kohlenstoffisotops 12C enthalten sind.
1 mol ist die Stoffmenge eines Systems, das aus ebenso vielen Einzelteilchen besteht, wie Atome in 0,012 kg des Kohlenstoffisotops 12C enthalten sind.
Auch wenn Ihnen diese Definition immer noch nicht so ganz behagt, hat sie doch eine ganz wichtige Bedeutung: 1 mol eines Stoffs enthält immer die gleiche Anzahl von Einzelteilchen. Diese Einzelteilchen können zum Beispiel Atome oder Moleküle sein.
 Die Teilchenzahl in der Stoffmenge 1 mol ist die Avogadro-Konstante N A. Diese besagt, dass ein Mol immer aus N A= 6,022 · 10 23Teilchen besteht.
Die Teilchenzahl in der Stoffmenge 1 mol ist die Avogadro-Konstante N A. Diese besagt, dass ein Mol immer aus N A= 6,022 · 10 23Teilchen besteht.
Avogadro bezieht die Teilchenzahl also nicht auf das Volumen, sondern auf ein Mol. Das ist rechentechnisch bei großen Teilchenzahlen auch irgendwie einfacher. Oder wollen Sie mit der kaum nachvollziehbar großen Summe von 6,022 · 10 23Teilchen rechnen? Da ist es doch besser, Sie haben ein Mol.
 Stellen Sie sich vor, Sie wollen Reis und Weizen kaufen. Sie kaufen jeweils 1 kg. Es würde Ihnen nicht einfallen, in den Laden zu gehen und von der Verkäuferin 33.333 Reiskörner zu verlangen. So viele Reiskörner sind nämlich bei einem Gewicht von circa 0,03 g pro Korn in einem Kilo enthalten. Der Einfachheit halber verlangen Sie sicherlich größere Gebinde. Wenn Sie Weizen kaufen, müssten Sie 20.000 Weizenkörner verlangen, da 1 Weizenkorn mit 0,05 g etwas schwerer ist als ein Reiskorn. Auch hier verlangen Sie ein Kilo. Sie verlangen ja auch keine 1000 Tropfen Bier! Der Wirt erschlägt Sie. Wir sind noch nicht beim Mol, ich weiß, aber Sie sehen, es ist sinnvoll, in größeren Einheiten zu rechnen. Beim Kilogramm haben Sie das Problem, dass die Anzahl der Reiskörner und die Anzahl der Weizenkörner in so einem Kilogramm unterschiedlich ist. Das stört Sie nicht, aber den Chemiker. Daher will er kein Kilogramm mit einer unbestimmten Teilchenzahl, sondern ein Mol mit immer exakt der gleichen Teilchenzahl.
Stellen Sie sich vor, Sie wollen Reis und Weizen kaufen. Sie kaufen jeweils 1 kg. Es würde Ihnen nicht einfallen, in den Laden zu gehen und von der Verkäuferin 33.333 Reiskörner zu verlangen. So viele Reiskörner sind nämlich bei einem Gewicht von circa 0,03 g pro Korn in einem Kilo enthalten. Der Einfachheit halber verlangen Sie sicherlich größere Gebinde. Wenn Sie Weizen kaufen, müssten Sie 20.000 Weizenkörner verlangen, da 1 Weizenkorn mit 0,05 g etwas schwerer ist als ein Reiskorn. Auch hier verlangen Sie ein Kilo. Sie verlangen ja auch keine 1000 Tropfen Bier! Der Wirt erschlägt Sie. Wir sind noch nicht beim Mol, ich weiß, aber Sie sehen, es ist sinnvoll, in größeren Einheiten zu rechnen. Beim Kilogramm haben Sie das Problem, dass die Anzahl der Reiskörner und die Anzahl der Weizenkörner in so einem Kilogramm unterschiedlich ist. Das stört Sie nicht, aber den Chemiker. Daher will er kein Kilogramm mit einer unbestimmten Teilchenzahl, sondern ein Mol mit immer exakt der gleichen Teilchenzahl.
 Jetzt aber wieder zum Mol. Ich will Ihnen zeigen, welche Vorteile diese Einheit gegenüber dem Kilogramm hat, speziell natürlich, wenn es um chemische Reaktionen geht. In Abbildung 2.9sind die drei Gase Wasserstoff (H 2), Stickstoff (N 2) und Methan (CH 4) gezeigt. Alle drei Gase nehmen mit
Jetzt aber wieder zum Mol. Ich will Ihnen zeigen, welche Vorteile diese Einheit gegenüber dem Kilogramm hat, speziell natürlich, wenn es um chemische Reaktionen geht. In Abbildung 2.9sind die drei Gase Wasserstoff (H 2), Stickstoff (N 2) und Methan (CH 4) gezeigt. Alle drei Gase nehmen mit 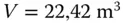 das gleiche Volumen ein. Der Druck und die Temperatur sind bei allen drei Gasen ebenfalls identisch
das gleiche Volumen ein. Der Druck und die Temperatur sind bei allen drei Gasen ebenfalls identisch 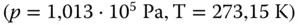 . Nun müssen Sie etwas in Ihren chemischen Grundlagen wühlen oder sich in Abbildung 2.10das Periodensystem der Elemente anschauen. Dann sehen Sie, dass 1 Mol Wasserstoff als Molekül (H 2) 2 g wiegt, Stickstoff als Molekül (N 2) 28 g und dementsprechend Methan
. Nun müssen Sie etwas in Ihren chemischen Grundlagen wühlen oder sich in Abbildung 2.10das Periodensystem der Elemente anschauen. Dann sehen Sie, dass 1 Mol Wasserstoff als Molekül (H 2) 2 g wiegt, Stickstoff als Molekül (N 2) 28 g und dementsprechend Methan 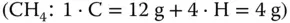 16 g. Da Sie alles auf ein Mol beziehen, müssen laut Avogadro alle drei Gase die gleiche Anzahl an Gasmolekülen enthalten, nämlich 6,022 · 10 23Teilchen pro Mol. Da die Masse von Wasserstoff am kleinsten ist, die Anzahl der Teilchen aber genauso groß ist wie bei den zwei anderen Gasen, können Sie daraus schließen, dass die Wasserstoffatome am kleinsten sein müssen. Sie können bei allen drei Gasen mit 1 Mol arbeiten, obwohl die Gase unterschiedliche Massen aufweisen. Aus Abbildung 2.9können Sie ebenfalls herauslesen, dass 1 Mol eines Gases bei einer Temperatur von 273,15 K und einem Druck von 1,013 · 10 5Pa ein Volumen von 22,42 m 3einnimmt.
16 g. Da Sie alles auf ein Mol beziehen, müssen laut Avogadro alle drei Gase die gleiche Anzahl an Gasmolekülen enthalten, nämlich 6,022 · 10 23Teilchen pro Mol. Da die Masse von Wasserstoff am kleinsten ist, die Anzahl der Teilchen aber genauso groß ist wie bei den zwei anderen Gasen, können Sie daraus schließen, dass die Wasserstoffatome am kleinsten sein müssen. Sie können bei allen drei Gasen mit 1 Mol arbeiten, obwohl die Gase unterschiedliche Massen aufweisen. Aus Abbildung 2.9können Sie ebenfalls herauslesen, dass 1 Mol eines Gases bei einer Temperatur von 273,15 K und einem Druck von 1,013 · 10 5Pa ein Volumen von 22,42 m 3einnimmt.
Читать дальше

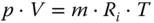
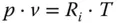
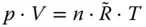
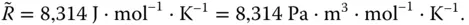
 Abbildung 2.8zeigt anhand eines einfachen Beispiels, wie das ideale Gasgesetz angewendet werden kann. In ein mit Wasser gefülltes Gefäß werden 5 mol Luft mit 20 °C (Temperatur des gesamten Systems aus Wasser und Luft) bei einem Druck 1,013 · 10 5Pa geleitet. Gesucht ist das Volumen, das die Luft einnimmt.
Abbildung 2.8zeigt anhand eines einfachen Beispiels, wie das ideale Gasgesetz angewendet werden kann. In ein mit Wasser gefülltes Gefäß werden 5 mol Luft mit 20 °C (Temperatur des gesamten Systems aus Wasser und Luft) bei einem Druck 1,013 · 10 5Pa geleitet. Gesucht ist das Volumen, das die Luft einnimmt.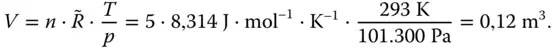

 1 mol ist die Stoffmenge eines Systems, das aus ebenso vielen Einzelteilchen besteht, wie Atome in 0,012 kg des Kohlenstoffisotops 12C enthalten sind.
1 mol ist die Stoffmenge eines Systems, das aus ebenso vielen Einzelteilchen besteht, wie Atome in 0,012 kg des Kohlenstoffisotops 12C enthalten sind.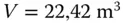 das gleiche Volumen ein. Der Druck und die Temperatur sind bei allen drei Gasen ebenfalls identisch
das gleiche Volumen ein. Der Druck und die Temperatur sind bei allen drei Gasen ebenfalls identisch 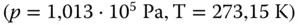 . Nun müssen Sie etwas in Ihren chemischen Grundlagen wühlen oder sich in Abbildung 2.10das Periodensystem der Elemente anschauen. Dann sehen Sie, dass 1 Mol Wasserstoff als Molekül (H 2) 2 g wiegt, Stickstoff als Molekül (N 2) 28 g und dementsprechend Methan
. Nun müssen Sie etwas in Ihren chemischen Grundlagen wühlen oder sich in Abbildung 2.10das Periodensystem der Elemente anschauen. Dann sehen Sie, dass 1 Mol Wasserstoff als Molekül (H 2) 2 g wiegt, Stickstoff als Molekül (N 2) 28 g und dementsprechend Methan 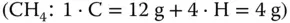 16 g. Da Sie alles auf ein Mol beziehen, müssen laut Avogadro alle drei Gase die gleiche Anzahl an Gasmolekülen enthalten, nämlich 6,022 · 10 23Teilchen pro Mol. Da die Masse von Wasserstoff am kleinsten ist, die Anzahl der Teilchen aber genauso groß ist wie bei den zwei anderen Gasen, können Sie daraus schließen, dass die Wasserstoffatome am kleinsten sein müssen. Sie können bei allen drei Gasen mit 1 Mol arbeiten, obwohl die Gase unterschiedliche Massen aufweisen. Aus Abbildung 2.9können Sie ebenfalls herauslesen, dass 1 Mol eines Gases bei einer Temperatur von 273,15 K und einem Druck von 1,013 · 10 5Pa ein Volumen von 22,42 m 3einnimmt.
16 g. Da Sie alles auf ein Mol beziehen, müssen laut Avogadro alle drei Gase die gleiche Anzahl an Gasmolekülen enthalten, nämlich 6,022 · 10 23Teilchen pro Mol. Da die Masse von Wasserstoff am kleinsten ist, die Anzahl der Teilchen aber genauso groß ist wie bei den zwei anderen Gasen, können Sie daraus schließen, dass die Wasserstoffatome am kleinsten sein müssen. Sie können bei allen drei Gasen mit 1 Mol arbeiten, obwohl die Gase unterschiedliche Massen aufweisen. Aus Abbildung 2.9können Sie ebenfalls herauslesen, dass 1 Mol eines Gases bei einer Temperatur von 273,15 K und einem Druck von 1,013 · 10 5Pa ein Volumen von 22,42 m 3einnimmt.










