1 ...6 7 8 10 11 12 ...17 Hierbei orientieren wir uns an der Leitlinie der Dt. Gesellschaft für Neurologie, deren Gültigkeit allerdings abgelaufen ist, sowie an aktuellen Übersichtsartikeln (Rosenow 2012; Strzelczyk et al. 2018; Strzelczyk und Rosenow 2018).
2.4.1 Verlauf des Status in 4 Phasen
Klinisch hat sich eine Unterscheidung des Status in vier Phasen bewährt. Diese finden sich im Folgenden. Die Behandlung erfolgt stufenadaptiert.
2.4.2 Stufe 1: Initialphase
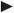 Die Behandlung eines konvulsiven Status epilepticus soll schnellstmöglich beginnen, auch schon prähospital.
Die Behandlung eines konvulsiven Status epilepticus soll schnellstmöglich beginnen, auch schon prähospital. 
Ein beginnender CSE soll schnellstmöglich behandelt werden. Benzodiazepine sind die Mittel der 1.Wahl, auch schon prähospital. Für die Initialtherapie durch Laien oder Ersthelfer empfiehlt sich die Gabe von Midazolam buccal oder nasal. Vorteile sind rasche Resorption und leichte Applizierbarkeit. Diazepam rektal wird ebenfalls schnell resorbiert, ist in der Handhabung aber schwieriger und bei Applikation in der Öffentlichkeit stigmatisierend für die Betroffenen. Benzodiazepine oral oder Lorazepam-Schmelztabletten sublingual sind aufgrund ihrer längeren Resorptionszeit für die Statustherapie nicht zu empfehlen.
Bereits prähospital erfolgt häufig durch den Notarzt eine Behandlung mit Benzodiazepinen intravenös (i. v.) oder auch durch den Rettungsdienst nasal oder buccal. Nach i. v. Applikation werden Diazepam und Midazolam schnell ins Gewebe umverteilt und haben somit eine kürzere intrazerebrale Wirksamkeit als Lorazepam und Clonazepam. Bewährt hat sich intrahospital die Therapieeinleitung mit Lorazepam i. v. Aufgrund der längeren Wirksamkeit ist die Möglichkeit eines Anfallsrezidivs geringer, sodass oft keine weitere Therapieeskalation erforderlich ist.
Eine Übersicht über verschiedene Benzodiazepine gibt Tabelle 2.1.
Tab. 2.1: Benzodiazepine zur Statusbehandlung
MedikamentÜbliche Initialdosis (i. v., Erwachsene)Empfohlene i. v.-DosierungApplikationsart
2.4.3 Stufe 2: etablierter Status
Wenn der Status nach der Initialbehandlung mit Benzodiazepinen nicht sistiert, ist eine antiepileptische Schnellaufsättigung i.v. erforderlich. Dies gilt in der Regel auch nach initialer Gabe eines Benzodiazepins mit kurzer antiepileptischer Wirksamkeit (Diazepam oder Midazolam) zur Vermeidung erneut auftretender Anfälle.
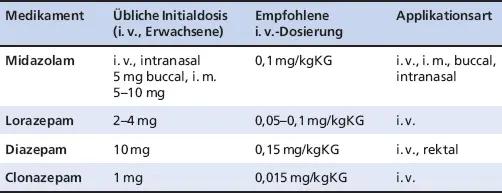
In Tabelle 2.2 sind die i.v. applizierbaren AED zusammengefasst.
Tab. 2.2: Intravenös applizierbare AED
MedikamentÜbliche Initialdosis (beim Erwachsenen)Empfohlene i.v. DosierungInfusionsgeschwindigkeit
* Unter Intubationsbereitschaft
Über Jahrzehnte war Phenytoin in der Behandlung der Stufe 2 das Mittel der Wahl. Es wird auch noch in der jüngsten Version der Leitlinie der Deutschen Gesellschaft für Neurologie (dgn.org/leitlinien/2303-ll-2a-2012-status-epilepticus-im-erwachsenenalter) empfohlen (Rosenow 2012). Problematisch ist das Nebenwirkungsspektrum (Hypotonie, kardiale Arrhythmien, Gewebetoxizität). Die Gabe soll unter Kreislaufmonitoring und idealerweise über einen zentralen Venenkatheter erfolgen. Zumindest muss die Gabe über einen gesonderten, sicher liegenden und großlumigen i. v. Zugang erfolgen. Seit kurzem ist das im Vergleich zur Injektionslösung besser verträgliche Infusionskonzentrat nicht mehr verfügbar.
Die folgenden Substanzen sind Alternativen, z. B. bei Kontraindikationen gegen Phenytoin i. v.:
Levetiracetam hat ein deutlich geringeres Wechselwirkungs- und Nebenwirkungspotential. In vielen Zentren wird es in der Stufe 2 der Statusbehandlung präferiert, insbesondere bei kardial vorerkrankten Patienten. Levetiracetam ist für die Statusbehandlung zwar nicht zugelassen, in den DGN-Leitlinien wird aber Folgendes ausgeführt: »Die Datenlage zu Levetiracetam ist mittlerweile so robust, dass diese Substanz als alternatives Medikament in der 2. Therapiestufe (nach Gabe eines Benzodiazepins) in Betracht gezogen werden kann«.
Valproinsäure ist in der Statusbehandlung vergleichsweise gut verträglich, bei Lebervorschädigung, Vorliegen einer Pankreatitis oder Einnahme von Marcumar jedoch problematisch. Bei Mitochondriopathie ist Valproinsäure kontraindiziert.
Lacosamid ist für die Statusbehandlung nicht zugelassen. Es scheint vor allem bei Patienten ohne Natrium-Kanal-Blocker in der Komedikation einen guten Effekt zu haben. Bei Vorliegen eines AV-Blocks II oder III ist Lacosamid kontraindiziert.
Wichtig:
Wenn Anfälle nach Behandlung in Stufe 2 nicht sistieren, ist die Diagnose zu überprüfen und ein Status psychogener nichtepileptischer Anfälle zu erwägen (  Kap. 3).
Kap. 3).
2.4.4 Stufe 3: refraktärer Status
Wenn der Status nach der Behandlung in Stufe 2 nicht sistiert und seine epileptische Natur feststeht, handelt es sich um einen refraktären Status epilepticus. Es ist die Einleitung einer therapeutischen Narkosebehandlung unter EEG-Monitoring erforderlich. Aufgrund des günstigeren Nebenwirkungsprofils sind dabei Midazolam oder Propofol dem Thiopental vorzuziehen.
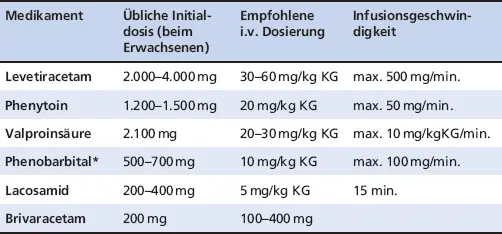
Tabelle 2.3 listet Medikamente zur therapeutischen Intubationsnarkose auf.
Tab. 2.3: Narkotika
MedikamentInitialer BolusErhaltungsdosis
Das vorrangige Therapieziel der Narkosebehandlung unter EEG-Kontrolle ist die vollständige Anfallssuppression. Das Erreichen eines Burst-Suppression-Musters im EEG wird häufig angestrebt, ist aber nach neueren Daten möglicherweise nicht notwendig (Hocker et al. 2013). Eine komplette EEG-Suppression sollte nicht erfolgen. Nach 24 Stunden sollte sich eine Aufwachphase über 6 bis 12 Stunden anschließen, während der das Wiederauftreten von Anfallsaktivität im EEG sorgfältig zu beobachten ist.
2.4.5 Stufe 4: superrefraktärer Status
Persistiert ein Status auch nach 24-stündiger therapeutischer Intubationsnarkose, ist er superrefraktär. Es gibt für die Behandlung keine evidenzbasierten Empfehlungen. Prinzipiell können alle enteral und parenteral verfügbaren AED eingesetzt werden. Es gibt Fallberichte zum Einsatz von ketogener Diät, Ketamin, Magnesium, Steroiden, Immunglobulinen und Hypothermie. Bei Vorliegen einer läsionellen Epilepsie ist auch die Durchführung eines notfallmäßigen epilepsiechirurgischen Eingriffs eine prüfbare Option.
2.4.6 Notfallbehandlung nach klinikinternem Algorithmus
Ein einheitlicher klinikinterner Behandlungsalgorithmus ist bei der Behandlung des CSE entscheidend.
Abbildung 2.3 zeigt das entsprechende Behandlungsschema aus dem Krankenhaus Mara, Epilepsiezentrum Bethel, erstellt in Anlehnung an (Trinka et al. 2015b).
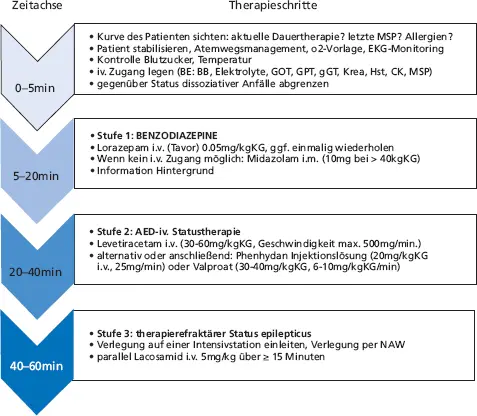
Abb. 2.3: Beispiel für einen klinikinternen Behandlungsalgorithmus: Behandlungsschema für den CSE, Epilepsiezentrum Bethel, Krankenhaus Mara
Читать дальше

 Die Behandlung eines konvulsiven Status epilepticus soll schnellstmöglich beginnen, auch schon prähospital.
Die Behandlung eines konvulsiven Status epilepticus soll schnellstmöglich beginnen, auch schon prähospital. 


 Kap. 3).
Kap. 3).












