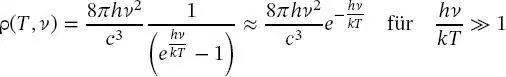Max Planck versuchte, das beobachtete Emissionsprofil mithilfe der klassischen Theorie auf der Basis von schwingenden atomaren Dipoloszillatoren (Kerne und Elektronen) zu reproduzieren. Dieser Versuch ergab, dass die Strahlungsdichte ρ , die ein klassischer Schwarzer Körper als Funktion von ν und T in ein Frequenzband dv abgibt, durch (1.5)beschrieben werden kann:
(1.5) 
Hier ist k die Boltzmann-Konstante ( k = 1,381 · 10 −23J/K). Dieses Ergebnis deutet, dass die Gesamtenergie, die ein Schwarzer Körper nach diesem ,,klassischen“ Modell ausstrahlt, mit ν 2zunimmt, wie die gestrichelte Kurve in Abb. 1.2b zeigt. Wenn diese Gleichung korrekt wäre, dann wäre jede Temperatur eines Materials über dem absoluten Nullpunkt unmöglich, da jedes Material über dem absoluten Temperaturnullpunkt uneingeschränkt Strahlung gemäß (1.5)emittieren und die ausgestrahlte Gesamtenergie unendlich würde. Insbesondere in Richtung einer höheren Frequenz würde immer mehr Strahlung emittiert werden und der Schwarze Körper würde sich augenblicklich auf 0K abkühlen. Daher wäre jede Temperatur über 0K unmöglich. (Für eine detailliertere Diskussion dieser ,,UV-Katastrophe“ siehe Engel und Reid [2].)
Dies steht natürlich im Widerspruch zu experimentellen Ergebnissen und wurde von Max Planck (1901) dadurch gelöst, dass er den Term 1/( ehv/(kT) — 1) in die Schwarzkörpergleichung einführte, wobei h die Planck’sche Konstante ist:
(1.6) 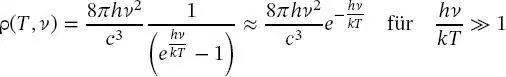
Die Form des modifizierten Schwarzkörperemissionsprofils nach (1.6)stimmt mit den experimentellen Ergebnissen überein. Der von Planck eingeführte neue Faktor ist im Grunde genommen eine exponentielle Abklingfunktion, die das gesamte Emissionsprofil zwingt, sich bei hoher Frequenz null zu nähern. Der Zähler des Exponentialausdrucks enthält die Größe hv , wobei h die Planck’sche Konstante ist ( h = 6,626 · 10 −34J s). Dieser Zähler impliziert, dass Licht als „Quanten“ oder Lichtteilchen (Photonen) mit der Energie E existiert, wobei
(1.7) 
Dies war ein revolutionärer Gedanke, da die Welleneigenschaften des Lichts seit mehr als zwei Jahrhunderte zuvor bekannt und im späten 19. Jahrhundert durch Maxwell’s Gleichungen als Funktionen der elektrischen und magnetischen Felder beschrieben waren. Hier ergab sich zum ersten Mal die Erkenntnis, dass je nach Fragestellung zwei unterschiedliche Beschreibungen des Lichts in Bezug auf Wellen und Partikel angebracht waren. Ein ähnlicher ,,Teilchen-Wellen-Dualismus“ wurde später auch für Materie postuliert und bestätigt. So ist die Arbeit von Planck im frühen 20. Jahrhundert wirklich die Geburtsstunde der Ideen, die zur Formulierung der Quantenmechanik führten.
Im Übrigen ist die Form des Ausdrucks 1/( e hv/(kT)) oder e −hv/(kT)in der klassischen physikalischen Chemie nicht unbekannt. Er vergleicht die Energie eines Ereignisses, beispielsweise eines Moleküls, das die Flüssigkeit für die Gasphase verlässt, mit dem Energieinhalt der Umgebung. Zum Beispiel hängt der Dampfdruck einer reinen Flüssigkeit von einem Faktor e −ΔHvap/(RT)ab, wobei Δ H vapdie Verdampfungsenthalpie der Flüssigkeit ist und RT = NkT ist Energie bei der Temperatur T, R ist die Gaskonstante und N ist die Avogadro-Zahl. Ebenso ist die Abhängigkeit der Reaktionsgeschwindigkeitskonstante und der Gleichgewichtskonstante von der Temperatur durch äquivalente Ausdrücke gegeben, die die Aktivierungsenergie bzw. die Reaktionsenthalpie im Zähler des Exponenten enthalten. In (1.6)wird die Photonenenergie durch den Energieinhalt des emittierenden Materials dividiert und liefert eine Wahrscheinlichkeit für das Auftreten dieses Ereignisses.
Abbildung 1.2a zeigt, dass die emittierte Gesamtenergie mit zunehmender Temperatur zunimmt und dass sich die Spitzenwellenlänge maximaler Intensität zu einer niedrigeren Wellenlänge hin verschiebt (Wien’sches Gesetz). Die von einem Schwarzen Körper pro Flächeneinheit und Zeiteinheit in einem Raumwinkel abgestrahlte Gesamtenergie W (die sogenannte Bestrahlungsstärke), über alle Wellenlängen integriert, ist der absoluten Temperatur zur vierten Potenz proportional:
(1.8) 
Die Bestrahlungsstärke wird in Einheiten von W/(m 2s sr) oder Photonen/(m 2s sr) ausgedrückt. Die Implikation des oben erwähnten Welle-Teilchen-Dualismus wird im nächsten Abschnitt diskutiert.
1.3 Der photoelektrische Effekt
Im Jahr 1905 berichtete Einstein über experimentelle Ergebnisse, die die Energiequantelung von Licht weiter demonstrierten. In dem photoelektrischen Experiment beleuchtete Licht variabler Farbe (Frequenz) eine in einer evakuierten Röhre enthaltene Photokathode. Eine Anode in derselben Röhre war extern mit der Kathode über einen Strommesser und einer Batterie verbunden. Da die Kathode und die Anode durch ein Vakuum getrennt waren, wurde kein Strom beobachtet, es sei denn, wenn Licht mit einer Frequenz über einer Schwellenfrequenz die Photokathode beleuchtete. Einstein folgerte, dass Lichtteilchen oder Photonen mit einer Frequenz oberhalb dieses Schwellenwerts ausreichende kinetische Energie besitzen, um Elektronen aus den Metallatomen der Photokathode herauszuschlagen. Diese ,,Photo-elektronen“ verlassen die Metalloberfläche mit einer kinetischen Energie E kin:
(1.9) 
Dabei ist φ die Austrittsarbeit oder die Energie, die erforderlich ist, um ein Elektron aus den Metallatomen zu entfernen. Diese Energie ist im Grunde die Ionisierungsenergie eines Atoms multipliziert mit der Avogadro-Konstante. Darüber hinaus berichtete Einstein, dass der durch die Bestrahlung der Photokathode erzeugte Photostrom proportional zur Lichtintensität oder zur Anzahl der Photonen war. Eine Erhöhung der Lichtintensität mit einer Frequenz unterhalb des Schwellenwerts erzeugte jedoch keinen Photostrom. Dies lieferte einen weiteren Beweis für (1.9).
Dieses Experiment zeigte weiter, dass Licht einen Teilchencharakter hat, wo die kinetischen Energie der Photonen durch (1.7)gegeben ist. Dies führte weiterhin zum Konzept des Welle-Teilchen-Dualismus des Lichts. Später theoretisierte de Broglie, dass der Impuls p eines Photons durch
(1.10) 
gegeben sei. Gleichung (1.10)ist als De-Broglie-Gleichung bekannt. Der Welle-Teilchen-Dualismus wurde später (1927) auch für bewegte Massen durch das Elektronenbeugungsexperiment von Davisson und Germer bestätigt. In diesem Experiment wurde ein Elektronenstrahl durch ein Atomgitter gebeugt und erzeugte ein deutliches Interferenzmuster, das darauf hindeutete, dass sich bewegende Elektronen Welleneigenschaften zeigten. Der Welle-Teilchen-Dualismus von Photonen und bewegter Materie kann wie folgt zusammengefasst werden:
Читать дальше