KOCHSALZ HILFT BEIM GAREN Kochsalz (NaCl) wirkt nicht nur als Aromenverstärker und natürlicher Geschmacksverstärker (  salzig, Seite 53), sondern beschleunigt außerdem den Garprozess: Gemüse wird schneller weich, weil die Ionen Na +und Cl -die ionischen Bindungen über Ladungen lockern: Erstens scharen sich die positiven Natriumionen um die negativen Ladungen der Pektine. Die Calciumbindung der Pektine wird dabei schwächer, die Molekülketten werden flexibler (in der Physik ist der Effekt als Debye-Hückel-Abschirmung bekannt). Auch auf die Bindung der Hemicellulosen an die Cellulosefasern hat Kochsalz einen lockernden Einfluss: Natrium- und Chloridionen binden Wasser, dabei wird die Bindung zwischen Hemicellulosen und Cellulosen schwächer. Und zum Dritten verändert die erhöhte „ionische Stärke“ durch die Salzzugabe die Form und Stabilität der Glycoproteine, deren strukturgebende Eigenschaften durch einwertige Ionen aus Natriumchlorid oder Kaliumchlorid geschwächt werden. Aus diesen Gründen kann man mit einer Zugabe von Salz das Garwerden von Gemüse beschleunigen. Das gilt im Übrigen auch für getrocknete Bohnen und andere Hülsenfrüchte. Selbst wenn man das oft hört oder liest – die Zugabe von Salz verlängert nicht die Kochzeit von Kichererbsen & Co., im Gegenteil!
salzig, Seite 53), sondern beschleunigt außerdem den Garprozess: Gemüse wird schneller weich, weil die Ionen Na +und Cl -die ionischen Bindungen über Ladungen lockern: Erstens scharen sich die positiven Natriumionen um die negativen Ladungen der Pektine. Die Calciumbindung der Pektine wird dabei schwächer, die Molekülketten werden flexibler (in der Physik ist der Effekt als Debye-Hückel-Abschirmung bekannt). Auch auf die Bindung der Hemicellulosen an die Cellulosefasern hat Kochsalz einen lockernden Einfluss: Natrium- und Chloridionen binden Wasser, dabei wird die Bindung zwischen Hemicellulosen und Cellulosen schwächer. Und zum Dritten verändert die erhöhte „ionische Stärke“ durch die Salzzugabe die Form und Stabilität der Glycoproteine, deren strukturgebende Eigenschaften durch einwertige Ionen aus Natriumchlorid oder Kaliumchlorid geschwächt werden. Aus diesen Gründen kann man mit einer Zugabe von Salz das Garwerden von Gemüse beschleunigen. Das gilt im Übrigen auch für getrocknete Bohnen und andere Hülsenfrüchte. Selbst wenn man das oft hört oder liest – die Zugabe von Salz verlängert nicht die Kochzeit von Kichererbsen & Co., im Gegenteil!
WARUM EINE GESALZENE GEMÜSEBRÜHE STÄRKER DUFTET ALS EINE UNGESALZENE In wässriger Umgebung lösen sich nur wenige der flüchtigen Aromastoffe (  Flüchtigkeit und Löslichkeit, Seite 19). Dass überhaupt Aroma in die Gemüsebrühe gelangt und sich nicht alles verflüchtigt, liegt an der leichten Polarität der Wassermoleküle. Diese sind am Sauerstoffatom leicht negativ, an den beiden Wasserstoffatomen leicht positiv „geladen“, orientieren sich daher gemäß ihrer Dipol-Dipol-Wechselwirkung zueinander und können einzelne kleine, hydrophobe Moleküle in einem Wasser-„Käfig“ einschließen (
Flüchtigkeit und Löslichkeit, Seite 19). Dass überhaupt Aroma in die Gemüsebrühe gelangt und sich nicht alles verflüchtigt, liegt an der leichten Polarität der Wassermoleküle. Diese sind am Sauerstoffatom leicht negativ, an den beiden Wasserstoffatomen leicht positiv „geladen“, orientieren sich daher gemäß ihrer Dipol-Dipol-Wechselwirkung zueinander und können einzelne kleine, hydrophobe Moleküle in einem Wasser-„Käfig“ einschließen (  siehe Abbildung, Seite 70). Der Käfig wird durch Wassermoleküle der unmittelbaren Umgebung mit der der Polarität entsprechenden Orientierung stabilisiert. Befinden sich die so hydratisierten Aromastoffe in der Nähe der Luft-Wasser-Grenzfläche, bricht die Hydrathülle wegen der veränderten Umgebung auf. Das hydrophobe Molekül geht in die Dampfphase über und erreicht so die Nase (oder auch die Detektoren des Chromatografen, die mit sogenannten „headspace“-Verfahren Aromastoffe direkt nachweisen) – die Gemüsebrühe duftet.
siehe Abbildung, Seite 70). Der Käfig wird durch Wassermoleküle der unmittelbaren Umgebung mit der der Polarität entsprechenden Orientierung stabilisiert. Befinden sich die so hydratisierten Aromastoffe in der Nähe der Luft-Wasser-Grenzfläche, bricht die Hydrathülle wegen der veränderten Umgebung auf. Das hydrophobe Molekül geht in die Dampfphase über und erreicht so die Nase (oder auch die Detektoren des Chromatografen, die mit sogenannten „headspace“-Verfahren Aromastoffe direkt nachweisen) – die Gemüsebrühe duftet.
RELEVANTE TEMPERATURBEREICHE BEIM GEMÜSEGAREN
40 – 60 °C: Die Zellmembran (aus Phospholipiden) beginnt weicher und flexibler zu werden. Die Zellwände verändern sich nicht.
50 °C: Enzyme werden aus den Zellmembranen freigesetzt, z. B. Enzyme, die Vitamin C abbauen oder bei grünem Gemüse für Grauverfärbung verantwortlich sind. Die Zellwände verändern sich nicht.
60 – 68 °C: Enzyme werden inaktiviert, z. B. Enzyme, die Vitamin C abbauen. Blanchiertemperaturen sollten daher 68 °C Kerntemperatur erreichen. Die Zellwände bleiben stabil, die Zellen sind immer noch prall mit Zellwasser gefüllt, die Textur der Gemüse ist nach wie vor „knackig“.
70 – 75 °C: Hemicellulosen und Pektine beginnen sich zu verändern, sie brechen nach und nach ab und lösen sich von den Cellulosefasern. Der Zelldruck wird höher, Zellwände platzen an manchen Stellen auf, das Wasser aus den Zellen tritt aus.
85 – 90 °C: Die Zellwände werden immer weniger stabil, das Gemüse wird weich, ohne dass dabei die Cellulosefasern brechen.
90 – 100 °C: Wegen der fehlenden Bindung der Hemicellulosen und des Pektinnetzwerks separieren sich die Zellen, das Gemüse „zerkocht“ nach und nach. Gleichzeitig lösen sich immer mehr der ionischen Calciumverbindungen.
Wird Natriumchlorid (NaCl) zugegeben, entstehen einwertige positive Natriumionen (Na +) und negativ geladene Chloridionen (Cl -), die selbst eine starke Hydrathülle um sich bilden. Die Wechselwirkung in der Nähe der hydratisierten Aromen wird durch die Ionen stark gestört, weil die Wechselwirkung der polaren Wassermoleküle mit den Ionen (wegen des Coulombfelds um die Ionen) stärker ist und eine höhere Reichweite hat. Im Konkurrenzkampf um das Hydratwasser gewinnen die Ionen des Salzes, die Hydrathüllen der Aromastoffe werden schwächer und brechen auf. Die Löslichkeit der hydrophoben Stoffe wird dadurch schlechter. Bei höherer Konzentration der apolaren Aromastoffe können diese sich leichter zu Tröpfchen zusammenlagern, die von den Wasserkäfigen nicht mehr gehalten werden können. In der Nähe der Luft-Wasser-Grenzfläche brechen die Käfige noch rascher auf. Die Konzentration der hydrophoben Duftstoffe in der Dampfphase über der gesalzenen Gemüsebrühe ist damit höher.
Die unterschiedlichen Ionenradien des jeweiligen Salzes (beispielsweise von Natrium und Kalium) spielen dabei ebenfalls eine wichtige Rolle, denn sie definieren zusammen mit der Ionenladung, wie viele Wassermoleküle um die jeweiligen Ionen Platz finden und wie groß die Hydrathülle ist.
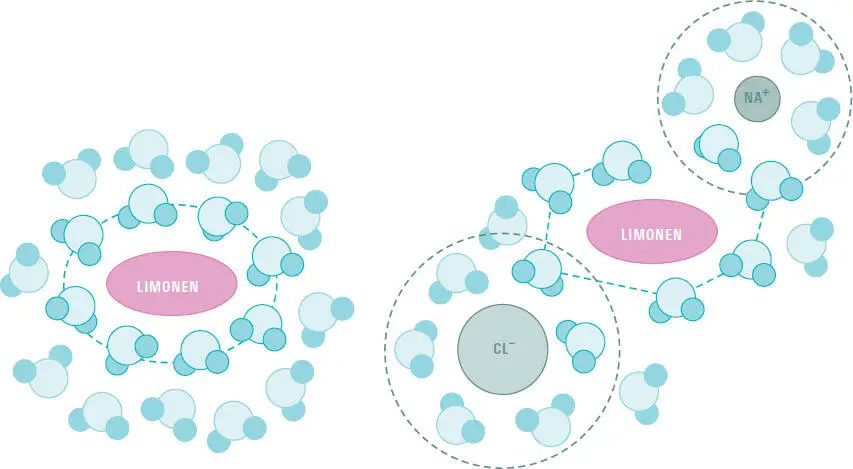
Hydrophobe Moleküle, z. B. Limonen (rote Ellipse), werden von polaren Wassermolekülen in Hydrathüllen eingefangen (links). Kommen Natrium und Chloridionen hinzu, entsteht ein Kampf um das Wasser, den das Salz wegen der elektrischen Ladung gewinnt. Die Hydrathüllen brechen auf, die Aromastoffe werden deutlich rascher flüchtig und erreichen die Nase.
DER PH-WERT BEEINFLUSST FESTIGKEIT UND FARBE VON GEMÜSE Der Ladungszustand der Pektine und Hemicellulosen ist deutlich pH-abhängig. Garen in saurer Umgebung bei pH-Werten zwischen 3 und 6 erhält die Festigkeit von Gemüse: Die Hemicellulosen lassen sich schlechter lösen, die äußere Schicht des Gemüses bleibt, trotz Garung, fester. Was bei der stärkereichen Kartoffel eher unerwünscht ist – in Sauerkraut mitgegarte Kartoffeln bleiben unangenehm hart –, ist bei Wurzelgemüse wie Karotten, Pastinaken oder Sellerie, das man in säuerlicher Umgebung, beispielsweise in einer Tomatensauce, gart, von Vorteil. Es bilden sich gegarte Aromen (z. B. das karamellig-suppige SOTOLON beim Sellerie) und das Gemüse ist vollkommen gar, bleibt aber dennoch schön fest. Der Nachteil bei dieser Methode ist, dass das Gemüse Farbe verliert und grau wird.
Garen in alkalischer Umgebung (bei pH-Werten zwischen 7 und 9) hingegen hat genau den gegenteiligen Effekt: Es lässt Gemüse weicher werden und erhält die Farbe. Die Löslichkeit der Pektine und Hemicellulosen wird bei hohen pH-Werten verbessert, da sie mehr Wasserstoffprotonen abgeben. Das Netzwerk zwischen den Pektinen wird daher rascher „weich“, die Textur weniger fest. Die Gemüsefarbe bleibt deutlich besser erhalten, insbesondere bei Chlorophyll, weil dessen Zentralion Magnesium in basischer Umgebung weniger rasch oxidiert. In der Küche lässt sich dafür das klassische Hausnatron (Natriumhydrogencarbonat, NaHCO 3) verwenden. Löst sich dieses in Wasser, sorgt das Carbonatanion für die Erhöhung des pH-Werts. Die basische OH-Gruppe (alkalisch) geht in Lösung und bildet kein Proton (sauer). Diese Methode empfiehlt sich beispielsweise bei grünen Gartenbohnen oder Erbsen. Die Garung erfolgt rascher, und die Farbe des Gemüses bleibt leuchtend grün.
HARTES WASSER – FESTES GEMÜSE Gart man Gemüse in „hartem“ Wasser oder gibt eigens Calziumsalze hinzu, kann man die Festigkeit des Gemüses erhöhen. Die zweiwertigen Ionen Ca 2+im Kochwasser verhindern, dass sich die Calciumbindung der Pektine auch bei hohen Kochtemperaturen löst. Das Gemüse bleibt – ähnlich wie in saurer Umgebung – fester, ohne dass der Geschmack des Gerichts beeinflusst wird. Wichtig ist dies unter Umständen bei frittiertem Gemüse. Dieses bleibt länger knusprig, wenn es zuvor in einer Calciumlaktat- oder Calciumchloridlösung blanchiert wird. Das klassische Beispiel sind Pommes frites. Werden die Stäbchen in Calciumbäder gelegt (blanchiert), werden sie knuspriger. Ähnliches lässt sich auch nach einem Bad in „hartem“ Wasser beobachten.
Читать дальше

 salzig, Seite 53), sondern beschleunigt außerdem den Garprozess: Gemüse wird schneller weich, weil die Ionen Na +und Cl -die ionischen Bindungen über Ladungen lockern: Erstens scharen sich die positiven Natriumionen um die negativen Ladungen der Pektine. Die Calciumbindung der Pektine wird dabei schwächer, die Molekülketten werden flexibler (in der Physik ist der Effekt als Debye-Hückel-Abschirmung bekannt). Auch auf die Bindung der Hemicellulosen an die Cellulosefasern hat Kochsalz einen lockernden Einfluss: Natrium- und Chloridionen binden Wasser, dabei wird die Bindung zwischen Hemicellulosen und Cellulosen schwächer. Und zum Dritten verändert die erhöhte „ionische Stärke“ durch die Salzzugabe die Form und Stabilität der Glycoproteine, deren strukturgebende Eigenschaften durch einwertige Ionen aus Natriumchlorid oder Kaliumchlorid geschwächt werden. Aus diesen Gründen kann man mit einer Zugabe von Salz das Garwerden von Gemüse beschleunigen. Das gilt im Übrigen auch für getrocknete Bohnen und andere Hülsenfrüchte. Selbst wenn man das oft hört oder liest – die Zugabe von Salz verlängert nicht die Kochzeit von Kichererbsen & Co., im Gegenteil!
salzig, Seite 53), sondern beschleunigt außerdem den Garprozess: Gemüse wird schneller weich, weil die Ionen Na +und Cl -die ionischen Bindungen über Ladungen lockern: Erstens scharen sich die positiven Natriumionen um die negativen Ladungen der Pektine. Die Calciumbindung der Pektine wird dabei schwächer, die Molekülketten werden flexibler (in der Physik ist der Effekt als Debye-Hückel-Abschirmung bekannt). Auch auf die Bindung der Hemicellulosen an die Cellulosefasern hat Kochsalz einen lockernden Einfluss: Natrium- und Chloridionen binden Wasser, dabei wird die Bindung zwischen Hemicellulosen und Cellulosen schwächer. Und zum Dritten verändert die erhöhte „ionische Stärke“ durch die Salzzugabe die Form und Stabilität der Glycoproteine, deren strukturgebende Eigenschaften durch einwertige Ionen aus Natriumchlorid oder Kaliumchlorid geschwächt werden. Aus diesen Gründen kann man mit einer Zugabe von Salz das Garwerden von Gemüse beschleunigen. Das gilt im Übrigen auch für getrocknete Bohnen und andere Hülsenfrüchte. Selbst wenn man das oft hört oder liest – die Zugabe von Salz verlängert nicht die Kochzeit von Kichererbsen & Co., im Gegenteil!











