Zur peripheren Glia zählt man die Schwann-Zellen und die Satellitenzellen (siehe unten). Mit der Unterteilung des Nervensystems in einen peripheren- und einen zentralen Anteil werden wir uns im nächsten Kapitel noch beschäftigen. Hier wird aber schon deutlich, dass beide Anteile durch verschiedene zelluläre Komponenten gebildet werden.
Astrozyten
Die häufigsten Gliazellen im Gehirn sind die Astrozyten. Sie werden zu den Makrogliazellen gerechnet. Eine wichtige Funktion der Astrozyten besteht darin, das chemische Milieu des Extrazellulärraums zu regulieren. So umhüllen Astrozyten beispielsweise die Synapsen im Gehirn und begrenzen dadurch die Ausbreitung von freigesetzten Neurotransmittermolekülen. Spezielle Transporter-Proteine in den Membranen von Astrozyten entfernen Neurotransmitter aktiv aus dem synaptischen Spalt. Vor kurzem hat man entdeckt, dass Astrozytenmembranen nicht nur Transporter, sondern auch Rezeptoren für Neurotransmitter exprimieren können, die wie die Rezeptoren der Neuronen im Inneren der Gliazellen biochemische Reaktionen auslösen können. 4 , 5 Nervenzellen und Gliazellen können dadurch miteinander kommunizieren.
Morphologisch können zwei Arten von Astrozyten unterschieden werden: protoplasmatische (Astrocytus protoplasmaticus – auch: Kurzstrahler) und fibrillenreiche (Astrocytus fibrosus – auch: Langstrahler) Astrozyten. Protoplasmatische Astrozyten kommen vor allem in der grauen Substanz des Zentralnervensystems vor, fibrillenreiche überwiegend in der weißen Substanz ( Abb. 1.9).
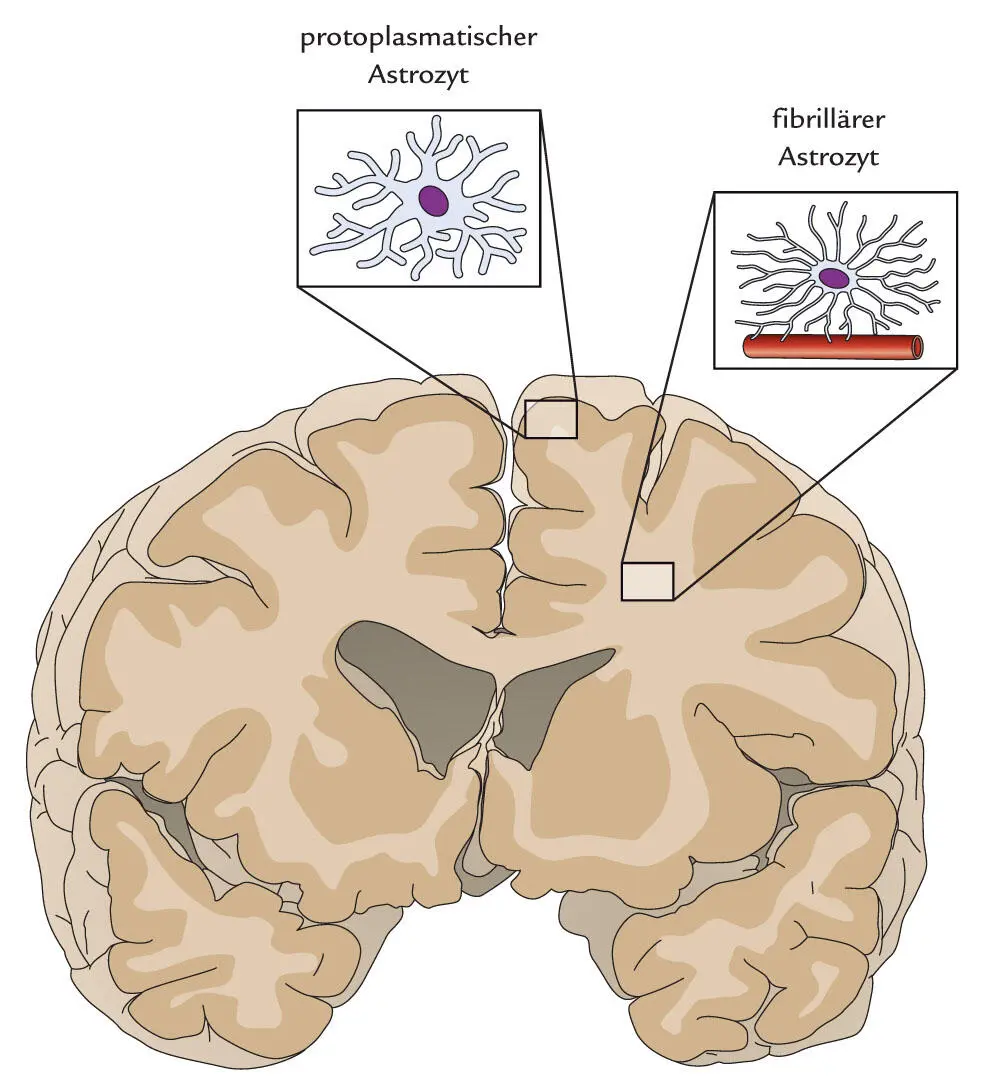
Abb. 1.9
Astrozyten
Astrozyten sind die häufigsten Gliazellen im Gehirn. Ihre Aufgabe besteht in der chemischen Regulation des Extrazellulärraums. Dies erreichen sie beispielsweise durch isolierende Eigenschaften oder das Ausbilden von Rezeptoren für Neurotransmitter. Man unterscheidet protoplasmatische Astrozyten, die größtenteils in der grauen Hirnsubstanz vorkommen, von fibrillenreichen Astrozyten, die in der weißen Substanz zu finden sind.
Astrozyten sind über Nexus (Gap junctions) verbunden und besitzen viele verzweigte Fortsätze, von denen einige an Blutgefäßen enden und hier eine Schicht aus Gliafüßchen aufbauen, die sogenannte Membrana limitans gliae perivascularis. Sie ist am Aufbau und der Funktion der Blut-Hirn-Schrankebeteiligt (einer Struktur, welche verhindert, dass Blutbestandteile ohne weiteres in das Gehirn eindringen können). Astrozyten der grauen Substanz sind darüber hinaus am Aufbau der sogenannten Membrana limitans gliae superficialisbeteiligt. Diese Grenzmembran, aufgebaut aus einer dichten Schicht von astrozytären Zellfortsätzen und einer direkt daran angrenzenden Basalmembran, stellt die äußere Grenzfläche des Hirngewebes dar. Jenseits der Basalmembran beginnt die weiche Hirnhaut (Pia mater, Abb. 1.10).
Abb. 1.10
Astrozyten übernehmen viele Aufgaben im Gehirn. Man unterscheidet die der weißen (fibrillären) und der grauen (protoplasmatischen) Sub-stanz. Unter anderem bilden sie isolierende Barrieren nach außen hin, entweder in Richtung Hirnoberfläche (Glia limitans superficialis, a) oder um Gefäße herum (Glia limitans perivascularis, b). Färbung gegen GFAP (Glial fibrillary acidic protein).
Die Funktion der Membrana limitans gliae superficialis besteht darin, das Eindringen von Erregern von außen zu verhindern.
Darüber hinaus sind Astrozyten an der sogenannten neurovaskulären Kopplung beteiligt. Die neurovaskuläre Kopplungist ein physiologischer Mechanismus zur Regulierung der Blutversorgung des Gehirns, um den Mehrbedarf von aktivem Nervengewebe an Sauerstoff und Glukose durch lokale Steigerung des Blutflusses zu decken. Was genau kann man sich unter dem Begriff neurovaskuläre Kopplung nun vorstellen? Wie funktioniert dieser Mechanismus, und welche Rolle spielen hierbei die Astrozyten? Lange Zeit ist man davon ausgegangen, dass eine Synapse aus exakt zwei Elementen besteht: der Axonterminalen der präsynaptischen Nervenzelle, und den Dornen (Spines) der postsynaptischen Nervenzelle. Man nannte dieses Modell bi-partite Synapse („bi“ steht hierbei für die Tatsache, dass zwei Partner beteiligt sind; eine solche Synapse ist in Abb. 1.5dargestellt, s. o.). Weitere Studien konnten zeigen, dass Fortsätze von Astrozyten einen sehr engen Kontakt mit diesen Synapsen eingehen, sie strecken quasi einen ihrer Fortsätze in bzw. um den synaptischen Spalt ( Abb. 1.11).
Abb. 1.11
Mechanismus der neurovaskulären Kopplung, vermittelt durch Astrozyten:
1Glutamat wird freigesetzt.
2Glutamat bindet u. a. an metabotrope Rezeptoren (mGluR) von umliegenden Astrozyten.
3Dies bewirkt die Aktivierung einer Signalkaskade im Innern der Astrozyten.
4Die Signalkaskade hat eine Ausschüttung von NO an einem peri-arteriellen Fortsatz zur Folge.
5NO ruft dort eine lokale Vasodilatation hervor.
Freigesetzter Neurotransmitter (hier dargestellt für eine erregende = exzitatorische Nervenzelle, welche Glutamat als Neurotransmitter benutzt) wird in Folge dessen nicht nur von der postsynaptischen Membran, sondern auch vom Fortsatz des Astrozyten gebunden und aktiviert dort einen metabotropen Glutamatrezeptor (mGluR). Die Aktivierung des metabotropen Glutamatrezeptors bewirkt innerhalb des Zellleibes der Astrozyten die Aktivierung verschiedener Signalkaskaden, welche schlussendlich dazu führen, dass an einem peri-arteriellen Fortsatz Stickstoffmonoxid (NO) ausgeschüttet wird. Das freigesetzte Stickstoffmonoxid führt zu einer lokalen Erweiterung (Vasodilatation) der Arteriole, und damit verbunden zu einem lokal begrenzten Anstieg des Blutstroms. Astrozyten koppeln über diesen Mechanismus neuronale Aktivität mit vaskulärer Dilatation, kurz neurovaskuläre Kopplung. 6 Dieser von Astrozyten vermittelte Mechanismus macht durchaus Sinn: Aktive Nervenzellen benötigen lokal mehr Sauerstoff und Glukose und sind deswegen auf eine vorübergehende Steigerung des Blutflusses angewiesen. Nicht zwei, sondern vielmehr drei Strukturen sind also am Aufbau einer Synapse beteiligt: Man spricht deswegen von einer tri-partiten Synapse.
Astrozyten haben, je nachdem in welchem Teil des Nervensystems sie sich befinden, eigene Namen. Bergmann-Glianennt man eine spezialisierte Astrozytenpopulation in Kleinhirn. Sie spielen dort unter anderem eine wichtige Rolle für die Migration der Nervenzellen während der Entwicklung. 7 Müller-Zellensind die Gliazellen der Retina. Diese versorgen die Ganglienzellen der Retina mit Nährstoffen und entfernen deren katabole Stoffwechselprodukte. Sie regulieren den pH-Wert und die Konzentration der Ionen im Extrazellulärraum. So nehmen sie z. B. Kaliumionen auf, welche die Bipolarzellen bei der Depolarisation in den Extrazellulärraum ausschütten und setzen sie bei Bedarf an anderer Stelle wieder frei („Kalium-Siphoning“). Ihnen wird darüber hinaus eine wichtige Funktion in der Entwicklung und bei regenerativen Prozessen zugeschrieben. 8 Zu guter Letzt gibt es noch die Pituizyten. Dies sind spezifische Gliazellen des Hypophysenhinterlappens (Neurohypophyse).
 Klinik
Klinik
Der Mechanismus der neurovaskulären Kopplung kann klinisch für die Darstellung neuronaler Aktivität(PET; Positronen-Emissions-Tomographie) ausgenutzt werden. Die Positronen-Emissions-Tomographie beruht im Wesentlichen auf einem lokalen Anstieg der zerebralen Durchblutung bei Gehirnaktivität, vermittelt durch Astrozyten. Eingesetzt wird diese Methode unter anderem bei der Diagnose des M. Parkinson. Hierbei handelt es sich um eine Störung dopaminerger Zellen. Radioaktiv markiertes Dopa hilft zusätzlich, die metabolische Störung im Striatum (dem beim M. Parkinson unter anderem betroffenen Gehirnteil) quantitativ darzustellen.
Читать дальше

 Klinik
Klinik










