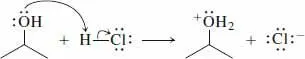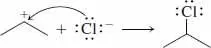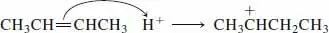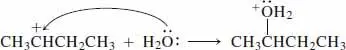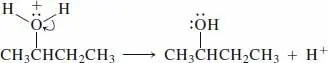Nucleophile: (a) und (d). In diesen Verbindungen haben I –bzw. S ein oder mehr freie Elektronenpaare, die sie zu Lewis-Basen machen. Diese können elektronenarme Atome, z. B. in Lewis-Säuren, angreifen.
Elektrophile: (b), (c), (e) und (f). In allen vier Spezies fehlen voll besetzte Außenschalen; alle sind Lewis-Säuren und können mit elektronenreichen Verbindungen wie Lewis-Basen (Nucleophilen) chemisch wechselwirken.
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
7 (g)
8 (h)
9 (i)
10 (j)
1 (a) Das δ+-Kohlenstoffatom (Pfeil) zieht das negativ geladene Sauerstoffatom des Hydroxid-Ions an.
2 (b) Das δ+-Kohlenstoffatom zieht das freie Elektronenpaar am δ–-Stickstoffatom von Ammoniak an. Gleichzeitig zieht das δ–-Sauerstoffatom ein δ+-Wasserstoffatom von Ammoniak an.
3 (c) Ein freies Elektronenpaar des δ–-Sauerstoffatoms bindet an H+
4 (d) Das δ+-Kohlenstoffatom des Ketons zieht das negativ geladene Kohlenstoffatom des Carbanions an.
5 (e) Das freie Elektronenpaar am Stickstoffatom wird vom positiv geladenen Kohlenstoffatom angezogen.
6 (f) Keine Reaktion. Butan hat keine polarisierten Atome und reagiert daher nicht mit geladenen oder polarisierten Spezies.
1 (a) Vgl. Beispiel 3(b) in Abschn. 2.2.
2 (b) Wie Beispiel 4(a), nur ist der Elektronenpaar-Donor neutral und nicht negativ.
3 (c) Ähnlich wie Beispiel 2, nur der Donor ist neutral.
4 (d)
5 (e) Wie Teil (c) oben
Wonach ist gefragt, und was haben wir? Sie sollen gebogene Pfeile zeichnen und damit drei Reaktionsschritte ergänzen. Im Kapitel haben Sie bereits Modelle für jeden Schritt gesehen.
Wie gehen wir vor? Ergänzen Sie alle Lewis-Formeln, sodass wir die Ausgangs- und Endpositionen aller Elektronen kennen.
Information: Bestimmen Sie jeden Reaktionstyp und suchen Sie ein analoges Beispiel.
Fahren Sie fort, indem Sie gebogene Pfeile hinzufügen, die mit denen in unseren Modellbeispielen übereinstimmen.
Schritt 1.Als Modell können wir Wasser + HCl verwenden (Abschn. 2.3).
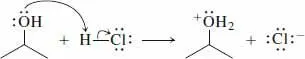
Das Sauerstoffatom wird durch die starke Säure protoniert, indem es ein Elektronenpaar an das acide Wasserstoffatom abgibt, wobei Chlorid frei wird.
Schritt 2.Dissoziation einer polaren kovalenten Bindung. Vergleichen Sie den Bruch der C–Br-Bindung in (CH 3) 3–Br (Abschn. 2.2, Beispiel 1(b). Also
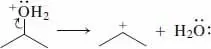
Die C–O-Bindung bricht auf, indem ihr Elektronenpaar auf das elektronegative und positiv geladene Sauerstoffatom übergeht; dabei bleibt die Ladung auf dem C-Atom und H 2O wird abgespalten.
Schritt 3.Ein nucleophiles Chlorid-Ion und ein elektrophiles positives C-Atom verbinden sich:
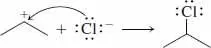
Suchen Sie wie bei Aufgabe 2.42 Modellbeispiele für jede Umwandlung und zeichnen Sie danach gebogene Pfeile, die die gleichen Bindungsänderungen bewirken.
Schritt 1.Als Modell können wir die Addition von H +an H 2C=CH 2nutzen, die als Beispiel 4b in Abschn. 2.2 beschrieben wurde. Also,
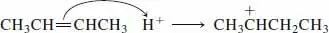
In diesem Schritt wird eine der CH-Gruppen der Doppelbindung zu CH 2umgewandelt, wobei auf dem anderen C-Atom der ursprünglichen Doppelbindung eine positive Ladung verbleibt. Damit erkennen wir, dass der Säurekatalysator die Aufgabe hat, ein positives und hoch elektrophiles Kohlenstoffatom zu bilden.
Schritt 2.Ein nucleophiles Wassermolekül bindet an das positive Kohlenstoffatom, indem es eins seiner freien Elektronenpaare am Sauerstoffatom abgibt und eine Bindung bildet:
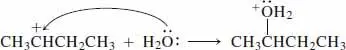
Das Produkt dieses Schritts enthält ein Sauerstoffatom mit drei Bindungen und einer positiven Ladung. Die an solche Sauerstoffatome gebundenen Wasserstoffatome sind stark sauer, wie Sie es von Hydronium-Ion kennen. Der letzte Schritt ist eine logische Folge:
Schritt 3.Eine der O–H-Bindungen wird getrennt, wenn ihr Elektronenpaar auf das positiv geladene Sauerstoffatom übergeht. Das Resultat ist die Abspaltung eines H +, womit der in Schritt 1 verbrauchte Protonenkatalysator regeneriert wird.
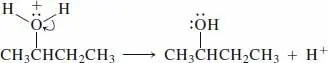
Vermeiden Sie unbedingt den sehr häufigen Fehler, die Deprotonierung mit einem Pfeil zu zeigen, der am Wasserstoffatom beginnt und ins Leere geht. Das ist keine Chemie, nicht einmal gute Sciencefiction.
Bedenken Sie, dass Kurzstrukturformeln nur zeigen, welche Atome miteinander verknüpft sind, nicht aber die tatsächliche räumliche Anordnung eines Moleküls. Die längste Kette ist die Kette mit den meisten Atomen; das ist nicht unbedingt die in der Aufgabenstellung horizontal gezeichnete.
1 (a) 2,3-Dimethylpentan
2 (b) Die Hauptkette ist bereits horizontal; man nummeriert von links nach rechts (Nonan): 2-Methyl-5-(1-methylethyl)-5-(1-methylpropyl)nonan.
3 (c) 3,3-Diethylpentan, wie man es auch betrachtet.
4 (d) Hauptkette: 10 Kohlenstoffatome, 4-Ethyl-3,4,5-trimethyl-5-(2-methylpropyl)decan
5 (e) Umzeichnen: 2,3,4,5-Tetramethylhexan
6 (f) Hexan (lassen Sie sich nicht durch die Art der Darstellung beirren).
7 (g) 2-Methylpropan. (Methylpropan wäre genauso richtig. Die Methylgruppe kann nur an C2 angefügt werden, damit ist die Ziffer überflüssig.) Wenn nötig, zeichnen Sie diese und die nächsten drei Formeln unter Darstellung aller Atome um.
8 (h) 2,2-Dimethylbutan
9 (i) 2-Methylpentan
10 (j) 2,5-Dimethyl-4-(1-methylethyl)heptan
1 (a) Pentan ist kein korrekter Stammname. Der richtige Name ist 3-Ethyl-2-methylhexan.
2 (b) Der Name ist korrekt.
3 (c) Das ist kein Heptan. Der Name ist 2,3,4-Trimethyl-4-propyloctan.
4 (d) Hauptkette und Nummerierung sind falsch. Der korrekte Name lautet 4-(1,1-Dimethylethyl)-2,3-dimethylheptan.
5 (e) Die Hauptkette ist falsch. Die Verbindung heißt 3-Ethyl-5-propylundecan.
6 (f) Die Nummerierung muss umgekehrt erfolgen. Die Verbindung heißt 2,2,4-Trimethylpentan.
7 (g) Die Hauptkette ist falsch, sie widerspricht der Regel der „maximalen Zahl von Substituenten“. Die Verbindung heißt 3-Methyl-4-propylheptan.
8 (h) Isoheptan ist ein Trivialname: Beachten Sie die (CH3)2CH-Gruppe am Ende der sonst geraden Kette. IUPAC-Name: 2-Methylhexan.
9 (i) Ebenfalls ein Trivialname: Neo bezeichnet die endständige (CH3)3C-Gruppe. Der IUPAC-Name ist 2,2-Dimethylpentan.
1 (a) Der Name ist falsch. Die Nummerierung muss umgekehrt (von rechts nach links) erfolgen, sodass man 3-Chlor-2-methylhexan erhält.
Читать дальше