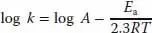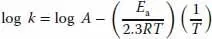2 (b) Ea = 125.6 kJ/mol = 125 600 J/mol(1) Für eine Temperaturerhöhung um 10 K erhält man(2) Für eine Temperaturerhöhung um 30 K erhält man k330 K = 96.9k300 K(3) Für eine Temperaturerhöhung um 50 K erhält man k350 K = 1320k300 K
3 (c) Ea = 188.4 kJ/mol = 188 400 J/mol(1) Für eine Temperaturerhöhung um 10 K erhält man(2) Für eine Temperaturerhöhung um 30 K erhält man k330 K = 958.6k300 K(3) Für eine Temperaturerhöhung um 50 K erhält man k330 K = 48 480k300 K
Wir fassen die gerundeten Ergebnisse in einer Tabelle zusammen:
| E a= |
62.8 kJ/mol |
125.6 kJ/mol |
188.4 kJ/mol |
| k 310 K/ k 300 K |
2 |
5 |
10 |
| k 330 K/ k 300 K |
10 |
100 |
1 000 |
| k 350 K/ k 300 K |
40 |
1300 |
50 000 |
Diese Aufgabe veranschaulicht die Wirkung einer Temperaturänderung auf die Geschwindigkeitskonstanten von Reaktionen mit drei verschiedenen Aktivierungsenergien. Daraus ergibt sich Folgendes:
1 Reaktionen mit hohen Aktivierungsenergien sind gegenüber Temperaturänderungen am empfindlichsten.
2 Auch Reaktionen mit niedrigeren Aktivierungsenergien sprechen recht signifikant selbst auf moderate Temperaturerhöhungen an. Das ist deshalb von Bedeutung, weil die Aktivierungsenergien vieler Reaktionen in der organischen (und biologischen) Chemie zwischen 60 und 120 kJ/mol liegen.
Die allgemeine Geradengleichung mit der Auftragung x gegen y lautet: y = (Achsenabschnitt) + (Steigung)( x ). Vergleichen Sie diese mit der Gleichung in der Aufgabe:
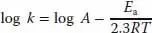
Durch Ausklammern Terms 1/ T erhalten Wir
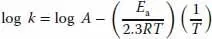
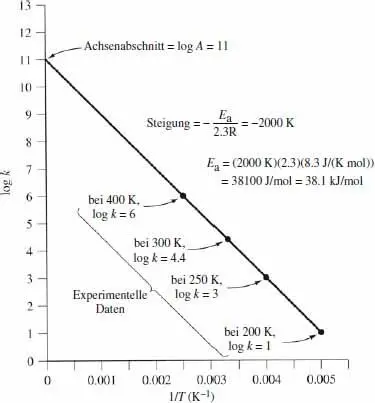
Vergleicht man diese Gleichung mit einer Geradengleichung, erkennt man, dass der Graph log k gegen 1/ T die Steigung –( E a/2.3 R ) und den Achsenabschnitt lg A hat. Demzufolge ergibt sich E adurch Multiplizieren der Geradensteigung mit –2.3 R . Ein solcher Graph sieht beispielsweise so aus:
1 (a) Es gibt hier ein kleines Problem: Das positiv polarisierte Kohlenstoffatom in Bromethan hat eine vollbesetzte Schale und ist daher nicht Lewis-acid. Zu weiteren Reaktionen von Halogenalkanen mit Lewis-Basen siehe Aufgabe 2.61.
2 (b)
3 (c)
4 (d)
5 (e)
1 (a) Aus 2.54(a) haben wir ΔG° = –5.53 kJ/mol. T = 298 K und ΔS° = +5.9 J/(mol K) = +5.9 × 10–3 kJ/(mol K). Daher muss ΔG = ΔH° – TΔS° umgeformt und nach ΔH° aufgelöst werden: ΔH° = ΔG° + TΔS° = –5.53 + 298(+5.9 × 10–3) = –5.53 + 1.76. ΔH° = –3.77 kJ/mol.Dieser Wert stimmt sehr gut mit dem Wert ΔH° = –3.8 kJ/mol überein, der in Aufgabe 2.54(b),(c) aus der Zahl der gauche-Wechselwirkungen in der 0°-Konformation relativ zur 120°-Konformation berechnet wurde.
2 (b) Vergessen Sie nicht, °C in K umzuwandeln und 273 zu addieren!
3 (c) Verwenden Sie ΔG° = –RT ln K = –2.303RT lg K. Das lässt sich umformen zu – ΔG°/(2.303RT) = lg K oder K = 10–Δ/G(2.303RT)(1) Bei T = –250 °C = 23 K, ΔG° = –3.91 kJ/mol = –3910 J/mol; –ΔG°/(2.303RT) = –[–3910/(2.303 × 8.414 × 23)] = 8.65 – lg K, daraus folgt K = 4.5 × 108.(2) Bei T = –100°C = 173 K, ΔG° = –4.79 kJ/mol = –4790 J/mol; –ΔG°/(2.303RT) = –[–4790/(2.303 × 8.314 × 173)] – 1.42 = lg K, damit ist K = 26.(3) Bei T = 500°C = 773K, ΔG° = –8.33 kJ/mol = –8330J/mol; –ΔG°/(2.303RT) = –[–8330/(2.303 × 8.314 × 773)] – 0.55 = lg K, damit ist K = 3.5.
Wir können die Ergebnisse der Übungen 2.60 und 2.54 in einer kleinen Tabelle zusammenfassen:
| T (K) |
Δ G ° |
K |
| 23 |
–3.91 |
4.5 × 10 8 |
| 173 |
–4.79 |
26 |
| 298 |
–8.33 |
9 |
| 773 |
–5.53 |
3.5 |
Diese Werte verdeutlichen zwei Punkte. Am offensichtlichsten ist der große Effekt der Temperatur auf K . Bei 23 K (das ist sehrkalt) haben nur zwei von einer Milliarde Molekülen 2-Methylbutan die energiereichere Konformation (0°)! Die Umgebung enthält nur sehr wenig thermische Energie für eine Bindungsrotation. Bei höheren Temperaturen nehmen die Werte für K hingegen ab, da die steigende thermische Energie immer mehr Molekülen den Übergang in weniger stabile Konformationen ermöglicht. Die Δ S °-Werte bewirken ebenfalls eine Änderung von Δ G ° mit der Temperatur, der Effekt ist allerdings gering, weil Δ S ° klein ist.
Es ist allgemein empfehlenswert, die gegebenen Informationen zu nutzen: Notieren Sie die Fakten so, dass Sie sie vor Augen haben, bevor Sie versuchen, die Frage zu beantworten.
1 (a) Diese Reaktion läuft 10 000-mal langsamer ab als die obere.
2 (b) Die Reaktionszentren sind in den obigen Strukturformeln durch Punkte gekennzeichnet. Beide sind primäre Kohlenstoffatome, denn sie sind mit nur einem weiteren Kohlenstoffatom direkt verknüpft.
3 (c) Aus elektrostatischen Gründen sollte das negative Iodid-Ion vom positiv polarisierten Kohlenstoffatom der C–Br-Bindung angezogen werden. Da dieses Kohlenstoffatom jedoch bereits eine voll besetzte Schale hat, kann das Iodid eigentlich kein Elektronenpaar zur Bindung beisteuern, wenn nicht ein anderes Atom, z. B. das Bromatom, abgespalten wird und ein Elektronenpaar mitnimmt. Die Kinetik zweiter Ordnung spricht nicht für eine Sequenz, in der das Bromid-Ion abgespalten wird, bevor das Iodid-Ion eintritt. Daher laufen beide Vorgänge höchstwahrscheinlich gleichzeitig ab:Die gegenüber der ersten Reaktion wesentlich geringere Reaktionsgeschwindigkeit der zweiten Umsetzung lässt darauf schließen, dass die in diesem Fall größere Alkylgruppe das Iodid-Ion hindert, an das Kohlenstoffatom zu binden (zu einem Beispiel für sterische Hinderung siehe Abschn. 2.8). Diese Annahme ist dann sinnvoll, wenn das Iodid-Ion zum Knüpfen der Bindung nahe an dieser Alkylgruppe vorbei muss, vielleicht auf einer Bahn ähnlich der nachstehend skizzierten:
4 (d)
3
Die Reaktionen der Alkane
Bindungsdissoziationsenergien, radikalische Halogenierung und relative Reaktivität
3.15
Diese Übung gehört eigentlich noch zum vorherigen Kapitel. Der Kürze wegen verwenden wir die Symbole 1° = primär, 2° = sekundär und 3° = tertiär.
1 (a)
2 (b)
3 (c)
4 (d) In Kapitel 4werden Sie erfahren, dass die meisten “Ringverbindungen” genauso betrachtet werden können wie Moleküle ohne Ringe.
1 (a) Beachten Sie, dass Radikale anhand des radikalischen Kohlenstoffatoms als primär, sekundär oder tertiär zugeordnet werden. Alle anderen Kohlenstoffatome spielen hierbei keine Rolle. Die Hyperkonjugation im 1-Methylpropyl-Radikal lässt sich auf zwei Arten darstellen: durch Überlappung von zwei C–H-Bindungen mit dem radikalischen p-Orbital oder unter Beteiligung einer C–C-Bindung anstelle einer C–H-Bindung:
2 (b) Bei der Benennung ist zu beachten, dass das radikalische Kohlenstoffatom immer C1 ist (genau wie das „verknüpfende“ Kohlenstoffatom in Alkylgruppen). Der Stammname basiert auf der längsten, mit C1 beginnenden Kohlenstoffkette, alle „Anhänge” werden als Substituenten benannt:
Читать дальше