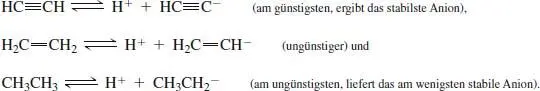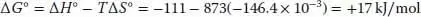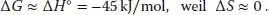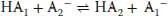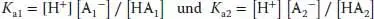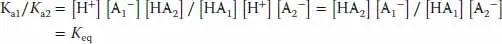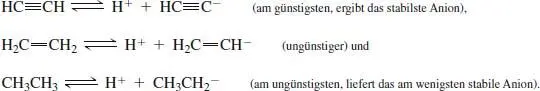
Damit hat die Säurestärke die Reihenfolge HC≡CH > H 2C=CH 2> CH 3CH 3.
e > c > d > a > b. Zunächst das Kation; bei den anderen Verbindungen hängt der positive Charakter des Kohlenstoffatoms von der Zahl der (polarisierten) Bindungen zu elektronegativen Atomen ab.
Die Buchstaben in der folgenden Strukturformel entsprechen den Buchstaben in der Übung. In einigen Fällen sind nur repräsentative Bindungen oder Atome bezeichnet
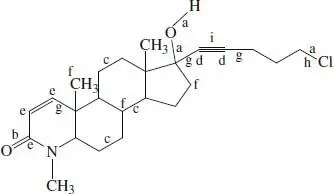
1 (a)
2 (b) und (c)
3 (d) Das δ+-Kohlenstoffatom, das vom Cyanid-Ion angegriffen wird, hat bereits ein Oktett. Um die Oktettregel nicht zu verletzen, muss ein Elektronenpaar der Doppelbindung auf das Sauerstoffatom übergehen.
2
Struktur und Reaktivität: Säuren und Basen, polare und unpolare Moleküle
2.31
Um diese Aufgabe zu lösen, gehen wir davon aus, dass der Raum mit dem Ofen vom umgebenden Universum isoliert ist. Sobald Sie den Ofen ausgeschaltet haben, bleibt der Wärmeinhalt des Systems „Raum + Ofen“ unabhängig vom Stand der Ofentür konstant. Durch Öffnen der Tür verteilt sich der hohe Wärmegehalt des Ofens in den Raum, bis beide im Gleichgewicht dieselbe Temperatur haben, aber die Gesamtenthalpie bleibt konstant. Dagegen führt die Verteilung der Wärmeenergie vom Ofen in den Raum zu einer positiven Gesamtänderung der Entropie. Da Δ S ° positiv ist und Δ G ° = Δ H ° – T Δ S ° gilt, können wir schlussfolgern, dass die Änderung der freien Energie negativ ist, was einem thermodynamisch günstigen Gesamtprozess entspricht. Machen Sie nun weiter und genießen Ihre Pizza!
1 (a) Berücksichtigen Sie die Beziehung(i) Um den ΔH°-Wert für das Aufbrechen einer der beiden Bindungen in der Kohlenstoff-Kohlenstoff-Doppelbindung zu berechnen, verwenden wir ΔH°(C=C) als Beitrag für den Bindungsbruch und ΔH°(C–C) als Beitrag für die Bindungsbildung:(ii)
2 (b) Bei der Reaktion (i) verbinden sich zwei Moleküle zu nur einem Molekül. Dadurch konzentriert sich der Energieinhalt des Systems auf weniger Teilchen, sodass für Reaktion (i) ein hoher negativer Wert für ΔS° (–146.4 Entropieeinheiten) resultiert. Man könnte auch sagen, das System wird „geordneter“, was praktisch das Gleiche bedeutet. In Reaktion (ii) entstehen aus zwei Molekülen zwei andere Moleküle. Die Verteilung des Energieinhalts des Systems ändert sich nicht wesentlich, daher beträgt ΔS° annähernd Null.
3 (c) Für (i) bei 25 °C
Für (i) bei 600 °C
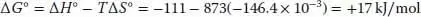
Für (ii) gilt bei 25 °C wie bei 600 °C:
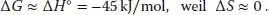
Für beide Reaktionen ist Δ G ° bei 25 °C negativ, daher sind beide thermodynamisch günstig. Bei 600 °C macht der Wert von Δ S ° für Reaktion (i) Δ G ° positiv: Die Reaktion ist daher energetisch ungünstig. Reaktion (ii) verläuft noch ebenso gut wie bei 25 °C.
Überlegen Sie, welche Verbindungen Protonen abgeben, bevor Sie versuchen, die Säuren zu bestimmen; viele der hier aufgeführten Verbindungen können als Säure wie als Base wirken! Das Gleichgewicht liegt aufseiten des schwächeren Säure-Base-Paars, wie die unterschiedlich langen Pfeile für Hin-und Rückreaktion andeuten. Mithilfe von Tab. 2.2 können Sie die stärkeren Säuren anhand ihres größeren K a- oder kleineren (weniger positiven oder stärker negativen) p K a-Werts bestimmen. Die Gleichgewichtskonstante für jede Reaktion erhält man, indem man den K a-Wert der Säure auf der linken Seite durch den K a-Wert der Säure auf der rechten Seite dividiert. Hierzu kommt man folgendermaßen: Für die allgemeine Reaktion
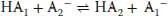
gilt
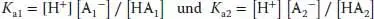
Damit ist
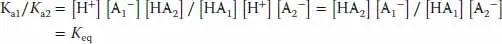
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
1 (a) Die Pfeile sind richtig. Ein Elektronenpaar bewegt sich vom negativen und nucleophilen Kohlenstoff- zum H-Atom, wobei ein Elektronenpaar aus der O–H-Bindung frei wird und auf das positiv geladene Sauerstoffatom übergeht.
2 (b) Falsch. Auch wenn es so aussieht, als bewege sich das H-Atom in die richtige Richtung, ist die Elektronenbewegung umgekehrt – sie sollte vom negativen N-Atom zum δ+-H-Atom gehen, wobei die Elektronen der O–H-Bindung auf das elektronegative Sauerstoffatom übergehen:
3 (c) Wieder falsch, aus dem gleichen Grund. Es stimmt zwar, dass F das elektronegativste Element ist, und Sie könnten versucht sein, Elektronen dorthin zu verschieben, aber es hat bereits eine negative Ladung und ein vollständiges Oktett. Es gibt keinen Platz für ein weiteres Elektronenpaar. Verschieben Sie die Elektronen wie bei (b) in die andere Richtung:
4 (d) und (e) sind richtig.
5 (f) ist ganz falsch. Wie bei (b) und (c) zeigen wir mit Zwei-Elektronen-Pfeilen die Bewegung eines H-Atoms, das keine Elektronen mitnimmt! Noch schlimmer ist, dass der zweite Pfeil die Verschiebung eines fünften Elektronenpaars zu einem O-Atom zeigt, das negativ geladen ist und bereits ein Oktett hat. So ist es richtig:
1 (a) CN– ist eine Lewis-Base
2 (b) CH3OH ist eine Lewis-Base
3 (c) (CH3)2CH+ ist eine Lewis-Säure
4 (d) MgBr2 ist eine Lewis-Säure
5 (e) CH3BH2 ist eine Lewis-Säure
6 (f) CH3S– ist eine Lewis-Base
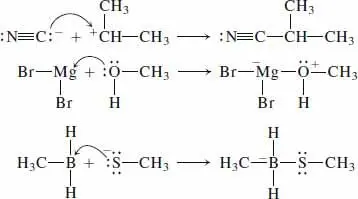
Bei der Lösung des zweiten Teils wollen wir geschickt vorgehen. Wir haben drei Lewis-Säuren und drei Lewis-Basen. Wir fassen sie zu Paaren zusammen und beantworten die Frage mit nur drei Reaktionsgleichungen. Aus Gründen der Übersicht wurden die drei freien Elektronenpaare an jedem Halogenatom weggelassen:
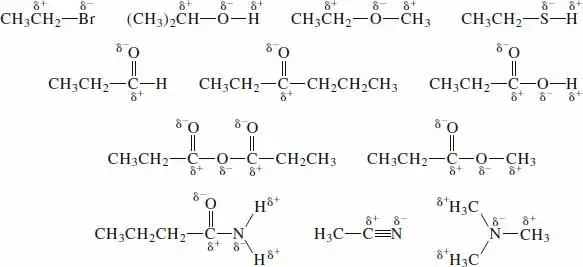
Verwenden Sie eine Elektronegativitätstabelle, um die Bindungspolaritäten zu bestimmen. Butan, 2-Methylpropen, 2-Butin und Methylbenzol haben keine polarisierten Bindungen. Die anderen Verbindungen haben die hier gezeigten polarisierten Bindungen.
 Читать дальше
Читать дальше