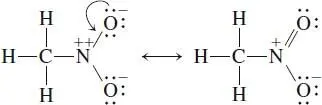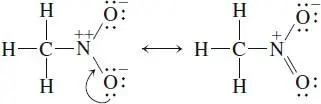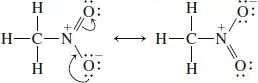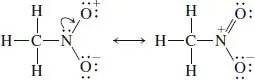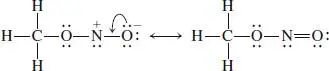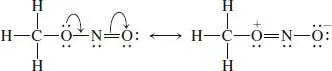7 (g) Alle drei Nichtwasserstoffatome haben zumindest einmal eine Doppelbindung, daher sind alle sp2-hybridisiert. C und N sind trigonal-planar, am O ist die Anordnung gewinkelt mit einem freien Elektronenpaar in einem sp2-Orbital.
8 (h) Das links stehende Kohlenstoffatom hat vier Einfachbindungen, es ist sp2-hybrdisiert und tetraedrisch. Das mittlere C- und das N-Atom sind in der mittleren Struktur dreifach gebunden und demzufolge sp-hybridisiert und linear.
Beachten Sie vor Beginn, dass die Aufgabenstellung angibt, wie die Atome verknüpft sind: Beide Verbindungen haben zwei N–O-Bindungen, daher steht das N-Atom bei Nitromethan in der Mitte. Wir beginnen mit den σ -Bindungen:
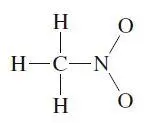
Die Valenzschalen des Kohlenstoffatoms und der Wasserstoffatome sind damit besetzt, aber dem Stickstoffatom und den Sauerstoffatomen fehlen Elektronen. Wir haben aber 24 Elektronen zur Verfügung (3 von den H-Atomen + 4 von C + 5 von N + 12 von den O-Atomen), davon sind erst 12 in den 6 Bindungen verbraucht. Wir können die übrigen 12 verwenden, um an jedes O-Atom drei freie Elektronenpaare anzufügen. Danach benennen wir die formalen Ladungen an den Atomen:
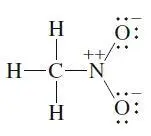
Das ist eine „erlaubte“ Lewis-Formel, wir haben keine Regeln verletzt und die O-Atome haben Oktetts erhalten, allerdings hat das N-Atom nur ein Sextett und die Ladung 2+. Lässt sich das verbessern? Wir verschieben ein Elektronenpaar vom negativen zum positiven Atom und sehen uns das Ergebnis an.
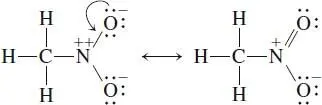
Schon besser: N hat nun ebenfalls ein Oktett. Wir hätten natürlich auch ein Elektronenpaar vom anderen Sauerstoffatom verschieben können. Das Ergebnis ist das gleiche wie eben, nur die N–O-Einfachbindung und die N=O-Doppelbindung sowie die zugehörige negative Ladung sind vertauscht:
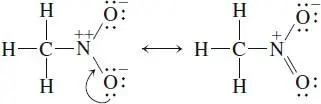
Könnte man zwei Elektronenpaare zum N verschieben, eins von jedem O-Atom? Nein: Das würde die Oktettregel am N verletzen und zu einer verbotenen Lewis-Struktur führen:
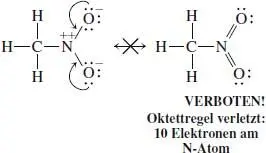
Die beiden besten Strukturen sind demnach die oben erhaltenen mit Oktetts an allen Nichtwasserstoffatomen und einem Ladungspaar. Die Pfeile darunter kennzeichnen die Verschiebung der Elektronenpaare beim Übergang von einer Struktur zur anderen:
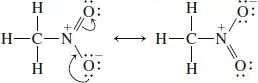
Da die beiden Formeln gleich sind, ist ihr Beitrag zum Resonanzhybrid gleich groß. Die N–O-Bindungen sind polar, wobei N die positive Gesamtladung trägt und die negative Ladung je zur Hälfte auf die beiden O-Atome verteilt ist.
Sie fragen sich vielleicht, was geschehen wäre, wenn man zu Beginn dieser Übung zunächst eins der übrigen Elektronenpaare am N-Atom platziert hätte, anstatt alle auf die Sauerstoffatome zu verteilen? Gute Frage! In unserer Ausgangsstruktur (unten, links) hätten dann das N-Atom und eins der O-Atome ein Oktett, aber das andere O-Atom hätte ein Sextett. Durch Verschieben des freien Elektronenpaars vom N-zum elektronenarmen O-Atom gelangen wir zur gleichen Endstrukturen wie oben:
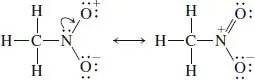
Demzufolge gilt: Solange alle σ -Elektronen an Ort und Stelle bleiben und wir mit den übrigen die Oktettregel nicht verletzen, führt jede Ausgangsstruktur letztlich zu der/den besten Lösung(en).
Betrachten wir nun Methylnitrit. Wir gehen genauso vor und beginnen nur mit Einfachbindungen, danach fügen wir die übrigen Elektronen als freie Elektronenpaare beliebig an, wobei wir nur darauf achten, die Oktettregel nicht zu verletzen. Ein Ergebnis ist die Struktur unten links, sie enthält ein stark elektronenarmes N-Atom, wie wir es zunächst auch bei Nitromethan erhalten haben. Wir „stabilisieren“ es auf die gleiche Weise, indem wir ein Elektronenpaar vom negativ geladenen endständigen O-Atom nach „innen“ verschieben:
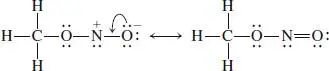
Das sieht gut aus: Alle Nichtwasserstoffatome haben Oktetts und sind ungeladen. Gibt es noch andere vernünftige Resonanzformeln? Im Lehrbuch gibt es ein allgemeines Muster für Verbindungen, in denen ein Atom mit mindestens einem freien Elektronenpaar an eins von zwei Atomen gebunden ist, die über eine Mehrfachbindung verknüpfte sind. Man verschiebt das freie Elektronenpaar nach „innen“ und eine π -Bindung nach „außen“:

Durch Anwenden dieser Vorgehensweise auf Methylnitrit erhalten wir
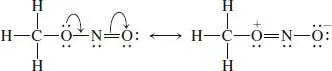
Das Ergebnis ist die zweitbeste Resonanzformel und bezüglich der Oktetts in Ordnung. Da aber die Ladungen getrennt sind, ist ihr Resonanzbeitrag kleiner als der der linken Lewis-Formel. Das Resonanzhybrid wird eher der linken Struktur mit zwei nicht äquivalenten N–O-Bindungen gleichen. Der Beitrag der rechten Struktur ist zwar klein, macht aber die endständige N–O-Bindung zur polarsten des Moleküls, wobei O das negative Ende bildet.
Für die Lewis-Strukturen und die Resonanzformeln, die wir erhalten haben, spricht auch, dass die N–O-Bindungen in CH 3ONO unterschiedlich lang sind: 142pm für die CH 3O–NO-Bindung und 117 pm für die CH 3ON=O-Bindung. In CH 3NO 2sind sie dagegen mit 122 pm gleich lang. Der Wert liegt zwischen den Werten für Einfach- und Doppelbindung, entspricht aber mehr einer Doppelals einer Einfachbindung. Der Grund hierfür ist wahrscheinlich die zusätzliche Coulomb-Anziehung zwischen dem positiven Stickstoffatom und den partiell negativen Sauerstoffatomen.
1 (a) Chlor-Atom (sieben Valenzelektronen, neutral)Chlorid-Ion (acht Elektronen, negativ geladen)
2 (b) Boran ist planar (6 e– um B), Phosphan dagegen pyramidal ( 8 e– um P wie beim N-Atom in Ammoniak):
3 (c) CF4 ist tetraedrisch, dagegen ist BrF4– mit acht Elektronenpaaren um das Br-Atom und freien Elektronenpaaren über und unter dem Br-Atom quadratischplanar. Für diese Antwort brauchen wir nur das Elektronenabstoßungsmodell VSEPR. Es ist nicht notwendig, zuerst die Hybridisierung herauszufinden.
4 (d) Wir gehen nach der gleichen Methode vor: Zeichnen Sie die Lewis-Formeln und verwenden Sie dann das Elektronenabstoßungsmodell VSEPR, um die geometrische Anordnung anzugeben. Lassen Sie die Hybridisierung zunächst außer Acht.Stickstoffdioxid enthält 17 Valenzelektronen (6 von jedem O- und 5 vom N-Atom), im Nitrit-Ion sind es 18 (das zusätzliche Elektron ergibt die Ladung–1). Das N-Atom steht in der Mitte, damit haben wir O–N–O (4 Elektronen in σ-Bindungen). In beiden Verbindungen können wir an die Sauerstoffatome 12 der übrigen Elektronen als freie Elektronenpaare anfügen. Das letzte Elektron (für NO2) bzw. die letzten beiden Elektronen (für NO2–) lassen sich am N-Atom unterbringen, sodass man für NO2 und für NO2– erhält. Beiden Lewis-Formeln fehlt das Oktett am Stickstoffatom, sie können aber durch Resonanzdelokalisierung eines Elektronenpaars vom Sauerstoffzum Stickstoffatom verbessert werden:Für NO2, Für NO2– Damit hat das Stickstoffatom nun 7 Valenzelektronen in NO2 und 8 in NO2–. Wie sieht es mit der Geometrie aus? Beginnen wir mit NO2–, weil alle seine Elektronen gepaart sind und sich das Elektronenpaarabstoßungsmodell VSEPR direkt anwenden lässt. Das mittlere N-Atom ist von zwei σ-Bindungspaaren und einem freien Elektronenpaar umgeben (π-Elektronen werden im Elektronenabstoßungsmodell nicht berücksichtig), und drei Paare führen zu einer gebogenen Geometrie (die sich durch sp2-Hybridisierung erklären lässt, wenn man will). Tatsächlich beträgt der O–N–O-Bindungswinkel in Nitrit 115°. Er ist etwas kleiner als der Sollwinkel von 120° für eine trigonal-planare Struktur, weil das freie Elektronenpaar, das sich nur an einem Atom befindet, größere Abstoßung ausübt als die bindenden Paare, sodass der Bindungswinkel etwas kleiner wird. Wir betrachten nun Stickstoffdioxid. Das N-Atom trägt jetzt ein einzelnes nichtbindendes Elektron anstelle eines freien Elektronenpaars. Da ein Elektron weniger Abstoßung ausübt als zwei, können wir vorhersagen, dass der O–N–O-Bindungswinkel in Stickstoffdioxid größer sein sollte als in Nitrit. Ihre Informationen reichen aber nicht aus, um anzugeben, wie viel größer der Winkel sein wird. Tatsächlich beträgt er 134°. Dass er größer ist als 120°, bedeutet, dass die beiden bindenden Elektronenpaare eine stärkere Abstoßung ausüben als das einzelne nichtbindende Elektron.Es wird Sie zweifellos interessieren, dass Stickstoffdioxid ein wesentlicher Bestandteil im Smog von Großstädten ist. Das giftige, übel riechende bräunliche Gas ist zum großen Teil ursächlich für den unverwechselbaren Charakter smoghaltiger Luft.
Читать дальше