4 (d) Die C–N-Bindung ist eine sp3–sp3-Überlappung, die N–H-Bindungen sind sp3–s-Überlappungen.
5 (e) Die beiden an der Dreifachbindung beteiligten Kohlenstoffatome sind sp-hybridisiert. Demnach ist die σ-Bindung zwischen ihnen eine sp–sp-Überlappung. Es gibt zwei π-Bindungen zwischen beiden Atomen, beide entstehen durch seitliche p–p-Überlappung. Die Bindung zum anderen (tetraedrischen) Kohlenstoffatom ist eine sp–sp3-Überlappung.
6 (f) Die C–N-σ-Bindung ist eine sp2–sp2-Überlappung, weil das Kohlenstoffatom ebenfalls trigonal-planar und sp2-hybridisiert ist. Die übrigen (p-)Orbitale am Stickstoff-und Kohlenstoffatom ergeben durch seitliche Überlappung eine p–p-π-Bindung. Die N–H-Bindungen sind sp2–s-Überlappungen.
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
1 (a), (b) und (c) Jedes Kohlenstoffatom ist an vier weitere Atome gebunden und hat daher annähernd tetraedrische Anordnung. Jedes Kohlenstoffatom in diesen Molekülen ist sp3-hybridisiert.
2 (d) Jedes Kohlenstoffatom ist an drei weitere Atome gebunden (zwei Wasserstoffatome und das andere Kohlenstoffatom). Die Bindungen zu den Wasserstoffatomen sind σ-Bindungen. Eine der C–C-Bindungen ist eine σ-Bindung, die andere eine π-Bindung. Demzufolge hat jedes Kohlenstoffatom annähernd trigonale Anordnung (wie das Boratomin BH3) und ist sp2-hybridisiert. Oder anders gesagt: Jedes Kohlenstoffatom nutzt sp2-Orbitale in den drei σ-Bindungen und das übrige p-Orbital in einer π-Bindung.
3 (e) Jedes Kohlenstoffatom ist an zwei weitere Atome gebunden (ein Wasserstoff- und das andere Kohlenstoffatom). Die C–H-Bindungen sind ebenso σ-Bindungen wie eine der C–C-Bindungen. Die anderen beiden C–C-Bindungen (in der Dreifachbindung) sind π-Bindungen. Die Anordnung ist linear (wie bei Beryllium in BeH2). Jedes Kohlenstoffatom ist sp-hybridisiert und nutzt zwei sp-Orbitale für σ-Bindungen und zwei p-Orbitale für π-Bindungen.
4 (f)
5 (g) Die Hybridisierung muss beiden Kohlenstoffatomen die Doppelbindung ermöglichen (rechte Resonanzstruktur). Daher sind beide sp2-hybridisiert.
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f) Strichformeln geben in der Regel nicht die wahren Bindungswinkel wieder.
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
1 (a) H2NCH2CH2NH2
2 (b) CH3CH2OCH2CN
3 (c) CHBr3
In Kurzstrukturformeln stehen die Wasserstoffatome normalerweise direkt hinterden Atomen, an die sie gebunden sind. Diese Vereinbarung wird gelegentlich beim ersten , in einer Kurzstrukturformel links stehenden Atom umgekehrt, beispielsweise in der Formel (a), die mit H 2N statt mit NH 2beginnt, oder bei einem Methylsubstituenten, der an dieser Stelle als H 3C statt als CH 3erscheinen kann. Achten Sie darauf, Wasserstoffatome niemals von den Atomen, an die sie gebunden sind, durch ein anderes Elementsymbol zu trennen.
1 (a) (CH3)2NH
2 (b)
3 (c) CH3CHOHCH2CH2SH
4 (d) CF3CH2OH
5 (e) CH3CH=C(CH3)2
6 (f)
Für einige Strukturen der Übungen 1.42 und 1.43 gibt es mehrere richtige Antworten.
Aus Übung 1.40:
1 (a) –CN
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
Aus Übung 1.43:
1 (a)
2 (b)
3 (c)
4 (d)
5 (e)
6 (f)
1 (a)
2 (b)
3 (c)
4 (d)
1 (a) C5H12. Beginnen Sie mit dem Isomer, in dem alle Kohlenstoffatome geradkettig verknüpft sind. Verkürzen Sie dann die Kette um jeweils ein Kohlenstoffatom, das Sie als Substituenten an innere Positionen der verbliebenen Kette knüpfen, bis jede Möglichkeit gezeichnet ist. Es gibt drei Isomere:(1) CH3–CH2–CH2–CH2–CH3 oder CH3CH2CH2CH2CH3 oder CH3(CH2)3CH3. Alle sind häufig verwendete Formen von Kurzstrukturformeln derselben Verbindung.Strichformel:(2) ist das gleiche Molekül gedreht.(3) ist das Gleiche wie (CH3)4C. Strichformel:
2 (b) CH3H8O. Auch hier gibt es drei Isomere:(1) CH3–CH2–CH2–OH ist das Gleiche wie CH3 CH2CH2OHStrichformel: (2) (3) CH3–CH2–O–CH3 ist das Gleiche wie CH3–O–CH2–CH3 oder CH3–O–CH2–CH3 oder CH3CH2OCH3. Strichformel:
Zur Erinnerung: Am wichtigsten ist das Vorliegen von Elektronenoktetts an möglichst vielen Atomen (natürlich mit Ausnahme von H). In den folgenden Strukturen haben alle C-, N- und O-Atome Oktetts.
1 (a) HC≡CCH3 und H2C=C=CH2
2 (b) Ladungen in CH3CN: für N(;für .
3 (c) und Keines der obigen Molekülpaare besteht aus Resonanzformeln: In jedem Fall unterscheiden sich die Strukturen durch die relativen Positionen der Atome. Resonanzformeln unterscheiden sich nur in Anordnung der Elektronen.
1 (a)(1) (2) (3) Das Symbol R steht hier für CH3
2 (b) Die Oktettregel hat Priorität vor den Ladungstrennungsregeln, daher sind bei allen drei Verbindungen die Strukturen mit Doppelbindung bevorzugt.
3 (c) In jeder Doppelbindungsstruktur trägt ein elektronegatives Atom (F, O oder N) eine positive Ladung. Aufgrund der Elektronegativitätsreihenfolge F > O > N kann F die positive Ladung am schlechtesten aufnehmen. Daher ist die Resonanzform mit Ladungstrennung bei R2BF am ungünstigsten. Diese Resonanzform ist für R2 BOR günstiger und für R2BNR2 noch besser, weil die Fähigkeit des elektronegativen Atoms zur Aufnahme der positiven Ladung in der Reihenfolge F < O < N zunimmt.
4 (d) Die Resonanzformeln mit der Doppelbindung erfordern in beiden Fällen eine sp2-Hybridisierung.
Jedes markierte Kohlenstoffatom ist mit seinen drei nicht markierten Nachbaratomen trigonal - planar verknüpft. Diese Anordnung lässt sich am besten mit einer sp 2-Hybridisierung an C* erklären, wobei die drei sp 2-Hybride die Bindungen zwischen jedem C* und seinen CH 2-Nachbarn bilden. Die σ -Bindung zwischen den beiden C *-Atomen steht senkrecht auf den beiden, durch die sp 2-Hybride gebildeten Ebenen und resultiert aus der Überlappung der übrigen reinen p -Orbitale an jedem C *:
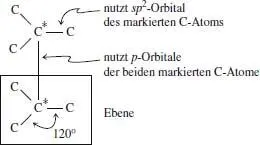
Die durch Überlappung nicht hybridisierter p -Orbitale gebildete C *–C *-Bindung ist länger und wesentlich schwächer als die normale sp 3– sp 3-Einfachbindung.
1 (a)(1) Das negativ geladene Kohlenstoffatom ist an drei weitere Atome gebunden und hat ein freies Elektronpaar ähnlich wie N in NH3: sp3.(2) Vergleichen Sie mit 1.39(d): Das Kohlenstoffatom ist sp2-hybridisiert (die Doppelbindung benötigt ein p-Orbital).(3)Vergleichen Sie mit 1.39(e): Das Kohlenstoffatom ist sp-hybridisiert (die Dreifachbindung benötigt zwei p-Orbitale).
2 (b) Wie hängen die Orbitalenergie und die Fähigkeit zur Aufnahme einer negativen Ladung zusammen? Verbindungen mit Elektronen in energiearmen Orbitalen sind stabiler als Verbindungen mit Elektronen in energiereicheren Niveaus. Aus der Reihenfolge der Orbitalenergie sp < sp2 < sp3 ergibt sich das relative Aufnahmevermögen für eine negative Ladung: HC≡C– (Ladung in einem sp-Orbital) > CH2=CH– (sp2) > CH3CH2– (sp3).
3 (c) Aus (b) ergibt sich, dass HC≡C– stabiler ist als CH2=CH– und dieses stabiler als CH3CH2–. Die Anionen entstehen in den Gleichgewichten
Читать дальше













