5 (e) Vergleichen wir nun die beiden neuen Dioxide SO2 und ClO2 mit dem schon betrachteten NO2. Zuerst die Lewis-Strukturen und Resonanzformeln:Die beiden Strukturen ganz rechts haben erweiterte Valenzschalen (größer als Oktetts), was bei Atomen der dritten Reihe in Ordnung ist.Auf der Basis des Elektronenabstoßungsmodells hätten SO2 und ClO2 wegen des freien Elektronenpaars am S-Atom bzw. des freien Elektronenpaars + des einzelnen ungepaarten Elektrons am Cl-Atom gebogene Strukturen. Der tatsächliche Bindungswinkel beträgt in SO2 129° und in ClO2 116°, der Unterschied ist auf die zusätzliche Abstoßung durch das dritte nichtbindende Elektron am Cl-Atom zurückzuführen.Ungeachtet der Tatsache, dass ClO2 übel riechend und giftig ist und zur Explosion neigt, wird es als wichtige Industriechemikalie in der Papierherstellung zum Bleichen von Zellstoff verwendet. Sicherheitshalber wird es direkt vor der Verwendung hergestellt und muss nicht gelagert werden.
1 (a) Die Molekülorbitale erhält man wie folgt:Daraus resultieren Elektronenkonfigurationen für H2 (σ)2 mit zwei bindenden Elektronen und für H2+ (σ)1 mit einem bindenden Elektron. Folglich hat H2 die stärkere Bindung.
2 (b) Wie in Übung 1.14.
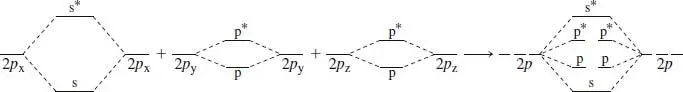
3 (c) und (d) Wir erstellen auf analoge Weise ein Orbitaldiagramm. Wie fangen wir an? Zunächst müssen wir feststellen, welche der im Kapitel besprochenen Orbitale wir berücksichtigen müssen und welche nicht. Bei Molekülen mit Mehrfachbindungen und mehreren Atomen, z. B. Ethen und Ethin (siehe Abb. 1.21, Lehrbuch), müssen wir Hybridorbitale heranziehen, weil wir sie zur Klärung der geometrischen Anordnung brauchen. Da bei zweiatomigen Molekülen wie O2 und N2 aber keine „Geometrie“ zu klären ist, erfüllt die Orbitalhybridisierung keinen Zweck und wir können von einfachen Atomorbitalen ausgehen. Das macht das Ganze leichter! Außerdem stellen wir fest, dass die 1s-und 2s-Orbitale von N und O vollständig besetzt sind. In solchen Fällen ist es üblich, die s-Orbitale zu ignorieren, weil ihre Überlappung zu keiner Nettobindung führt (genau wie zwischen zwei He-Atomen) – eine weitere willkommene Vereinfachung. Für die Bindung müssen wir nur noch die drei 2p-Orbitale jedes Atoms berücksichtigen, weil sie als einzige teilweise besetzt sind. Entsprechend Abb. 1.21 kann man sich die endständige Überlappung (σ-Bindung) der einander zugewandten px-Orbitale (eins an jedem Atom) und die seitliche Überlappung (π-Bindung) der übrigen p-Orbitale (zwei an jedem Atom, py und pz) vorstellen.Das vollständige Molekülorbital-Diagramm enthält demzufolge drei Gruppen von Orbitalwechselwirkungen, die nachstehend separat und – ganz rechts – kombiniert dargestellt sind. Zuerst ist die endständige (σ-)Überlappung der px-Orbitale gezeigt, die zu σ- und σ*-Orbitalen (bindend bzw. antibindend) führt. Danach folgen die beiden π-Überlappungen der py-und pz-Orbitalpaare, die zwei Sätze von π- bzw. π*-Orbitalen ergeben. Da die σ-Überlappung im Allgemeinen besser ist als die π-Überlappung, ist der Energieabstand zwischen σ- und σ*-Orbital in den hier gezeigten Diagrammen größer als der zwischen π-und π*-Orbital – nach Abb. 1.12 hängt der Energieunterschied zwischen Atom- und Molekülorbitalen mit der Stärke der Bindung zusammen – und entspricht der Energieänderung beim Übergang der Atome zum Molekül. (Weitergehende theoretische Analysen lassen erkennen, dass die tatsächliche Anordnung der Orbitalenergien nicht bei jedem zweiatomigen Molekül der zweiten Reihe ganz so ist wie hier gezeigt, aber das ist hier nicht von Bedeutung.)
| Für (c): |
O 2, ( σ ) 2( π ) 2( π ) 2( π* ) 1( π *) 1, insgesamt 4 bindende Elektronen; dagegen O 2 +, ( σ ) 2( π ) 2( π ) 2( π *) 1, mit insgesamt 5 bindenden Elektronen. Demnach hat O 2 +die stärkere Bindung. |
| Für (d): |
N 2, ( σ ) 2( π ) 2( π ) 2, insgesamt 6 bindende Elektronen; demgegenüber N 2 +, ( σ ) 2( π ) 2( π ) 1, mit insgesamt 5 bindenden Elektronen. Demnach ist die Bindung in N 2stärker. |
Verwenden Sie das VSEPR-Modell (Valenzschalenelektronenpaarabstoßung), um die Geometrie um das jeweilige Kohlenstoff- oder Stickstoffatom anzugeben. Zählen Sie die anderen mit diesem Atom verknüpften Atome und addieren Sie die Zahl der freien Elektronenpaare hinzu, die das betreffende Atom möglicherweise enthält. 2 = linear und sp -hybridisiert; 3 = trigonal-planar und sp 2-hybridisiert; 4 = tetraedrisch und sp 3-hybridisiert. Das ist nicht schwer.
1 (a) Die vier mit dem markierten Kohlenstoffatom verknüpften Atome sind über vier Einfachbindungen gebunden und haben annähernd tetraedrische Geometrie, was durch die sp3-Hybridisierung erklärt wird. Die Anordnung ist nicht exakt tetraedrisch, weil die vier Atome nicht gleich sind (zwei Wasserstoffatome, ein Kohlenstoff- und ein Br-Atom).
2 (b) Machen Sie sich keine Gedanken über Mehrfachbindungen! Das betreffende Kohlenstoffatom ist mit drei anderen Atomen verknüpft und daher annähernd trigonal-planar mit sp2-Hybridisierung.
3 (c) Dieses Kohlenstoffatom ist mit drei anderen Atomen verknüpft. Also wie in (b): trigonal-planar, sp2-Hybridisierung.
4 (d) Das Stickstoffatom ist mit drei anderen Atomen verknüpft und hat ein freies Elektronenpaar, demnach ist es sp3-hybridisiert. Wir bezeichnen es aber nicht als tetraedrisch. Wenn wir für die geometrische Anordnung um ein Atom einen Ausdruck wählen, betrachten wir im Allgemeinen nur die Atome, an die es gebunden ist, und nicht die freien Elektronenpaare. Damit lässt sich das Stickstoffatom in CH3NH2 am besten als pyramidal beschreiben – so wie das Stickstoffatom in Ammoniak, NH3.
5 (e) Das Kohlenstoffatom befindet sich zwischen zwei anderen Atomen. Auch hier lässt das VSEPR-Modell Mehrfachbindungen außer Acht. Die geometrische Anordnung ist linear, das Kohlenstoffatom sp-hybridisiert.
6 (f) Das Stickstoffatom ist an drei andere Atome gebunden, daher trigonal-planar und sp2-hybridisiert.
1 (a) Das Kohlenstoffatom nutzt sp3-Hybridorbitale für seine vier σ-Bindungen. Das gilt auch für das andere Kohlenstoffatom im Molekül, daher erfolgt die Bindungsbildung zwischen den beiden C-Atomen durch Überlappung der beiden sp3-Hybridorbitale. Die C–H-Bindungen entstehen durch Überlappung zwischen dem sp3-Hybridorbital am Kohlenstoffatom und einem s-Atomorbital des Wasserstoffatoms. Die C–Br-Bindung resultiert aus der Überlappung des sp3-Hybridorbitals am Kohlenstoffatom mit einem p-Atomorbital des Bromatoms.
2 (b) Zwei der drei sp2-Orbitale am markierten Kohlenstoffatom führen zu normalen tetraedrischen Kohlenstoffatomen. Diese σ-Bindungen beinhalten demnach eine sp2–sp3-Überlappung. Das Sauerstoffatom ist an ein anderes Atom gebunden (das markierte Kohlenstoffatom) und hat zwei freie Elektronenpaare. 1+2 = 3. Es könnte als sp2-hybridisiert betrachtet werden, sodass die C–O-σ-Bindung eine sp2–sp2-Überlappung wäre. Wie in Übung 1.17 besprochen wurde, erfolgt die Orbitalhybridisierung am Sauerstoffatom aus energetischen Gründen aber nur zögernd, daher ist es genauer, für diese C–O-σ-Bindung eine C(sp2)–O(p)- Überlappung anzunehmen. Eins der übrigen p-Orbitale am Sauerstoffatom und das p-Orbital am Kohlenstoffatom sind seitlich parallel ausgerichtet und ergeben so die zweite (π-)Bindung zwischen den beiden Atomen.
3 (c) Jedes der drei in σ-Bindungen zum markierten Kohlenstoffatom verwendeten sp2-Orbitale führt zu einem anderen Atom. Eins geht zu dem anderen, ebenfalls trigonal-planaren Kohlenstoffatom, also eine sp2–sp2-Überlappung. Beide Kohlenstoffatome haben ein p-Orbital übrig, deren seitliche Überlappung eine p–p-π-Bindung ergibt. Das Sauerstoffatom ist an zwei Atome gebunden und hat zwei freie Elektronenpaare; wir könnten es als sp3-hybridisiert betrachten. Wie wir aber gerade festgestellt haben, ist das für ein Sauerstoffatom nicht wahrscheinlich. Die C–O-σ-Bindung ist eine C(sp2)–O(p)-Bindung. Die C–H-Bindung entsteht durch C(sp2)–H(s)-Überlappung.
Читать дальше













