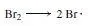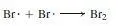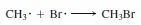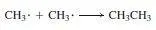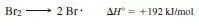3 (c) Von links nach rechts: 1,2-Dimethylpropyl-Radikal, sekundär, mittlere Stabilität; 1,1-Dimethylpropyl-Radikal, tertiär, am stabilsten; 3-Methylbutyl-Radikal, primär, am wenigsten stabil.
Die Hyperkonjugation im 1,1-Dimethylpropyl-Radikal ist die gleiche wie im 1-Ethyl-1-methylpropyl-Radikal [(b) oben]; in Ihrer Darstellung sollte eine der endständigen CH 3-Gruppen durch H ersetzt sein.
Bearbeiten Sie Aufgaben wie diese „mechanistisch“: Formulieren Sie allgemeine Reaktionsschritte ähnlich den im Lehrbuch gezeigten, bis Sie zu stabilen Molekülen gelangen. Die Pyrolyse von Propan beginnt folgendermaßen:
1 (1) Anschließend gibt es drei verschiedene mögliche Rekombinationen:
2 (2)
3 (3)
4 (4) (Umkehr des ersten Schritts)Für die Abspaltung des Wasserstoffatoms gibt es zwei Möglichkeiten:
5 (5)
6 (6)
Die Abspaltung kann nur von dem Kohlenstoffatom erfolgen, das dem radikalisehen Kohlenstoffatom benachbartist. Das Methyl-Radikal, ·CH 3, hat kein anderes benachbartes Kohlenstoffatom und kann daher kein Wasserstoffatom abspalten. Es kann aber noch ein Wasserstoffatom aufnehmen[Reaktion (5), oben].
Demnach entstehen beim Cracken von Propan vier neue Produkte: Methan, Ethan, Butan und Ethen (Ethylen).
1 (a) Die schwächste Bindung in Butan ist die C2–C3-Bindung, DH° = 368 kJ/mol (Tab. 3.2). Die Pyrolyse sollte daher folgendermaßen ablaufen:(1) (2) Umkehr von (1)(3) Abspaltung eines H-Atoms
2 (b) Die schwachsten Bindungen sind die drei aquivalenten C–C-Bindungen, DH° = 368 kJ/mol. Daher(1) Bindungsbruch(2) (3) (4) Umkehr von(1); Rekombination(5) Abspaltung eines H-Atoms(6)
Die DH °-Werte sind einfach den Tab. 3.1 und 3.4 zu entnehmen. Werte in kJ/mol.
1 (a) 435 + 159 – 2(565) = –536
2 (b) 435 + 242 – 2(431) = –185
3 (c) 435 + 192 – 2(364) = –101
4 (d) 435 + 151 – 2(297) = –8
5 (e) 389 + 159 –(460 + 565) = –477
6 (f) 389 + 242 –(339 + 431) = –139
7 (g) 389 + 192 –(280 + 364) = –63
8 (h) 389 + 151 –(218 + 297) = +25
1 (a) Zwei: 1-Halogenbutan und 2-Halogenbutan
2 (b) Drei (siehe Lösung zu Übung 3.21)
3 (c) Vier (siehe Lösung zu Übung 3.21)
4 (d) Vier:
1 (a)(i) CH3CH2CH2CH2Cl (1-Chlorpentan),CH3CH2CH2CHClCH3 (2-Chlorpentan) undCH3CH2CHClCH2CH3 (3-Chlorpentan)(ii) CH3CH2CH(CH3)CH2CH2Cl (1-Chlor-3-methylpentan),CH3CH2CH(CH3)CHClCH3 (2-Chlor-3-methylpentan),CH3CH2CCl(CH3)CH2CH3 (3-Chlor-3-methylpentan) undCH3CH2CH(CH2Cl)CH2CH3 3-(Chlormethyl)pentan
2 (b) Zur Beantwortung dieser Frage müssen Sie zunächst alle Wasserstoffatome im Ausgangsalkan zählen, deren Abspaltung zu jeweils einem der Produkte führen könnte, und sie als primär, sekundär oder tertiär bestimmen. Multiplizieren Sie dann die Zahl der Wasserstoffatome mit der relativen Reaktivität für diese Art von Wasserstoffatom bei den in der Aufgabe genannten Bedingungen: eine Chlorierungsreaktion bei 25°C. Auf diese Weise erhalten Sie den relativen Produktanteil entsprechend der Abspaltung dieser Wasserstoffatome. Nachdem Sie das für alle Produkte gemacht haben, überführen Sie diese relativen Anteile in Prozentausbeuten, indem Sie auf 100 beziehen (siehe unten).(i) 1-Chlorpentan entsteht durch Chlorierung eines der sechs primären Wasserstoffatome (jedes mit der relativen Reaktivität 1) an C1 und C5; daraus folgt eine relative Ausbeute von 6 × 1 = 6. 2-Chlorpentan wird durch Chlorierung eines der vier sekundären Wasserstoffatome (jedes mit der relativen Reaktivität 4) an C2 und C4 gebildet; daraus folgt eine relative Ausbeute von 4×4 = 16. 3-Chlorpentan entsteht durch Chlorierung eines von zwei sekundären Wasserstoffatomen (jedes mit der relativen Reaktivität 4) an C3; daraus ergibt sich eine relative Ausbeute von 2 × 4 = 8. Daraus errechnet sich die absolute prozentuale Ausbeute für jedes Produkt:Damit beträgt die Ausbeute an(ii) 1-Chlor-3-methylpentan wird durch Chlorierung eines der sechs primären Wasserstoffatome (relative Reaktivität 1) an C1 und C5 gebildet; daraus folgt eine relative Ausbeute von 6 × 1 = 6. 2-Chlor-3-methylpentan entsteht durch Chlorierung eines der vier sekundären Wasserstoffatome (relative Reaktivität 4) an C2 und C4; daraus folgt eine relative Ausbeute von 4×4 = 16. 3-Chlor-3-methylpentan wird durch Chlorierung des einzigen tertiären Wasserstoffatoms (relative Reaktivität 5) am Kohlenstoffatom 3 gebildet; damit beträgt die relative Ausbeute 1×5 = 5. 3-(Chlormethyl)pentan entsteht durch Chlorierung eines von drei primären Wasserstoffatomen (relative Reaktivität 1) der an C3 stehenden Methylgruppe; die relative Ausbeute ist daher 1 × 3 = 3.Damit beträgt die Ausbeute an
3 (c) Fortpflanzungsschritt 1 [die angegebenen Werte sind DH°-Werte (kJ/mol) für geknüpfte oder gelöste Bindungen]:Fortpflanzungsschritt 2:Für die Gesamtreaktion betragt ΔH° = –140 kJ/mol.
Der Mechanismus gleicht qualitativ dem der Chlorierung von Methan (Lehrbuch Abschn. 3.4).
Kettenstart:
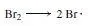
Fortpflanzungsschritte:
1 (1)
2 (2)
Kettenabbruch:
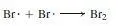
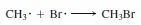
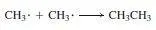
Die zur Erstellung der Diagramme benötigten Daten sind in Tab. 3.5 zu finden.
Beispiele aus den Abb. 3.7 und 3.8 können als Modelle dienen.
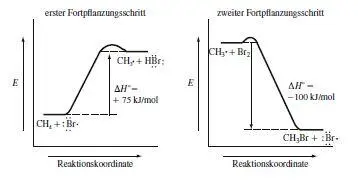
Kettenstart:
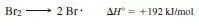
Kettenfortpflanzung:
1 (1)
2 (2) Der Gesamtwert für ΔH° unterscheidet sich nur wenig von den Werten für typische C–H-Bindungen der Alkane: Methan, ΔH° = –25 kJ/mol; primäre C–H, ΔH° = –42 kJ/mol; sekundäre C–H, ΔH° = –56 kJ/mol; tertiäre C–H, ΔH° = –65 kJ/mol. Allerdings ist der geschwindigkeitsbestimmende erste Fortpflanzungsschritt in der Reaktion von Benzol sehr viel endothermer als bei einer Alkanreaktion, weil die C–H-Bindungen in Benzol außergewöhnlich stark sind. Dadurch ist die Bromierung von Benzol nach diesem Mechanismus äußerst schwierig (sehr langsam) und kann kinetisch nicht mit den Bromierungsreaktionen typischer Alkane konkurrieren.
Qualitativ die gleiche Aufgabenstellung wie bei 3.23, aber mit anderen Werten für die Bindungsstärken.
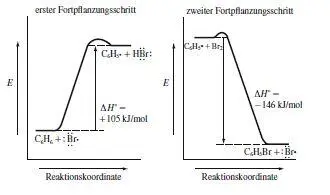
Das linke Diagramm zeigt, dass der erste Fortpflanzungsschritt einen späten Übergangszustand hat; er liegt auf der Reaktionskoordinate in der Nähe der Produkte. Der zweite Fortpflanzungsschritt (rechts) hat dagegen einen frühen Übergangszustand in der Nähe der Ausgangsverbindungen.
Читать дальше