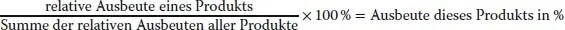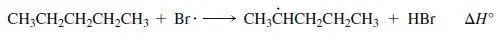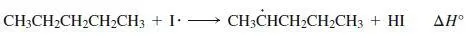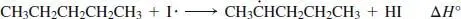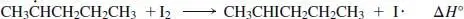1 (a)
2 (b) Die Ausgangsverbindung ist Propan. Um 1-Brompropan zu bilden, müsste ein Bromatom eins der sechs primären Wasserstoffatome an C1 oder C3 ersetzen. Zur Bildung von 2-Brompropan müsste eins der beiden sekundären Wasserstoffatome an C2 entfernt werden. Nach Tab. 3.6 reagieren Bromatome mit sekundären Wasserstoffatomen 80-mal schneller als mit primären Wasserstoffatomen. Wenn wir die relative Geschwindigkeit der Bromierung an einem primären Wasserstoffatom willkürlich = 1 setzen, beträgt die Gesamtgeschwindigkeit der Bromierung an allen sechs primären Wasserstoffatomen = 6 × 1 = 6. Sekundäre Wasserstoffatome reagieren 80-mal schneller; davon gibt es zwei, sodass die Gesamtgeschwindigkeit für die Bromierung an der sekundären Position = 80 × 2 = 160 ist. Zur Bestimmung des ungefähren Produktverhältnisses dividieren wir nur die Geschwindigkeiten: (Geschwindigkeit der Bildung von 2-Brompropan)/(Geschwindigkeit der Bildung von 1-Brompropan) = 160/6 = 26.7. Also entstehen für jedes gebildete Molekül 1-Brompropan 26.7 Moleküle des 2-Isomers. Damit ist 2-Brompropan das Hauptprodukt, das nach dieser Methode mit guter Selektivität und hoher Ausbeute entstehen sollte.Wie können wir diese Information in ungefähre Prozentausbeuten umwandeln? So: %-Ausbeute an 2-Brompropan = (Bildungsgeschwindigkeit von 2-Brompropan/Gesamtgeschwindigkeit der Bromierung) × 100% = 26.7/(26.7 + 1) = 96%. Ziemlich gut!
Gehen Sie davon aus, dass an jedes Alkanmolekül nur ein Halogenatom gebunden wird, wenn nichts anderes erwähnt ist.
1 (a) Keine Reaktion. Die Iodierung von Alkanen verläuft endotherm.
2 (b) CH3CHFCH3 + CH3CH2CH2F F2 reagiert nicht sehr selektiv.
3 (c) Die Bromierung erfolgt nach Möglichkeit an der tertiären Position. Siehe Anmerkung in der Antwort zu Übung 3.15(d).
4 (d) Es entsteht ein komplexes Gemisch. Cl2 reagiert zwar selektiver als F2, aber die tertiäre Position ist nur um den Faktor 5 gegenüber der primären bevorzugt.
5 (e) Br2 ist hoch selektiv für tertiäre C—H-Bindungen.
Relative Ausbeute = (Zahl der Wasserstoffatome der jeweiligen Art im Ausgangsalkan) × (relative Reaktivität)
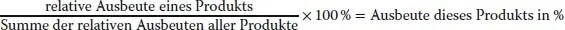
| Produkt |
Art des Wasserstoffatoms |
Zahl der Wasserstoffatome |
Relative Reaktivität |
Relative Ausbeute |
Ausbeute in % |
| (b) CH 3CHFCH 3 |
sekundär |
2 |
1.2 |
2.4 |
29 |
| CH 3CH 2CH 2F |
primär |
6 |
1 |
6 |
71 |
| (d) (CH 3) 2CClCH 2C(CH 3) 3 |
tertiär |
1 |
5 |
5 |
18 |
| ClCH 2CH(CH 3)CH 2C(CH 3) 3 |
primär |
6 |
1 |
6 |
21 |
| (CH 3) 2CHCHClC(CH 3) 3 |
sekundär |
2 |
4 |
8 |
29 |
| (CH 3) 2CHCH 2C(CH 3) 2CH 2Cl |
primär |
9 |
1 |
9 |
32 |
(c) und (e) Die Selektivität für die Substitution durch Br 2an der tertiären Position beträgt etwa 73 % bei (c) und 91 % bei (e).
Nur die Bromierungsreaktionen (c) und (e) sind für Synthesezwecke wirklich akzeptabel. Die übrigen Reaktionen liefern mehrere Produkte in ähnlichen Ausbeuten und eignen sich nicht für die Synthese. Die Fluorierung (b) sieht zwar auf dem Papier gut aus, aber in der Praxis ist die Verwendung des hoch reaktiven F 2als Reagens sehr schwierig.
1 (a) Pentan hat zwei Arten von Wasserstoffatomen, primäre und sekundäre, die sich aber auf drei verschiedene Gruppen verteilen, weil je nach Ort der radikalischen Bromierung drei verschiedene Monobrompentane möglich sind. Der Austausch eines beliebigen der sechs primären Wasserstoffatome an C1 und C5(Gruppe a in der Struktur unten) führt zu 1-Brompentan. Da die Reaktivität primärer Wasserstoffatome 80-mal geringer ist als die sekundärer Wasserstoffatome, sollte die Ausbeute an diesem Produkt am geringsten sein. Die sechs sekundären Wasserstoffatome an C2, C3 und C4 sind alle etwa gleich reaktiv. Der Austausch eines der beiden Wasserstoffatome an C3 (Gruppe b) liefert 3-Brompentan, während durch Substitution eines der vier Wasserstoffatome an C2 und C4 (Gruppe c) 2-Brompentan entsteht. Es ist das Hauptprodukt, weil für seine Bildung die meisten der reaktivsten Wasserstoffatome in der Ausgangsverbindung ersetzt werden können.
2 (b) und (c) Zeichnen Sie das Molekül zuerst in herkömmlicher Form und bestimmen sie die Rotationsbindung:Wählen Sie dann eine Blickrichtung zum Anfertigen der Newman-Projektionen, beispielsweise C2 vorne und C3 hinten. Beginnen Sie mit einer beliebigen gestaffelten Konformation und führen Sie danach 120°-Drehungen des einen Kohlenstoffatoms (sagen wir des hinteren, C3) bezüglich des anderen durch, sodass Sie für diese Verbindung alle gestaffelten Konformationen erhalten, die durch Drehung um die C2–C3-Bindung möglich sind. Die graphische Darstellung der potenziellen Energie kann direkt unter die Projektionen gezeichnet werden.
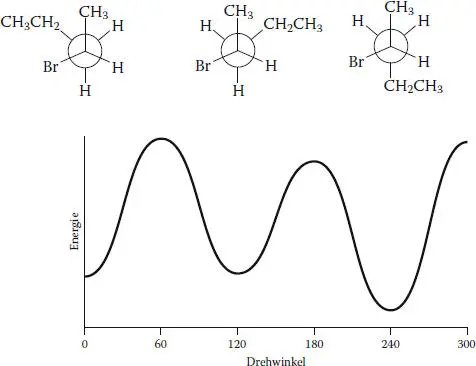
Formulieren Sie zuerst die Fortpflanzungsschritte und bestimmen Sie die zugehörigen Werte für ΔH° . Wie in Übung 3.31 angegeben entsteht das Hauptprodukt durch Halogenierung an C2. Zeichnen Sie die Diagramme mithilfe der Abb. 3.7 im Lehrbuch als Vorlage. Die Übergangszustände sind bei den Maxima für jeden Schritt im Diagramm lokalisiert.
Bromierungsschritte:
Fortpflanzungsschritt 1
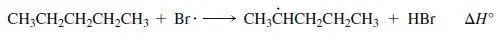
DH° = 412kJ/mol für sekundäre C–H-Bindung DH °(HBr) = 364 kJ/mol + 48kJ/mol
Fortpflanzungsschritt 2
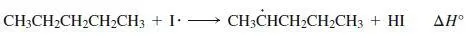
DH °(Br 2) = 192 kJ/mol DH ° = 297 kJ/mol für sekundäre C–Br-Bindung –105 kJ/mol Δ H °(gesamt) = –57 kJ/mol
Iodierungsschritte:
Fortpflanzungsschritt 1
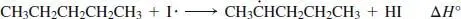
DH ° = 412 kJ∕mol für sekundäre C−H-Bindung DH ◦(HI) = 297 kJ∕mol +115 kJ∕mol
Fortpflanzungsschritt 2
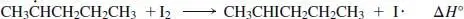
DH °(I 2) = 151 kJ∕mol DH ° = 234 kJ∕mol für sekundäre C−I-Bindung –83 kJ/mol Δ H ◦(gesamt) = +32 kJ∕mol
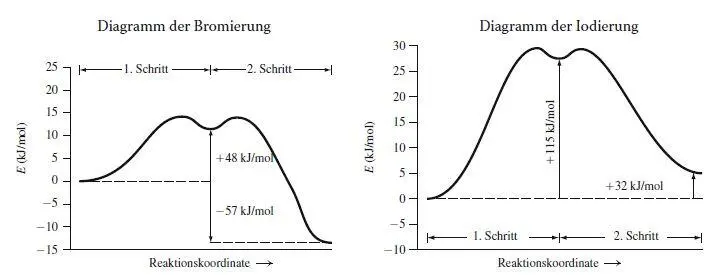
Der Hauptunterschied zwischen den beiden Halogenierungen ist der für die Iodierung deutlich endothermere erste Fortpflanzungsschritt, durch den auch die Gesamtreaktion endotherm wird.
Читать дальше