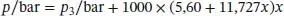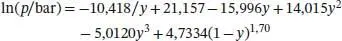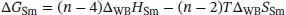S4.2.16In Abb. 4.13ist die Abhängigkeit des chemischen Potenzials fester, flüssiger und gasförmiger Phasen von der Temperatur schematisch dargestellt. Alle Kurven besitzen negative Steigungen; allerdings ist es unwahrscheinlich, dass man wirklich – wie abgebildet – Geraden erhält. Geben Sie einen Ausdruck für die Krümmungen (die zweiten Ableitungen nach der Temperatur) der Kurven an. Gibt es bestimmte Einschränkungen für die Krümmungen? Vergleichen Sie die Krümmungen der Linien für die flüssige und die gasförmige Phase von Wasser in der Nähe des Normalsiedepunkts; für welche Phase ist die Kurve am stärksten gekrümmt? (Die molare Wärmekapazitäten bei konstantem Druck für die flüssige Phase ist 75,3 J K −1mol −1, und 33,6 J K −1mol −1für die gasförmige Phase.)
Abschnittsübergreifende Aufgaben
A4.1Konstruieren Sie das Phasendiagramm von Benzol im Bereich um seinen Tripelpunkt (bei 36 Torr und 5,50 °C) unter Verwendung der folgenden Angaben: Δ Sm H = 10,6 kJ mol −1, Δ V H = 30,8 kJ mol −1, ρ (s) = 0,891 g cm −3, ρ (l) = 0,879 g cm −3.
A4.2‡In einer Arbeit über thermochemische Eigenschaften von Toluol (Methylbenzol) gibt R.D. Goodwin Ausdrücke für zwei Phasengrenzen an ( J. Phys. Chem. Ref. Data 18, 1565 (1989)). Die Grenze zwischen fester und flüssiger Phase ist durch
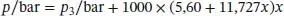
mit x = T / T 3− 1 gegeben; am Tripelpunkt ist p 3= 0,4362 µbar und T 3= 178,15 K. Die Grenze zwischen flüssiger Phase und Dampf wird durch
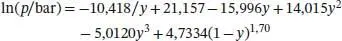
mit y = T / T krit= T /(593,95 K) beschrieben.
1 (a) Stellen Sie die Phasengrenzen fest/flüssig und flüssig/gasförmig grafisch dar.
2 (b) Wo liegt der Standardschmelzpunkt von Toluol?
3 (c) Wo liegt der Standardsiedepunkt von Toluol? (Zur Lösung der Gleichung, die Sie zur Beantwortung dieser Frage benötigen, müssen Sie auf mathematische Software zurückgreifen.) (d) Berechnen Sie die Standardverdampfungsenthalpie von Toluol. Gegeben sind die molaren Volumina der Flüssigkeit und des Dampfs am Standardsiedepunkt, 0,12 dm3 mol−1 bzw. 30,3 dm3 mol−1.
A4.3Proteine sind Polypeptide – Polymere aus Aminosäuren, die in verschiedenen durch zwischenmolekulare Wechselwirkungen stabilisierten, geordneten Strukturen existieren können. Wenn sich bestimmte Bedingungen ändern, kann das kompakt strukturierte Polypeptid jedoch zu einem ungeordneten, statistischen Knäuel (engl. random coil ) zusammenfallen. Diese Strukturänderung kann man als einen Phasenübergang bei einer charakteristischen Übergangstemperatur, der Schmelztemperatur T Sm, auffassen. Die Schmelztemperatur steigt mit zunehmender Zahl und Stärke der zwischenmolekularen Wechselwirkungen in der Kette. Die Schmelztemperatur T Sm, bei der eine durch Wasserstoffbrückenbindungen zusammengehaltene Polypeptid‐Helix zu einem statistischen Knäuel zusammenbricht, kann durch thermodynamische Berechnungen vorhergesagt werden. Zur Bildung einer α‐Helix, der am häufigsten natürlich vorkommenden Helixstruktur von Proteinen (siehe Abschn. 14.4), müssen in einem Polypeptid aus n Aminosäuren n − 4 Wasserstoffbrücken ausgebildet werden. Das erste und das letzte Kettenglied können sich frei bewegen; n − 2 Glieder bilden demnach die kompakte Helix und sind nur eingeschränkt beweglich. Die molare Freie Enthalpie des Zusammenbruchs einer Polypeptidhelix mit n ≥ 5 lässt sich dann wie folgt formulieren:
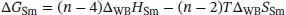
mit Δ WB H Smund Δ WB S Smals molare Enthalpie bzw. Entropie der Dissoziation der Wasserstoffbrückenbindungen im Polypeptid.
1 (a) Begründen Sie die Form der Gleichung für die Freie Enthalpie der Strukturänderung: Warum lautet der Enthalpieterm (n − 4)ΔWBHSm und der Entropieterm (n − 2)ΔWBSSm?
2 (b) Zeigen Sie, dass für TSm gilt:Stellen Sie TSm/(ΔWBHSm/ΔWBSSm) für 5 ≤ n ≤ 20 grafisch dar. Bei welchem Wert von n ändert sich TSm um weniger als 1 %, wenn n um 1 erhöht wird?
A4.4 ‡Die seit langem bekannte Verbindung Methan ist nach wie vor Gegenstand von Forschungsarbeiten, da sie als Bestandteil von Erdgas, einem wichtigen fossilen Brennstoff, praktische Bedeutung besitzt. Friend und Mitarbeiter veröffentlichten eine Übersicht über thermophysikalische Eigenschaften von Methan (D.G. Friend, J.F. Ely und H. Ingham, J. Phys. Chem. Ref. Data 18, 583 (1989)), die unter anderem folgende Angaben zum Dampfdruck an der Phasengrenze zwischen Flüssigkeit und Dampf enthält:
| T /K |
100 |
108 |
110 |
112 |
114 |
120 |
| p /MPa |
0,034 |
0,074 |
0,088 |
0,104 |
0,122 |
0,192 |
| T /K |
130 |
140 |
150 |
160 |
170 |
190 |
| p /MPa |
0,368 |
0,642 |
1,041 |
1,593 |
2,329 |
4,521 |
1 (a) Stellen Sie die Phasengrenzlinie flüssig/gasförmig grafisch dar.
2 (b) Berechnen Sie den Standardsiedepunkt von Methan.
3 (c) Berechnen Sie die Standardverdampfungsenthalpie von Methan. Gegeben sind die molaren Volumina von Flüssigkeit und Dampf am Standardsiedepunkt mit 3,8 × 10−2 dm3 mol−1 bzw. 8,89 dm3 mol−1.
A4.5‡Diamant, eine Modifikation von Kohlenstoff, ist das härteste bekannte Material und der beste bekannte Wärmeleiter. Aus diesen Gründen wird Diamant in der Industrie verbreitet als Schleif‐ und Poliermittel eingesetzt. Leider lässt sich Diamant nur schwer aus den leichter verfügbaren Modifikationen des Kohlenstoffs, wie z. B. Graphit, herstellen. Um sich dies vor Augen zu führen, sollen Sie den Druck berechnen, der erforderlich ist, um Graphit bei 25 °C in Diamant umzuwandeln (d. h. den Druck, an dem die Umwandlung von Graphit in Diamant freiwillig abläuft). Ziel ist es, einen Ausdruck für Δ R G für den Prozess Graphit → Diamant als Funktion des äußeren Drucks zu finden; mithilfe dieser Beziehung lässt sich anschließend der Druck berechnen, an dem die Änderung der Freien Enthalpie negativ wird.
1 (a) Leiten Sie die folgende Beziehung für die Druckabhängigkeit von ΔRG her:mit den Molvolumina von Graphit Vm,Graphit bzw. Diamant Vm,Diamant.
2 (b) Die Hauptschwierigkeit bei Anwendung der Beziehung aus Teilaufgabe (a) besteht darin, dass die beiden Molvolumina Vm druckabhängig sind; durch die nachfolgende Beziehung wird dieser Umstand berücksichtigt. Dabei wird ΔRG als Funktion des Drucks angegeben, und eine Taylor‐Reihe für p = p⊖ aufgestellt:Die beiden partiellen Ableitungen werden am Punkt p = p⊖ gebildet, und die Taylor‐Reihe bricht nach dem Term zweiter Ordnung ab. Term A kann aus der Beziehung aus Teilaufgabe (a) ermittelt werden, indem die molaren Volumina bei p⊖ eingesetzt werden. Die Lösung von Term B kann mithilfe der isothermen Kompressibilität von Feststoffen gefunden werden; es gilt κT = −(1/V)(∂V/∂p)T. Verwenden Sie diese Definitionsgleichung um zu zeigen, dass bei konstanter Temperatur gilt:mit den isothermen Kompressibilitäten von Diamant bzw. Graphit.
Читать дальше