Die mit dem Symbol ‡ gekennzeichneten Aufgaben wurden von Charles Trapp, Carmen Giunta und Marshall Cady beigesteuert.
Abschnitt 4.1 – Phasendiagramme reiner Stoffe
Diskussionsfragen
D4.1.1Beschreiben Sie, wie das Konzept des chemischen Potenzials die Diskussion von Phasengleichgewichten vereinheitlicht.
D4.1.2Warum hängt das chemische Potenzial auch für inkompressible Systeme (d. h. Systeme, deren Volumen sich unter Druck nicht verändert) vom Druck ab?
D4.1.3Erklären Sie, warum vier Phasen in einem Einkomponentensystem niemals im Gleichgewicht vorliegen können.
D4.1.4Was würde man beobachten, wenn eine Probe Wasser einen geschlossenen Kreisprozess in der Nähe des kritischen Punkts durchliefe?
Leichte Aufgaben
L4.1.1aWie viele Phasen liegen in Abb. 4.21aan den mit a − d gekennzeichneten Punkten jeweils vor?
L4.1.1bWie viele Phasen liegen in Abb. 4.21ban den mit a − d gekennzeichneten Punkten jeweils vor?
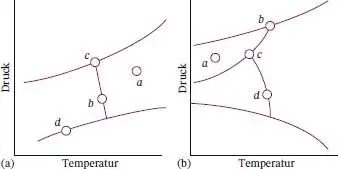
Abb. 4.21 Phasendiagramme zu den Aufgaben (a) L4.1.1a und (b) L4.1.1b.
L4.1.2aDer Unterschied der chemischen Potenziale zweier Bereiche eines Systems betrage + 7,1 kJ mol −1. Um welchen Betrag ändert sich die Freie Enthalpie des Systems, wenn 0,10 mmol einer Substanz vom einen in den anderen Bereich gebracht werden?
L4.1.2bDer Unterschied der chemischen Potenziale zweier Bereiche eines Systems betrage −8,3 kJ mol −1. Um welchen Betrag ändert sich die Freie Enthalpie des Systems, wenn 0,15 mmol einer Substanz vom einen in den anderen Bereich gebracht werden?
L4.1.3aWie viele Phasen können in einem Zweikomponentensystem maximal im miteinander Gleichgewicht stehen?
L4.1.3bWie viele Phasen können in einem Vierkomponentensystem maximal im miteinander Gleichgewicht stehen?
L4.1.4aWird im Phasendiagramm eines Einkomponentensystem die Bedingung P = 1 durch eine Fläche, eine Linie oder einen Punkt repräsentiert? Wie interpretieren Sie diesen Wert von P ?
L4.1.4bWird im Phasendiagramm eines Einkomponentensystem die Bedingung P = 2 durch eine Fläche, eine Linie oder einen Punkt repräsentiert? Wie interpretieren Sie diesen Wert von P ?
L4.1.5aBetrachten Sie Abb. 4.8. Welche Phase oder Phasen würden Sie in einer Probe CO 2erwarten, wenn folgende Bedingungen vorliegen: (i) 200 K und 2,5 atm; (ii) 300 K und 4 atm; (iii) 310 K und 50 atm?
L4.1.5bBetrachten Sie Abb. 4.9. Welche Phase oder Phasen würden Sie in einer Probe H 2O erwarten, wenn folgende Bedingungen vorliegen: (i) 100 K und 1 atm; (ii) 300 K und 10 atm; (iii) 273,16 K und 611 atm?
Schwerere Aufgaben
S4.1.1Betrachten Sie Abb. 4.8. Beschreiben Sie die Phase oder Phasen, die in einer Probe CO 2vorliegen, die ausgehend von 100 K bei einem konstanten Druck von
1 (a) 1 atm bzw.
2 (b) 70 atm erhitzt wird.
S4.1.2Betrachten Sie Abb. 4.8. Beschreiben Sie die Phase oder Phasen, die in einer Probe CO 2vorliegen, deren Druck ausgehend von 0,1 atm bei einer konstanten Temperatur von
1 (a) 200 K,
2 (b) 310 K bzw.
3 (c) 216,8 K erhöht wird.
S4.1.3Skizzieren Sie das Phasendiagramm eines Einkomponentensystems, das folgende Eigenschaften aufweist: bei niedrigen Temperaturen T und geringem Druck p liegt ausschließlich Phase γ vor; bei niedrigen T und hohem p liegt ausschließlich Phase β vor; bei hohen T und geringem p liegt ausschließlich Phase α vor; bei hohen T und hohem p liegt ausschließlich Phase δ vor; die Phasen γ und δ können niemals im Gleichgewicht sein. Diskutieren Sie etwaige Besonderheiten des von Ihnen erstellten Diagramms.
S4.1.4Skizzieren Sie das Phasendiagramm eines Einkomponentensystems, das folgende Eigenschaften aufweist: bei niedrigen Temperaturen T und geringem Druck p liegen die Phasen α und β im Gleichgewicht vor; bei steigenden Temperaturen und Drücken wird ein Punkt erreicht, an dem die Phasen α, β und γ im Gleichgewicht vorliegen; bei hohen T und hohem p liegt ausschließlich Phase γ vor; bei niedrigen T und hohem p liegt ausschließlich Phase α vor. Diskutieren Sie etwaige Besonderheiten des von Ihnen erstellten Diagramms.
Abschnitt 4.2 – Thermodynamische Betrachtung von Phasenübergängen
Diskussionsfragen
D4.2.1Was ist der physikalische Grund dafür, dass sich das chemische Potenzial einer reinen Substanz bei einer Temperaturerhöhung reduziert?
D4.2.2Was ist der physikalische Grund dafür, dass sich das chemische Potenzial einer reinen Substanz bei einer Druckerhöhung vergrößert?
D4.2.3Wie kann man mithilfe der dynamischen Differenzialkalorimetrie Phasenübergänge identifizieren?
Leichte Aufgaben
L4.2.1aDie molare Standardentropie von flüssigem Wasser bei 273,15 K ist 65 J K −1mol −1, und von Eis bei derselben Temperatur 43 J K −1mol −1. Berechnen Sie die Änderung der chemischen Potenziale von flüssigem Wasser und von Eis, wenn die Temperatur um 1 K ausgehend vom Normalschmelzpunkt erhöht wird. Welche Phase ist bei der neuen Temperatur die thermodynamisch stabilere? Begründen Sie ihre Antwort.
L4.2.1bWiederholen Sie die Berechnung aus Aufgabe L4.2.1a, jedoch diesmal für eine Absenkung der Temperatur um 1,5 K. Welche Phase ist bei der neuen Temperatur die thermodynamisch stabilere? Begründen Sie ihre Antwort.
L4.2.2aWasser wird von 25 °C auf 35 °C erhitzt. Um welchen Betrag ändert sich dabei sein chemisches Potenzial? Die molare Standardentropie von flüssigem Wasser bei 298 K ist 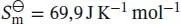 .
.
L4.2.2bEisen wird von 100 °C auf 150 °C erhitzt. Um welchen Betrag ändert sich dabei sein chemisches Potenzial? Verwenden Sie 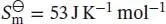 (den Mittelwert) über den gesamten Temperaturbereich.
(den Mittelwert) über den gesamten Temperaturbereich.
L4.2.3aUm welchen Betrag ändert sich das chemische Potenzial von Kupfer, wenn der Druck auf eine Probe von 100 kPa auf 10 MPa erhöht wird? Die Dichte von Kupfer beträgt 8960 kg m −3.
L4.2.3bUm welchen Betrag ändert sich das chemische Potenzial von Benzol, wenn der Druck auf eine Probe von 100 kPa auf 10 MPa erhöht wird? Die Dichte von Benzol beträgt 0,8765 g cm −3.
L4.2.4aAuf Wasser bei 20 °C wird mithilfe eines Kolbens Druck ausgeübt. Bei 1,0 bar beträgt der Dampfdruck von Wasser 2,34 kPa. Wie groß ist der Dampfdruck der Probe bei einem Druck von 20 MPa? Das Molvolumen von Wasser bei 20 °C ist 18,1 cm 3mol −1.
L4.2.4bAuf geschmolzenes Naphthalin bei 95 °C wird mithilfe eines Kolbens Druck ausgeübt. Bei 1,0 bar beträgt der Dampfdruck von Naphthalin 2,0 kPa. Wie groß ist der Dampfdruck der Probe bei einem Druck von 15 MPa? Die Dichte von Naphthalin bei 95 °C ist 1,16 g cm −3.
Читать дальше


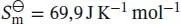 .
.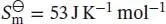 (den Mittelwert) über den gesamten Temperaturbereich.
(den Mittelwert) über den gesamten Temperaturbereich.










