52)Ein Hybridorbital (HO)ist der Aufenthaltsbereich eines Elektrons oder Elektronenpaares, der sich aus unterschiedlichen Atomorbitalen gebildet hat (Hybridisierung, Bildung von Mischorbitalen: sp,sp 2,sp 3,...). Beispiel: Drei 2p-POrbitale und ein 2s-Orbital bilden vier gleichwertige sp 3 -Mischorbitale (links), während zwei 2p-Orbitale und ein 2s-Orbital ein sp 2 -Hybridorbital ergeben (rechts):  sp 3
sp 3 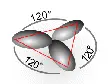 sp 2Bildquelle: User:sven, wikimedia commons, über: https://de.wikipedia.org/wiki/Hybridorbital#/media/File:Sp3-Orbital.svg (Lizenz: the Creative Commons Attribution-Share Alike 3.0 Unported)
sp 2Bildquelle: User:sven, wikimedia commons, über: https://de.wikipedia.org/wiki/Hybridorbital#/media/File:Sp3-Orbital.svg (Lizenz: the Creative Commons Attribution-Share Alike 3.0 Unported)
53)Ein Molekülorbital (MO)ist der Aufenthaltsbereich eines Elektrons oder Elektronenpaares in einem Molekül (zwischen Einzelatomen; -Bindung achsensymmetrisch, -Bindung unsymmetrisch durch Beteiligung von p-Orbitalen). MOs bilden sich aus Atom- und Hybridorbitalen (Die MO-Theorie ersetzt die frühere Valenzstruktur-, valence-bond - oder VB-Theorie, die bildende Elektronenpaare beschreibt). Beispiel 1: Zwei Wasserstoffatome bilden ein bindendes Molekülorbital (links) und ein leeres, antibindendes MO (rechts). 
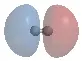 Bildquelle: Von Benjah-bmm27 - Eigenes Werk, Gemeinfrei, https://commons.wikimedia.org/w/index.php?curid=1970739) Beispiel 2: Ein Fluorwasserstoff-Molekülorbital entsteht im Fluorwasserstoff-Molekül H-F, wenn ein 1s-Atomorbital vom Wasserstoffatom H (oben links) und ein 2p-Atomorbitakl vom Fluoratom F (oben rechts, hantelförmig) zu einem MO verschmelzen (unten):
Bildquelle: Von Benjah-bmm27 - Eigenes Werk, Gemeinfrei, https://commons.wikimedia.org/w/index.php?curid=1970739) Beispiel 2: Ein Fluorwasserstoff-Molekülorbital entsteht im Fluorwasserstoff-Molekül H-F, wenn ein 1s-Atomorbital vom Wasserstoffatom H (oben links) und ein 2p-Atomorbitakl vom Fluoratom F (oben rechts, hantelförmig) zu einem MO verschmelzen (unten): 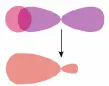 Bildquelle: Von Leyo - Eigenes Werk, based on Datei:MOHF.jpg by Benutzer:Hati, Gemeinfrei, über: https://commons.wikimedia.org/w/index.php?curid=8948600
Bildquelle: Von Leyo - Eigenes Werk, based on Datei:MOHF.jpg by Benutzer:Hati, Gemeinfrei, über: https://commons.wikimedia.org/w/index.php?curid=8948600
54)Molekülorbitale (MO) halten Atome in Molekülen zusammen und können polaroder unpolarsein (vgl. Merksatz 44).
Hinweis: Neben den drei Arten chemischer Bindung – der Atom-, Ionen- und Metallbindung – existieren auch Wasserstoffbrückenbindungen und koordinative Bindungen: Eine Wasserstoffbrückenbindung ist eine über Wasserstoffatome locker erfolgte Bindung zwischen zwei polaren Molekülen (Dipol-Dipol-Wechselwirkung) Eine koordinative Bindung ist eine Bindung höherer Ordnung (unabhängig von Wertigkeit und Oxidationszahl) in einem Komplex zwischen einem Nebengruppenmetall-Kation und Molekülen mit freien Elektronenpaaren (Liganden). Ein Ligand ist ein Molekül mit freien Elektronenpaaren in einem Komplex, die Koordinationszahl gibt an, mit wieviel „einzähnigen“ Liganden sich ein Zentralatom in einem Komplex umgeben kann.
8) Alkali- und Erdalkalimetalle
55)Elemente und ihre Verbindungen sind – mit Ausnahme von Kohlenstoff-Wasserstoff-Verbindungen – das Thema der Anorganischen Chemie.
56) Verbindungensind chemisch zerlegbare Reinstoffe, keine Stoffgemische.
Hinweis: Zu den Stoffgemischen gehören z.B. Emulsinen, Suspensionen und Aerosole: Eine Emulsion ist ein Stoffgemenge aus zwei nicht mischbaren Flüssigkeiten (z.B. Öl in Wasser). Eine Suspension ist ein Stoffgemenge / eine Aufschlämmung von unlöslichem Feststoff in einer Flüssigkeit. Ein Aerosol ist ein Stoffgemisch von Flüssigkeit in Gas (z.B. Nebel), ein Kolloid ist eine Aufschlämmung von Feststoff in Flüssigkeit, die sich ohne Ausflockung nicht filtrieren lässt.
57)Das Zerlegen von Verbindungen( Analyse) ist deshalb immer eine chemische Reaktion – im Unterschied zu Aggregatzustandsänderungen und zu den Stofftrennverfahren, bei denen Stoffgemische in Reinstoffe aufgetrennt werden.
Hinweis: Zu den Stofftrennverfahren gehören Filtration, Destillation und Extraktion. Aggregatzustandsänderungen sind Erstarren (Gefrieren), Sieden, Sublimieren und Kondensieren.
Definitionen dazu: Kondensation ist der Übergang vom gasförmigen zum flüssigen Aggregatzustand, Sublimation ist der Übergang vom festen zum gasförmigen Aggregatzustand. Eine Filtration ist ein Stofftrennverfahren zur Abtrennung unlöslicher Feststoffe aus einer Flüssigkeit (Suspension). Eine Destillation ist ein Stofftrennverfahren zur Auftrennung eines Flüssigkeiten-Gemisches durch Erhitzen über den Siedepunkt der flüchtigeren Substanz mit anschließender Kondensation zur Abtrennung derselben („Destillat“; ein Azeotrop ist ein durch Destillation nicht weiter auftrennbares Flüssigkeitsgemisch). Eine Extraktion ist ein Stofftrennverfahren zur Auftrennung eines Feststoffgemisches, bei dem dessen lösliche Bestandteile durch eine Flüssigkeit (Extraktionsmittels) abgetrennt werden („Extrakt“, „Auszug“). Eine Sedimentation ist die Bildung eines Niederschlages („Ausfällung“) aus einer Suspension, indem der unlösliche Feststoff (das „Sediment“) schwerkraftbedingt absinkt, sich unten absetzt.
58)Die Elemente werden in Haupt- und Nebengruppeneingeteilt (Vgl. Merksätze Nr. 9, 15, 35 und Periodensystem). Die wichtigsten Hauptgruppen heißen: 1: Alkalimetalle, 2: Erdalkalimetalle 7: Halogene 8: Edelgase Metalle stehen im Periodensystem links und unten, Nichtmetalle oben und rechts.

Elemente der fünften Hauptgruppe, von links nach rechts: Stickstoff, Phosphor, Arsen und Bismut - der metallische Charakter nimmt in dieser Gruppe von links nach rechts zu (im Periodensystem: Von oben nah unten; eig. Foto).
59)Die 1. Hauptgruppe im Periodensystem sind die Alkalimetalle(ohne Wasserstoff in „Vorperiode“, von arab. „ al kalja “ = Asche, aus Asche u. ähnl. herstellbar), 2. Hauptgruppe: Erdalkalimetalle(Oxide „erdig“). Sie alle sind metallisch (Leichtmetalle), sehr empfindlich (unedel) und brennbar. Sie reagieren mit Luftsauerstoff (O 2) zu Oxiden(Anion O 2-)und mit Wasser zu Laugen( Hydroxiden, Anion OH -) und Wasserstoffgas ( H 2).
Beispiele: 4 Li + O 2 → 2 Li 2O (aus Li +und O 2-2:1) 2 Mg + O 2 → 2 MgO (aus Mg 2++ O 2-1:1) 2 Li + 2 H 2O → 2 LiOH + H 2(Li +/OH -) Mg + 2 H 2O → 2 Mg(OH) 2(aus Mg 2+/ OH -1:2)

Alkalimetalle färben Flammen, hier z.B. im Feuerwerk (eig. Foto)
Читать дальше

 sp 3
sp 3  sp 2Bildquelle: User:sven, wikimedia commons, über: https://de.wikipedia.org/wiki/Hybridorbital#/media/File:Sp3-Orbital.svg (Lizenz: the Creative Commons Attribution-Share Alike 3.0 Unported)
sp 2Bildquelle: User:sven, wikimedia commons, über: https://de.wikipedia.org/wiki/Hybridorbital#/media/File:Sp3-Orbital.svg (Lizenz: the Creative Commons Attribution-Share Alike 3.0 Unported)
 Bildquelle: Von Benjah-bmm27 - Eigenes Werk, Gemeinfrei, https://commons.wikimedia.org/w/index.php?curid=1970739) Beispiel 2: Ein Fluorwasserstoff-Molekülorbital entsteht im Fluorwasserstoff-Molekül H-F, wenn ein 1s-Atomorbital vom Wasserstoffatom H (oben links) und ein 2p-Atomorbitakl vom Fluoratom F (oben rechts, hantelförmig) zu einem MO verschmelzen (unten):
Bildquelle: Von Benjah-bmm27 - Eigenes Werk, Gemeinfrei, https://commons.wikimedia.org/w/index.php?curid=1970739) Beispiel 2: Ein Fluorwasserstoff-Molekülorbital entsteht im Fluorwasserstoff-Molekül H-F, wenn ein 1s-Atomorbital vom Wasserstoffatom H (oben links) und ein 2p-Atomorbitakl vom Fluoratom F (oben rechts, hantelförmig) zu einem MO verschmelzen (unten):  Bildquelle: Von Leyo - Eigenes Werk, based on Datei:MOHF.jpg by Benutzer:Hati, Gemeinfrei, über: https://commons.wikimedia.org/w/index.php?curid=8948600
Bildquelle: Von Leyo - Eigenes Werk, based on Datei:MOHF.jpg by Benutzer:Hati, Gemeinfrei, über: https://commons.wikimedia.org/w/index.php?curid=8948600












