13.Kano SC, Binon PP, Curtis DA. A classification system to measure the implant-abutment microgap. Int J Oral Maxillofac Implants 2007;22:879–885.
14.Dibart S, Warbington M, Su MF, Skobe Z. In vitro evaluation of the implant-abutment bacterial seal: The locking taper system. Int J Oral Maxillofac Implants 2005;20:732–737.
15.Gross M, Abramovich I, Weiss EI. Microleakage at the abutment-implant interface of osseointegrated implants: A comparative study. Int J Oral Maxillofac Implants 1999;14:94–100.
16.Quirynen M, Bollen CM, Eyssen H, van Steenberghe D. Microbial penetration along the implant components of the Brånemark system. An in vitro study. Clin Oral Implants Res 1994;5:239–244.
17.Zipprich H, Miatke S, Hmaidouch R, Lauer HC. A new experimental design for bacterial microleakage investigation at the implant-abutment interface: An in vitro study. Int J Oral Maxillofac Implants 2016;31:37–44.
18.Hermann JS, Schoolfield JD, Schenk RK, Buser D, Cochran DL. Influence of the size of the microgap on crestal bone changes around titanium implants. A histometric evaluation of unloaded non-submerged implants in the canine mandible. J Periodontol 2001;72:1372–1383.
19.King GN, Hermann JS, Schoolfield JD, Buser D, Cochran DL. Influence of the size of the microgap on crestal bone levels in non-submerged dental implants: A radiographic study in the canine mandible. J Periodontol 2002;73:1111–1117.
20.Hermann F, Lerner H, Palti A. Factors influencing the preservation of the periimplant marginal bone. Implant Dent 2007;16:165–175.
21.Ericsson I, Persson LG, Berglundh T, Marinello CP, Lindhe J, Klinge B. Different types of inflammatory reactions in peri-implant soft tissues. J Clin Periodontol 1995;22:255–261.
22.Ericsson I, Nilner K, Klinge B, Glantz PO. Radiographical and histological characteristics of submerged and non-submerged titanium implants. An experimental study in the labrador dog. Clin Oral Implants Res 1996;7:20–26.
23.Hermann JS, Buser D, Schenk RK, Schoolfield JD, Cochran DL. Biologic width around one- and two-piece titanium implants. Clin Oral Implants Res 2001;12:559–571.
24.Hermann JS, Cochran DL, Nummikoski PV, Buser D. Crestal bone changes around titanium implants. A radiographic evaluation of unloaded nonsubmerged and submerged implants in the canine mandible. J Periodontol 1997;68:1117–1130.
25.Broggini N, McManus LM, Hermann JS, et al. Persistent acute inflammation at the implant-abutment interface. J Dent Res 2003;82:232–237.
26.Broggini N, McManus LM, Hermann JS, et al. Peri-implant inflammation defined by the implant-abutment interface. J Dent Res 2006;85:473–478.
27.Piattelli A, Vrespa G, Petrone G, Iezzi G, Annibali S, Scarano A. Role of the microgap between implant and abutment: A retrospective histologic evaluation in monkeys. J Periodontol 2003;74:346–352.
28.Linkevičius T, Apse P, Grybauskas S, Puišys A. Reaction of crestal bone around implants depending on mucosal tissue thickness. A 1-year prospective clinical study. Stomatologija 2009;11:83–91.
29.Davarpanah M, Martinez H, Tecucianu JF. Apical-coronal implant position: Recent surgical proposals. Technical note. Int J Oral Maxillofac Implants 2000;15:865–872.
30.Holt RL, Rosenberg MM, Zinser PJ, Ganeles J. A concept for a biologically derived, parabolic implant design. Int J Periodontics Restorative Dent 2002;22:473–481.
31.Todescan FF, Pustiglioni FE, Imbronito AV, Albrektsson T, Gioso M. Influence of the microgap in the peri-implant hard and soft tissues: A histomorphometric study in dogs. Int J Oral Maxillofac Implants 2002;17:467–472.
32.Lazzara RJ, Porter SS. Platform switching: A new concept in implant dentistry for controlling postrestorative crestal bone levels. Int J Periodontics Restorative Dent 2006;26:9–17.
33.Gardner DM. Platform switching as a means to achieving implant esthetics. N Y State Dent J 2005;71:34–37.
34.Prosper L, Redaelli S, Pasi M, Zarone F, Radaelli G, Gherlone EF. A randomized prospective multicenter trial evaluating the platform-switching technique for the prevention of postrestorative crestal bone loss. Int J Oral Maxillofac Implants 2009;24:299–308.
35.Vela-Nebot X, Rodríguez-Ciurana X, Rodado-Alonso C, Segalà-Torres M. Benefits of an implant platform modification technique to reduce crestal bone resorption. Implant Dent 2006;15:313–320.


3
INSERTIONSTIEFE
Die Insertionstiefe ist ein wichtiges Konzept, um eine Situation ohne Knochenverlust zu erreichen. Fälschlicherweise besteht die Annahme, dass alle Implantate auf derselben Höhe in den Knochenkamm gesetzt werden können. Tatsächlich hängt die Insertionstiefe aber vom Implantatdesign ab. Die wichtigsten erhältlichen Implantatdesigns sind Standardverbindungen (ohne Platform-Switching), Implantate auf Gewebeniveau (Tissue-Level-Implantate) und Implantate mit Platform-Switching ( Abb. 3-1). Wie bereits in Kapitel 2besprochen, sollte ein Implantat auf Gewebeniveau mit poliertem Hals immer oberhalb des Knochenkamms platziert werden, sodass nur die raue Oberfläche zur Osseointegration mit dem Knochen Kontakt hat. Implantate auf Knochenniveau (Bone-Level-Implantate) können hingegen unterschiedlich tief gesetzt werden: (1) auf Knochenhöhe (krestal), (2) suprakrestal oder (3) subkrestal ( Abb. 3-2).
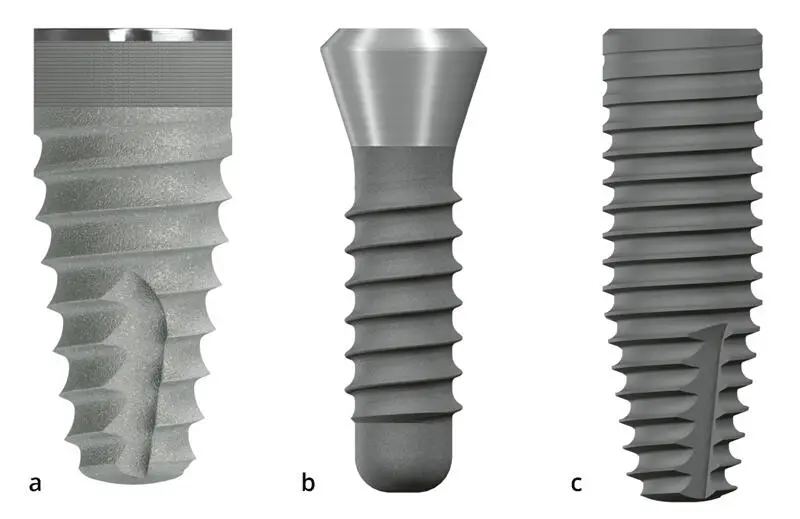
Abb. 3-1 (a) Ein Implantat auf Knochenniveau ohne Platform-Switching. (b) Ein Implantat auf Gewebeniveau. (c) Ein Implantat auf Knochenniveau mit Platform-Switching.
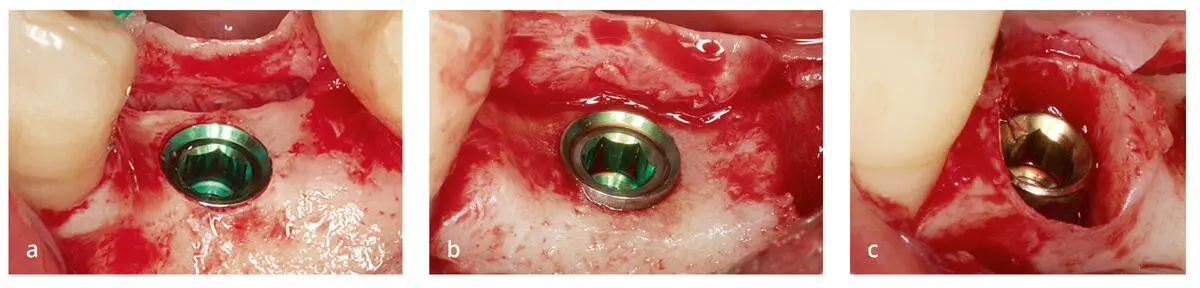
Abb. 3-2Die verschiedenen möglichen Positionen für Implantate auf Knochenniveau ohne Platform-Switching: (a) krestal, (b) suprakrestal und (c) subkrestal (nicht empfohlen). Diese Positionen sind auch bei Implantaten mit Platform-Switching möglich (s. Abb. 3-7).
Implantate auf Knochenniveau ohne Platform-Switching
Es wurde gezeigt, dass Implantate auf Gewebeniveau suprakrestal gesetzt werden sollten, damit der Mikrospalt und der polierte Hals keinen Kontakt mit dem Knochen haben. Weniger klar ist jedoch, welche Position für Implantate auf Knochenniveau ohne Platform-Switching am besten ist. Bei krestaler Platzierung ist der Mikrospalt nicht vom Knochen isoliert, sodass es zum Knochenverlust kommt ( Abb. 3-3). Bei suprakrestaler Platzierung bekommt ein Teil der rauen Oberfläche Kontakt mit dem Weichgewebe. Ein altes litauisches Sprichwort lautet: „Jeder Stock hat zwei Enden.“ Das bedeutet, dass man bei der Lösung eines Problems darauf achten muss, sich kein neues Problem zu schaffen, das womöglich schwerwiegender ist als das Ausgangsproblem. Während die suprakrestale Position eines Implantats ohne Platform-Switching die korrekte Lage des Mikrospalts mit sicherem Abstand zum Knochen gewährt, kann sie zu unerwarteten Weichgewebeproblemen führen, da die Implantatoberfläche gegenüber dem periimplantären Weichgewebe exponiert ist. Die raue Oberfläche ist für die Osseointegration gedacht und in einigen Studien führte die Exposition der rauen Oberfläche tatsächlich häufiger zu einer Periimplantitis 1–4. Einige der aktuellen Behandlungsverfahren der Periimplantitis umfassen eine Glättung der Implantatoberfläche 5,6. Einige Tierstudien legen nahe, dass durch eine Mikroanrauung des Implantathalses eine bessere Befestigung der Weichgewebe erreicht werden könnte, klinische Evidenz gibt es dazu aber noch nicht 7,8. Andererseits ist für poliertes Titan eine sehr gute Weichgewebeverträglichkeit belegt 9 . Dies alles wirft die Frage auf, wie Implantate auf Knochenniveau ohne Platform-Switching aufgebaut sein sollten.
Читать дальше