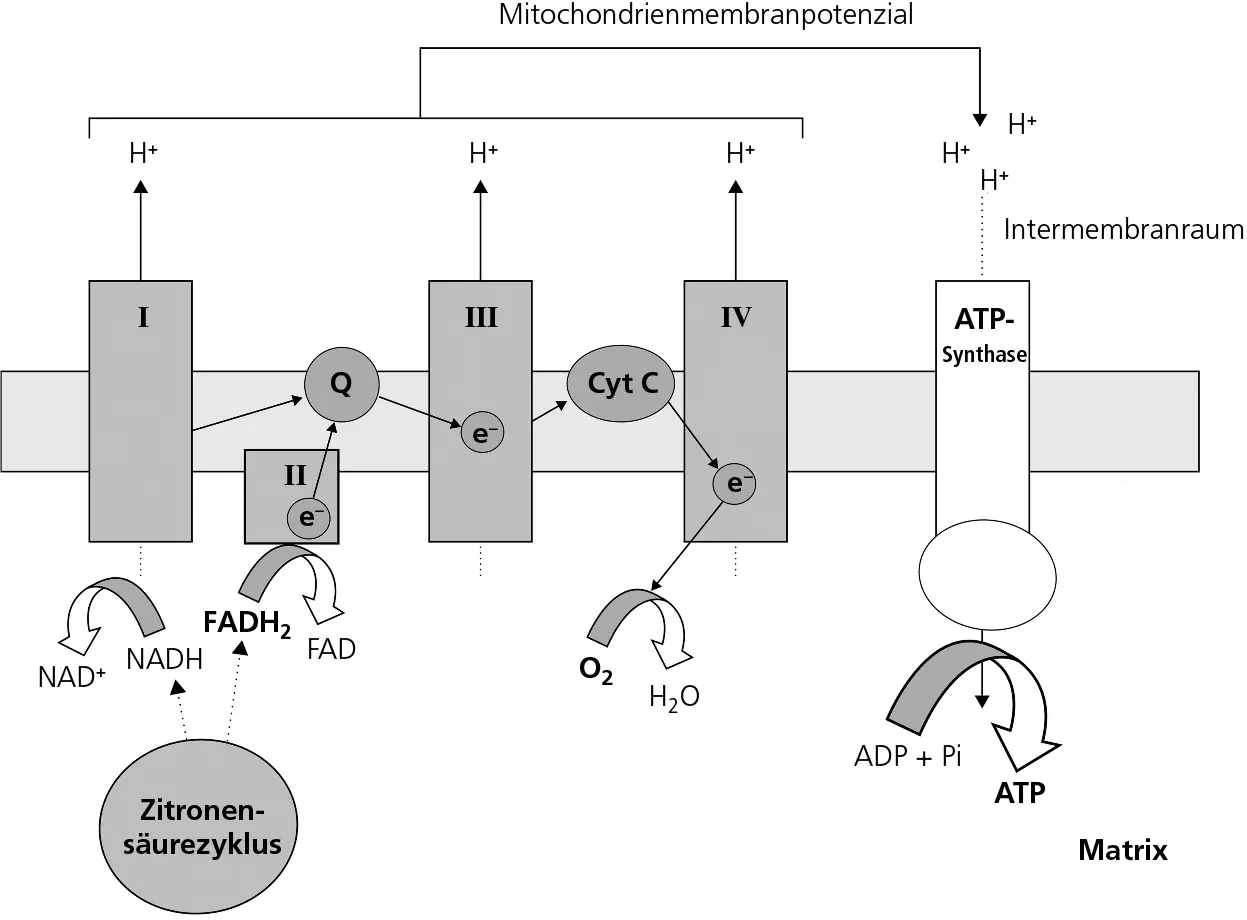
Abbildung 1.3Die Elektronentransportkette einschließlich ATP-Synthase: Der Zitronensäurezyklus erzeugt NADH und FADH 2, die in Komplex I beziehungsweise Komplex II in die Elektronentransportkette eintreten. Beide Komplexe geben die entstehenden Elektronen (e –) an Coenzym Q 10(Q) ab. Diese Elektronen wandern weiter, bis sie am Ende mit Sauerstoff (O 2) zu Wasser reagieren. In Komplex I, III und IV werden Protonen (H +) gepumpt, wodurch der Protonengradient entsteht. Über die ATP-Synthase fließen die Protonen zurück und bilden ATP.
Für alle, denen das Konzept der freien Radikale bereits vertraut ist, dürfte interessant sein, dass die endogenen freien Radikale (die wir selbst produzieren und die nicht aus anderen Quellen wie Umweltgiften stammen) in erster Linie der Elektronentransportkette entspringen. All dies wird gleich noch viel einleuchtender werden. Die Grundlagen der Elektronentransportkette und ihrer Bestandteile sind damit jedoch ausreichend erläutert.
Kohlenmonoxidvergiftung
Bei einer Kohlenmonoxidvergiftung ersetzt dieses Gift den Sauerstoff, der am Ende der Atmungskette die Elektronen aufnehmen sollte. Da diese Endabnahme nicht mehr möglich ist, kommt die Zellatmung zum Stillstand, denn die Elektronen können nicht entsorgt werden. Wird das Kohlenmonoxid nicht ausgeleitet, sterben die Mitochondrien. Das wiederum führt zum Zelltod und tötet am Ende den Menschen, der dem Kohlenmonoxid ausgesetzt war.
Komplex I: Die erste Stufe der Elektronentransportkette
Komplex I, die NADH-Dehydrogenase, ist ein großes Molekül, das sich aus 46 Proteinuntereinheiten zusammensetzt. Er spaltet zwei Elektronen von NADH ab und überträgt sie auf ein fettlösliches Carrier-Molekül, Ubiquinon. Ubiquinon ist oxidiertes CoQ10 oder „Q“. Über zwei Schritte wird CoQ10 zu Ubiquinol (QH 2) reduziert, wobei vier Protonen (H +) durch die Membran gepumpt werden und einen Protonengradienten erzeugen. An dieser Stelle in der Elektronentransportkette kommen die meisten Elektronen abhanden, die dann schädliche Superoxid-Radikale erzeugen.
Komplex II: Die zweite Stufe und eine Abkürzung zur Elektronentransportkette
Dieser einzigartige Komplex, auch als Succinat-Dehydrogenase bezeichnet, ist unmittelbar am Zitronensäurezyklus und der Elektronentransportkette beteiligt. Es handelt sich um einen kleinen Komplex aus nur vier Proteinuntereinheiten. In der Elektronentransportkette ist er der einzige Komplex, der keine Protonen pumpt. Er dient dazu, über FADH 2weitere Elektronen aus Succinat an das CoQ10 weiterzugeben. Über FADH 2kann Komplex II auch weitere Elektronendonatoren (z. B. Fettsäuren) in die Elektronentransportkette einspeisen.
Komplex III: Die Zwillinge und Meisterjongleure
Komplex III ist die Cytochrom-c-Reduktase, auch als Cytochrom-bc1-Komplex bezeichnet. Es handelt sich um ein Dimer, also einen Komplex, der aus zwei identischen, einfacheren Komplexen besteht. Jeder Teil des Dimers setzt sich aus elf Proteinuntereinheiten zusammen; insgesamt enthält Komplex III also 22 dieser Untereinheiten.
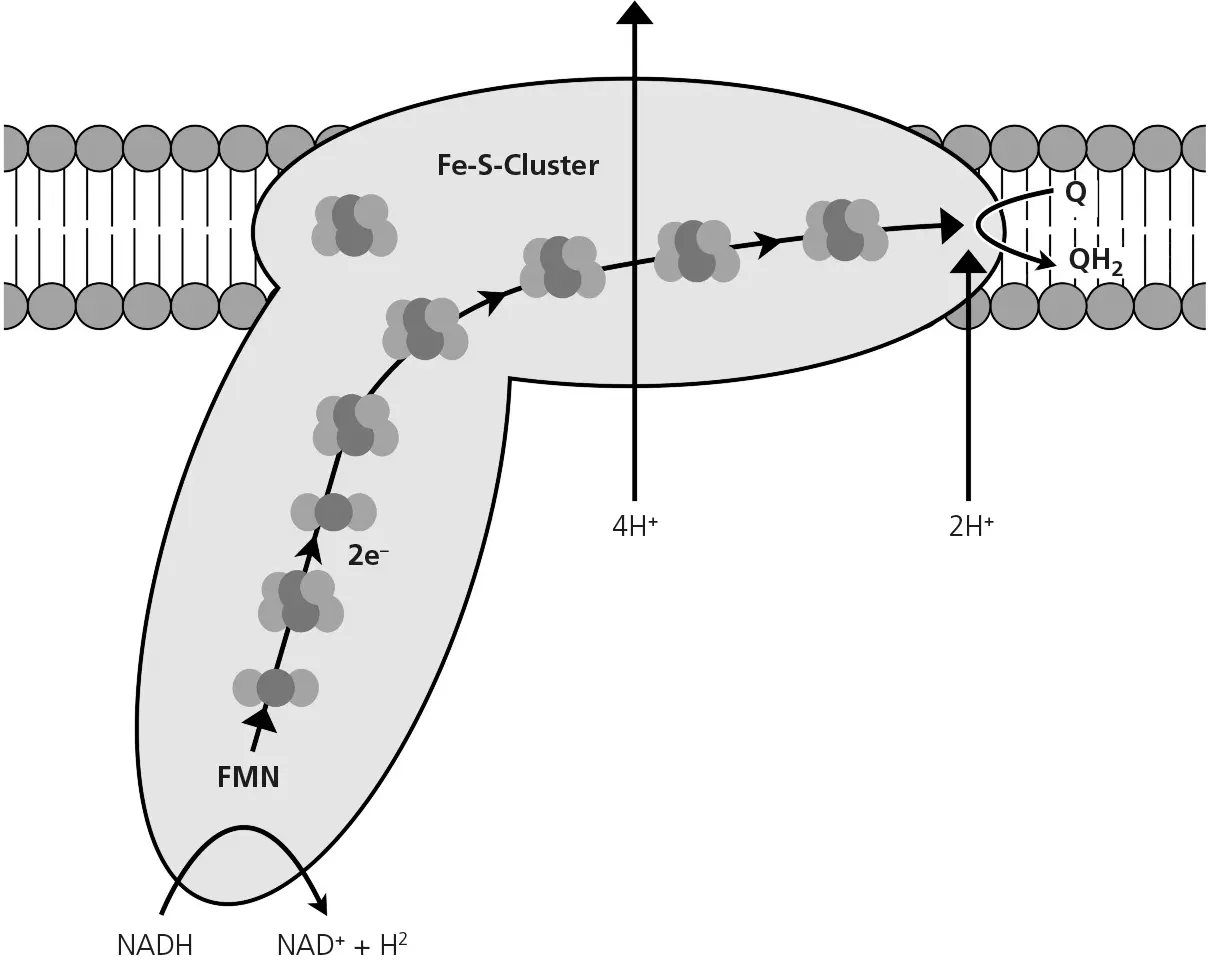
Abbildung 1.4Komplex I übernimmt Elektronen von NADH und schleust sie durch Eisen-Schwefel-Cluster (Fe-S-Cluster, auch als Eisen-Schwefel-Zentren bezeichnet) zu Coenzym Q 10(Q) Dabei ergeben sich vier Protonen (H +), die aus der Matrix in den Intermembranraum gepumpt werden.
In Komplex III läuft der Q-Zyklus ab, ein mehrstufiger Prozess, bei dem Ubiquinol (reduziertes CoQ10) zu Ubiquinon (oxidiertes CoQ10) umgewandelt wird. Bei diesem Prozess werden insgesamt vier Nettoprotonen ausgepumpt, die zum Protonengradienten beitragen.
Das ist in der Elektronentransportkette der zweithäufigste Entstehungsort, wo Elektronen ausscheren, die mit Sauerstoff dann Superoxid-Radikale bilden.
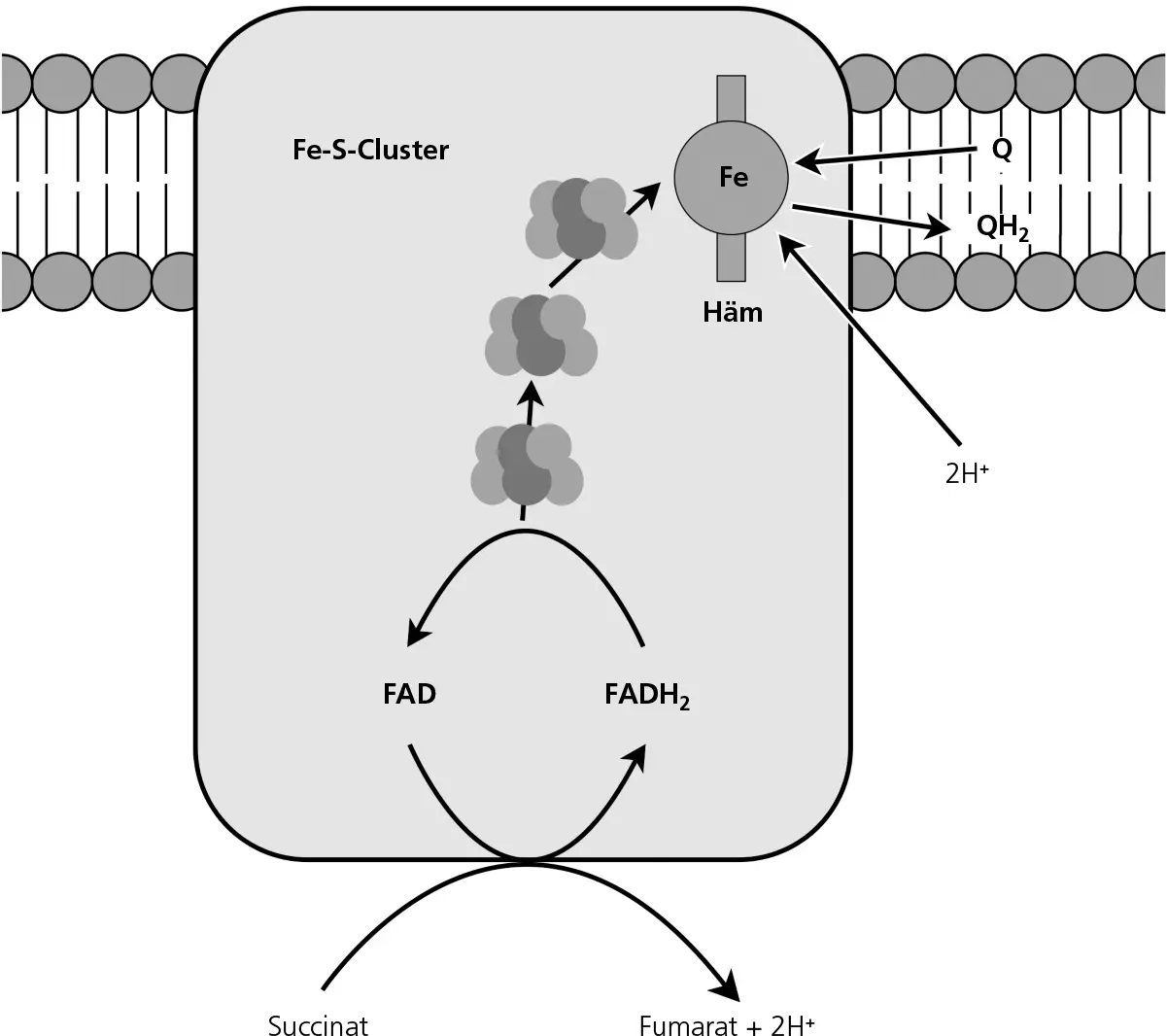
Abbildung 1.5Komplex II ist ein Bestandteil des Zitronensäurezyklus, in dem ebenfalls FADH 2entsteht. Die Elektronen aus FADH 2werden dann über Eisen-Schwefel-Cluster (Fe-S-Cluster) zu Coenzym Q 10(Q) weitergeleitet. Komplex II ist der einzige Komplex, der keine Protonen pumpt.
Komplex IV: Hier entsteht Wasser
Komplex IV oder Cytochrom-c-Oxidase besteht aus 13 Proteinuntereinheiten. In diesem Bereich werden aus vier Molekülen Cytochrom c vier Elektronen abgespalten und an molekularen Sauerstoff (O 2) weitergereicht, damit zwei Wassermoleküle entstehen können. Dabei werden zugleich vier Protonen frei, die durch die Membran gepumpt werden und zum Protonengradienten beitragen.
So speichern Kamele in der Wüste ihr Wasser
An dieser Stelle lohnt sich der Hinweis, dass Kamele in ihren Höckern keineswegs Wasser speichern, wie man es Kindern gern erklärt. Ihre Höcker sind vielmehr große Fettspeicher. Dieses Fett liefert nicht nur Energie, sondern wenn es über oxidative Phosphorylierung verstoffwechselt wird, entsteht bei Komplex IV Wasser (pro Gramm verbranntem Fett etwa 1 Gramm oder 1 Milliliter Wasser). Neben anderen Anpassungsleistungen ist dies einer der Gründe, warum Kamele so lange ohne Trinkwasser auskommen können.
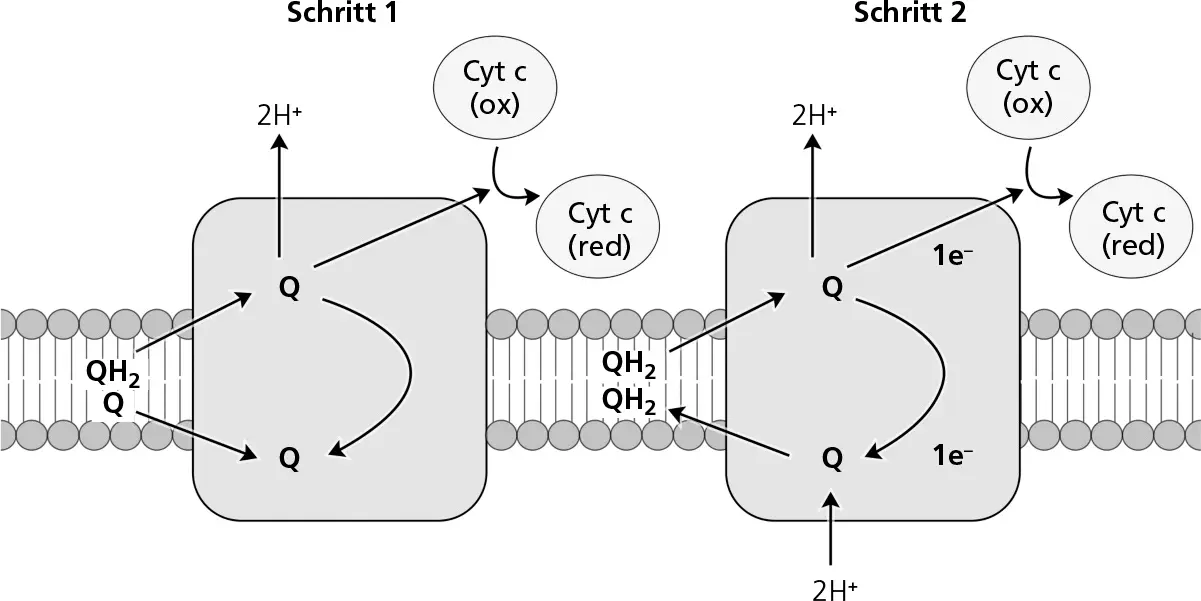
Abbildung 1.6Komplex III übernimmt über einen mehrstufigen Prozess, den Q-Zyklus, Elektronen aus der reduzierten Form von Coenzym Q10 (QH 2). Die Elektronen wandern weiter zu Cytochrom c (Cyt c), und vier Protonen (H +) gehen in den Intermembranraum über.
Cyanidvergiftung und Suizid
Cyanid (Blausäure) ist ein Gift, das bei dem Massensuizid in Jonestown, Guayana, verwendet wurde und historisch bestimmten Militärangehörigen gegeben wurde, um es bei einer eventuellen Gefangennahme zu schlucken. Es tötet durch Schließung der Elektronentransportkette. Dabei hemmt es spezifisch die Aktivität von Komplex IV, indem es die Eisenkomponente (FE) bindet, wodurch der Elektronenfluss gestoppt wird. Das aktuellste zugelassene Gegengift ist (zumindest in den USA) Hydroxocobalamin (eine Form von Vitamin B 12). Mit Cyanid reagiert es zu Cyanocobalamin (einer B 12-Variante, die in den meisten Nahrungsergänzungsmitteln vorliegt) und kann dann so über die Nieren problemlos ausgeschieden werden.
Superkomplexe: Turboschneller Elektronenfluss
Was ich gerade beschrieben habe, entspricht dem, was in der Oberstufe, aber auch an der Universität im Biologiekurs über die Elektronentransportkette gelehrt wird. Zu den zuvor beschriebenen vier Komplexen kommt die ATP-Synthase (die ich im Folgenden erkläre und die mitunter als Komplex V bezeichnet wird). Insgesamt besteht die Elektronentransportkette in den Mitochondrien somit aus fünf Enzymkomplexen, die für die ATP-Erzeugung zuständig sind. In jüngster Zeit wurde dieser Lehrsatz der Elektronentransportkette – dass in der inneren Mitochondrienmembran separate Enzyme verteilt sind – vom Modell des mitochondrialen Superkomplexes abgelöst, in dem die Atmungskomplexe stabile Verbindungen miteinander eingehen. Diese Struktur gestattet einen hoch effizienten Elektronentransfer, in dem die Distanz, die ein Elektron zwischen den Komplexen zurücklegen muss, auf einige Nanometer reduziert ist.
Читать дальше
















