
σ св. – связывающая МО 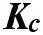
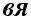
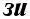

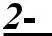
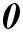

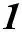 , т.е. кратность связи = 1 (ординарная связь)
, т.е. кратность связи = 1 (ординарная связь)
Для свободных МО в пространстве между ядрами наблю-
дается повышенная электронная плотность, что приводит к образованию ковалентной химической связи. Такая связь получи-ла название связывающей молекулярной орбитали. Пониженной электронной плотностью обладают разрыхляющие МО.
При образовании соединений с участием элементов 2–го периода, наряду с s-атомными орбиталями, принимают участие в образовании химических связей p-атомные орбитали (для об-легчения представляем распределение только валентных электронов).
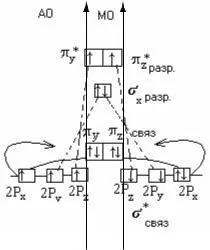
Ксвязи=(6–2)/2 =2
В результате взаимодействия 2р–орбитали возможны образования химических связей 2–х типов:
при взаимодействии двух Р–орбиталей образуется σ-связь.
при взаимодействии двух 2Р – образуется �-связь.
Метод МО является наиболее универсальным, способен объяснить многообразие физических и химических свойств, широко использовать для оценки реакционной способности и предсказания возможных свойств различных химических соединений: неорганических, органических, комплексных,
МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
В периодической системе элементов известно 16 электронов, содержащих по 1 валентному электрону, 57 элементов содержит 2 электрона, 4 элемента содержат 3 электрона, 3 элемента содержат 4 электрона, 2 элемента – 5 электронов, Ро – б электронов. У палладия – нет валентных электронов.
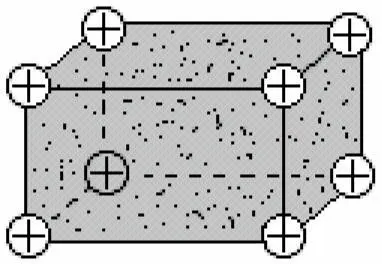
При изучении структуры кристаллов установлено, что в узлах кристаллической решетки находятся (+) ионы и нейтральные молекулы, т.е. металл представляет собой структуру (+) ионов, связанных с подвижными электронами, т.н. электронным газом.
Появление электронного газа объясняется тем, что для металла значение первого потенциала ионизации невелико. Таким образом, металлическая связь представляет собой нелокализованную (т.е. ненаправленную в пространстве) химическую связь.
Природа взаимодействия электронов с ионами имеет электростатический характер. Все многообразие физических и химических свойств металла объясняется металлической связью: ковкость, электропроводность, высокая температура плавления, магнитные свойства и т.д.
ВОДОРОДНАЯ СВЯЗЬ – связь водорода с наиболее электро-отрицательным элементом в атоме или между атомами (межмоле-
кулярная). Наличие ее в NH3, HF, H2O приводит к аномальным свойствам.
Девиз: ВСЕ В ПРИРОДЕ СТРЕМИТСЯ К МИНИМУМУ
ПОТЕНЦИАЛЬНОЙ ЭНЕРГИИ.
ВСЕЛЕННАЯ РАСШИРЯЕТСЯ.
ЛЕКЦИЯ 5
ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ.
ТЕРМОХИМИЯ, ТЕРМОДИНАМИКА
План:
Общие закономерности протекания химических процессов.
Законы термохимии.
Принцип Бертло.
Энтропия.
Энергия Гиббса.
Общая энергия Е любой молекулярной системы равняется
Е = Ек + Еп + U,
где Ек – кинетическая; Еп – потенциальная;
U – внутренняя энергия системы.
Под внутренней энергией и понимают совокупность энергии электрона, колебаний ядер, вращательную и сумму энергий их взаимодействий.
В настоящее время не существует теоретических и экспериментальных методов определения внутренней энергии любой системы. Можно определить с помощью различных физических и хи-
мических методов только лишь изменение внутренней энергии.
Известно, что в процессе химических реакций происходит выделение или поглощение энергии. В этих случаях теплота реакции, в соответствии с первым началом термодинамики, расходуется, как на совершение работы, так и на изменение внутренней энергии.
Q = U + A
Изменение внутренней энергии не зависит от способа проведения процесса, а зависит от начального и конечного состояния системы.
1) Все химические процессы проходят или при постоянном давлении или при постоянном объеме.
Читать дальше
Конец ознакомительного отрывка
Купить книгу


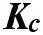
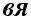
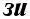

 , т.е. кратность связи = 1 (ординарная связь)
, т.е. кратность связи = 1 (ординарная связь)












