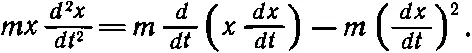
Мы разбили первоначальное слагаемое на два и должны усреднить их оба. Посмотрим, чему же равно произведение х на скорость. Это произведение не изменяется со временем, потому что, когда частица попадает в заданную точку, она уже не помнит, где она была раньше, и характеризующие такие ситуации величины не должны зависеть от времени. Поэтому среднее значение этой величины равно нулю. У нас осталось лишь mv 2, а об этой величине нам кое-что известно: среднее значение mv 2/2 равно 1/ 2 kT . Следовательно, мы установили, что
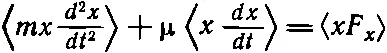
влечет за собой
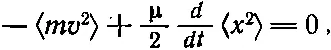
или
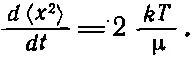 (41.20)
(41.20)
Это значит, что средний квадрат радиус-вектора частицы 2> к моменту t равен
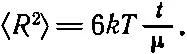 (41.21)
(41.21)
Таким образом, мы и в самом деле можем выяснить, как далеко уйдут частицы! Сначала нужно изучить реакцию частицы на постоянную силу, выяснить скорость дрейфа частицы под действием известной силы (чтобы определить μ), а тогда мы сможем узнать, далеко ли расползутся беспорядочно движущиеся частицы. Полученное нами уравнение имеет большую историческую ценность, потому что на нем основан один из первых способов определения постоянной k . Ведь в конце концов можно измерить величину μ, и время, определить расстояние, на которое удалится частица, и получить средние значения. Почему так важно определить точное значение k? Потому что по закону PV = RT для моля можно измерить R , которое равно произведению числа атомов в моле на k . Моль когда-то определялся как столько-то граммов кислорода 16 (теперь для этой цели используют углерод), поэтому числа атомов в моле сначала не знали. Это, конечно, интересный и важный вопрос. Каковы размеры атомов? Много ли их? Таким образом, одно из самых ранних определений числа атомов свелось к определению того, далеко ли уйдут мельчайшие соринки, пока мы будем терпеливо разглядывать их в микроскоп в течение строго определенного времени. После этого можно было найти и постоянную Больцмана k , и число Авогадро N 0, потому что R к этому времени было уже измерено.
Глава 42 ПРИМЕНЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ
Эта глава посвящена дальнейшим применениям кинетической теории. В предыдущей главе мы подчеркнули один из выводов этой теории, что средняя кинетическая энергия каждой степени свободы молекулы или любого другого объекта равна 1/ 2 kT . Сейчас центральным пунктом нашего изложения будет утверждение о том, что отнесенная к единице объема вероятность обнаружить частицу в том или ином месте пропорциональна ехр(-п.э./kT). (Это утверждение мы используем в ряде задач.)
Явления, которые мы собираемся изучить, довольно сложны: испарение жидкости, вылет электронов с поверхности металла или химическая реакция, в которой участвует много атомов. В таких случаях кинетическая теория не дает простых и точных предписаний, ситуация слишком сложна для этого. Поэтому выводы этой главы, за исключением особо оговоренных, весьма неточны. Мы только подчеркнем, что, исходя из кинетической теории, можно более или менее хорошо понять эти явления. Но гораздо более точное представление о них дают термодинамические аргументы или некоторые измерения отдельных критических величин.
Однако полезно знать, хотя бы очень приблизительно, почему то, что происходит, происходит именно так. Тогда, натолкнувшись на явление, которое содержит в себе нечто, чего мы еще не видели, или то, что проанализировать мы еще не собрались, мы, может быть, сможем более или менее точно сказать, что произошло. Такой анализ будет в высшей степени неточным, но в общих чертах верным — верным по сути, но чуть-чуть упрощенным, скажем, в некоторых тонких деталях.
Разберем первый пример — испарение жидкости. Предположим, что большой ящик при заданной температуре заполнен жидкостью и паром поровну. Будем считать, что средние расстояния между молекулами пара довольно велики, а вот в жидкости они упакованы плотно. Задача состоит в том, чтобы определить число молекул, находящихся в газовой фазе, по сравнению с числом молекул, находящихся в жидкости. Какова плотность пара при заданной температуре и как она зависит от температуры?
Читать дальше

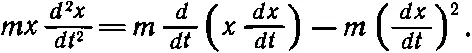
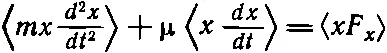
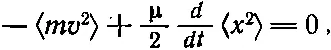
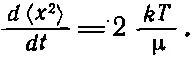 (41.20)
(41.20)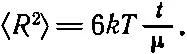 (41.21)
(41.21)




