Page 41
Ein Meister der Verkleidung: das Weiche, Harte, Runde
Verbindet Kohlenstoff sich mit Wasserstoff, stellt dies den Übergang von der anorganischen zur organischen Chemie dar. 19Dies ist eine wichtige Trennlinie innerhalb der Welt der Chemie. Ausgangspunkt der organischen Chemie ist die für lebende Materie typische Verbindung von Kohlenstoff mit Wasserstoff. Das einfachste organische Molekül ist das Methan (CH 4), häufig ein Produkt lebender Organismen, trotzdem aber kein Bestandteil des Lebens selbst. Ein Großteil der schier unendlich vielen organischen Verbindungen sind synthetischen Ursprungs. Das Wort organisch muss deshalb aus einem anderen Blickwinkel betrachtet werden als in anderen Bereichen. So gilt zum Beispiel das Insektizid DDT (Dichlordiphenyltrichlorethan), eine Kohlenstoff-Chlor-Verbindung, bestehend aus zwei sechseckigen Kohlenstoffringen mit angelagerten Chloratomen, aus Sicht eines Chemikers als organische Verbindung, während die biologisch-organische Landwirtschaft gerade dadurch gekennzeichnet ist, dass weder DDT noch andere Spritzmittel zur Anwendung kommen. Die Chemiker berufen sich, was die Bezeichnung »Organische Chemie« angeht, auf eine 120 Jahre alte Tradition. Bemerkenswert ist aber auch der Molekülaufbau des DDTs, denn während die chemische Formel Cl 5H 9C 14lautet, also 5 Chlor-, 9 Wasserstoff- und 14 Kohlenstoffatome, stellt man die Strukturformel in der Regel wie folgt dar:
Page 42 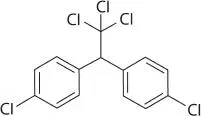
Abbildung 3: DDT (Dichlordiphenyltrichlorethan) – ein organisches Molekül, das in der biologisch-organischen Landwirtschaft aber verboten ist. In jeder Ecke der Sechsecke sitzt ein Kohlenstoffatom.
Es wird bei dieser Darstellung davon ausgegangen, dass in jeder Ecke und an jeder Bindung ein Kohlenstoffatom sitzt, was zu den insgesamt 14 Kohlenstoffatomen führt. In der organischen Chemie ist das derart selbstverständlich, dass man sich nicht einmal mehr die Mühe macht, die C-Atome einzuzeichnen. Genauso selbstverständlich ist die Tatsache, dass die 9 nicht erkennbaren H-Atome die vierte Bindung jedes C-Atoms, und die Doppelstriche Doppelbindungen darstellen (Kohlenstoff hat vier sog. Außenelektronen und damit vier normale Bindungsmöglichkeiten).
Grundsätzlich kommt Kohlenstoff in der Natur in drei reinen Formen vor: Graphit und Diamant sind schon lange bekannt, erst in jüngerer Zeit entdeckt wurde hingegen das Fulleren . Jeder weiß, dass sowohl das »Blei« im Bleistift als auch der Diamant aus reinem Kohlenstoff bestehen, und es fasziniert uns, dass das extrem Weiche und Billige und das extrem Harte und Teure aus derselben Substanz bestehen sollen. Dass der Diamant nicht nur in die Welt des Kohlenstoffs gehört, sondern aus reinem Kohlenstoff besteht, konnte bereits 1772 von Lavoisier nachgewiesen werden. Wenig später stellte sich dann heraus, dass das »Blei« im Bleistift, kein Blei war, wie man lange geglaubt hatte, sondern ebenfalls Kohlenstoff. Sowohl der Diamant als auch der Graphit geben bei ihrer Verbrennung die ihrem Gewicht entsprechende Menge CO 2ab.
Page 43
Einer der weltweit größten und bekanntesten Diamanten ist der Koh-i-Noor, der mit seinen ursprünglich 793 Karat über 5.000 Jahre hinweg von einem Herrscherhaus zum anderen weitergegeben wurde. 20Der allergrößte bisher bekannt Diamant ist der Cullinan-Diamant mit 3.106 Karat (620 Gramm) im ungeschliffenen Zustand, gefunden 1905 in Südafrika. Die seit Jahrhunderten andauernde Faszination für Diamanten ist sicher durch ihre Seltenheit und Beständigkeit zu erklären. Dabei ist auch die Lebensdauer von Diamanten nicht unbegrenzt, ja, man kann sie sogar verbrennen. Ihr Schmelzpunkt liegt bei 3.200 °C und ihr Siedepunkt bei 4.200 °C. An der Luft brennt ein Diamant aber schon bei 800 °C, nach der simplen Reaktionsgleichung C+O2=CO2. Aber wie kann ein und derselbe Stoff Ausgangspunkt dieser Extreme sein? Noch verblüffender als diese Frage ist die Tatsache, dass aus Graphit Diamant werden kann und aus Diamant Graphit, vorausgesetzt man setzt sie der richtigen Kombination aus Druck und Temperatur aus.
Der älteste Graphit, den wir kennen, ist möglicherweise auch ein Beweis für das älteste Leben hier auf diesem Planeten. Er wurde in einer Schicht von 3,8 Milliarden Jahre alten Sedimentgesteinen in Grönland gefunden und ist so rein, dass man damit schreiben kann. Er enthält das Isotop 13C (auf das wir noch zu sprechen kommen werden), was ein starker Hinweis auf seinen biologischen Ursprung ist. Einen abschließenden Beweis dafür werden Page 44wir aber nie erhalten. Der Graphit besteht aus Schichten von zu Sechsecken verbundenen Kohlenstoffatomen. Die Schichten werden von schwachen Bindungskräften zusammengehalten, sodass sie sehr leicht getrennt werden können. Dafür reicht schon die Reibung der Mine auf dem Papier. Im Diamant hingegen sind die Kohlenstoffatome in einem nahezu unangreifbaren Netz miteinander verbunden und bilden so einen der härtesten Stoffe, die wir kennen.

Abbildung 4: Diamant, Graphit und Fulleren sind die drei Hauptformen von reinem Kohlenstoff. Während der Diamant seine souveräne Stärke durch das Kristallgitter erhält, ist die Weichheit des Graphits auf dessen Schichtstruktur zurückzuführen. Das Fulleren hingegen ist wie ein Fußball aufgebaut und setzt sich aus 60 C-Atomen zusammen.
Diamant entsteht unter extremem Druck bei hohen Temperaturen. Natürliche Diamanten stammen sozusagen aus Druckkammern tief im heißen Inneren der Erde. Bei synthetischen Diamanten versucht man diese Bedingungen nachzuahmen, in dem man Kohlenstoffgas im Labor hohen Temperaturen und hohem Druck aussetzt. Chemisch gesehen sind auch das echte Diamanten, aber da sie auf künstlichem Wege entstanden sind, werden sie auf dem Edelsteinmarkt viel weniger geschätzt. Es ist interessant zu betrachten, welchen Vorrang das Natürliche vor dem Künstlichen hat. Das Natürliche gilt als »echt«, während das Synthetische als »unecht« dargestellt wird – egal ob das Produkt chemisch gesehen Page 45komplett identisch ist. Vermutlich akzeptieren wir nur in der Pharmazie die synthetischen Kopien der für die Gesundheit relevanten komplexen natürlichen Kohlenstoff verbindungen.
Es wird heftig diskutiert, wer als erster künstliche Diamanten hergestellt hat. Sicher ist, dass es bereits 1955 der General Electric Company gelungen ist, künstliche Diamanten in großem Stil herzustellen, wodurch der Wert der Firmenaktien an einem Tag um 300 Millionen Dollar anstieg. 21Heute übersteigt die jährliche Produktion synthetischer Diamanten 100 Tonnen pro Jahr. In erster Linie werden sie für industrielle Zwecke verwendet.
Mehr als 200 Jahre nach Lavoisier stellte sich heraus, dass der Kohlenstoff mit noch weiteren Überraschungen aufwarten kann. Kohlenstoff existiert nämlich nicht nur in den reinen Formen Diamant und Graphit. 1985 wurde eine völlig andere Form einer C-Verbindung entdeckt: Das Fulleren. Der merkwürdige Name leitet sich von dem noch seltsameren ursprünglichen Namen Buckminsterfulleren ab, benannt nach dem Architekten Richard Buckminster Fuller 22, der fantastische Kuppeln entwarf, die aus Fünf-und Sechsecken zusammengesetzt waren.
Die Entdeckung des ersten Fullerens basierte auf einem Zufall. Es war das unerwartete Nebenprodukt eines komplizierten Versuches. Um langkettigen Kohlenwasserstoffen auf die Spur zu kommen, wie sie im Inneren von Sternen entstehen, wurden die Prozesse im Inneren eines Gasplaneten simuliert. Bei der Auswertung des Experiments entdeckte man Moleküle aus exakt 60 Page 46Kohlenstoffatomen. Ein chemisches Retortenbaby, das sich in allem von der bis dato bekannten Kohlenstoffchemie unterschied. Kohlenstoff kann sehr vielfältige Strukturen mit einer extrem unterschiedlichen Anzahl von Kohlenstoffatomen annehmen. Die Tatsache, dass all diese Moleküle exakt 60 Atome enthielten, deutete darauf hin, dass es sich um eine spezielle Struktur, eine Art geschlossene Einheit, handelte. (Leider ist das nichts, was man so einfach unter dem Mikroskop untersuchen kann.)
Читать дальше














