Es stellt sich allerdings die Frage, ob es für uns überhaupt aussichtsreich ist, auf das Auffinden eines Todesgens zu hoffen. Bei fast allen höheren Lebewesen und mit großer Wahrscheinlichkeit auch beim Menschen existieren nämlich keinerlei Anzeichen für die Existenz wirklicher Alterungsgene, die sich quasi bei einem bestimmten Alter oder Lebensereignis einschalten oder deren Aufgabe es gar ist, Altern und Tod zu verursachen. Im ersten Teil des Buches haben wir gesehen, dass sich die Alterung beim Menschen aus vielen verschiedenen Gründen eingeschlichen hat und sehr unterschiedliche Gene daran beteiligt sind; auch pleiotrope Gene, die gleichzeitig wichtige positive Aufgaben haben. (Vgl. Abschnitt "Warum die Natur sich Altern leisten kann")
Bleibt die Frage, inwieweit der Teilungsstopp unserer Zellen als eine Art Todes- oder Alterungsbefehl wirkt. Sehen wir uns die Sache etwas genauer an.
Damit aus einer Zelle zwei neue voll funktionstüchtige Tochterzellen entstehen können, muss der im Zellkern gespeicherte Bauplan exakt kopiert werden. Schon in den 30er-Jahren des 20. Jahrhunderts fand man heraus, dass dabei an den Informationssträngen angelagerte Endkappen eine entscheidende Rolle spielen. Der spätere Nobelpreisträger James D. Watson konnte 1972 zeigen, warum diese Endkappen, die Telomere getauft wurden, so wichtig sind. Der Kopiervorgang kann die äußersten Enden der DNA-Stränge aus technischen Gründen nicht optimal erfassen. Ein unvollständiges Ablesen aber hätte fatale Folgen für weitere Zellgenerationen.
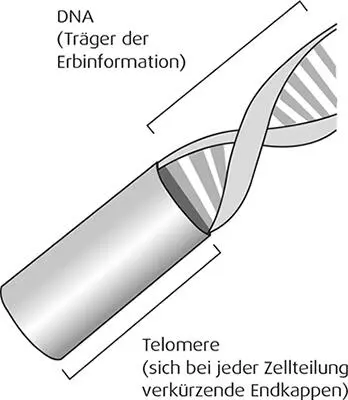
Die quasi überstehenden Endkappen (Telomere) sorgen dafür, dass die komplette DNA gelesen werden kann, allerdings dann auf Kosten der äußeren Enden dieser Telomere. Das heißt, mit jeder Zellteilung werden die Telomere kürzer. Erreicht die Telomerlänge einen kritischen Wert, muss die Zelle weitere Teilungen einstellen, wenn sie Ablesefehler vermeiden will. Das Ende ihrer Teilungsfähigkeit ist erreicht.
Telomerase – Enzym der Unsterblichkeit
Die Endstücke der Chromosomen (Informationsstränge) geben also bei jeder Zellteilung ein Stück von sich ab und ermöglichen so ein komplettes Ablesen der genetischen Information, bis sie sozusagen aufgebraucht sind. Eine gefahrlose weitere Teilung ist dann für die Zelle nicht mehr möglich.
„Stopp!“, werden Sie nun vielleicht sagen, „es gibt aber doch Einzeller wie beispielsweise Bakterien, die sich unentwegt durch Teilung fortpflanzen. Wie können diese Zellen sich wieder und wieder teilen, ohne dass die Endstücke ihrer Chromosomen irgendwann zu kurz werden?“ – Ein wirklich guter Einwand. Über Jahrzehnte vermochte ihn niemand zu beantworten.
Exakt diese Frage trieb auch Elizabeth Blackburn um, eine Biologieprofessorin der Universität von Kalifornien. Um dem Rätsel auf die Spur zu kommen, baute sie (kurz vor Weihnachten 1984) zusammen mit der erst 23 Jahre alten Studentin Carol Greider eine Art künstliche Telomere und tauchte sie in einen Extrakt aus zermahlenen Einzellern. Die junge Studentin konnte das Ergebnis kaum erwarten und so schlich sie sich noch am Weihnachtsabend ins Labor. Als sie die Zellbausteine herausnahm, hörte die Welt für einen Augenblick auf, sich zu drehen. Die Telomere waren wie von Geisterhand verlängert.
Des Rätsels Lösung lag in einem besonderen Enzym, das Einzeller in großer Menge besitzen. Es hat die Fähigkeit, die sich bei jeder Zellteilung verkürzenden Telomere wieder zu verlängern. Nur so wird das quasi ewige Leben der Einzeller ermöglicht. Die beiden Forscherinnen tauften das erstaunliche Enzym entsprechend seinen Fähigkeiten auf den Namen Telomerase.
Ein Enzym, das Zellen unendlich am Leben halten kann. Ein Baustein der Unsterblichkeit. Was für ein Fund! Wie immer dauerte es, bis die Tragweite erkannt wurde. Doch 2009 wurde Blackburn und Greider sowie dem Biologen Jack Szostak für diesen Durchbruch der Nobelpreis für Physiologie und Medizin verliehen.
Beneidenswerte Bakterien. Warum besitzt der Mensch das Enzym nicht? Tut er. Auch beim Menschen gibt es unsterbliche Zellen: Krebszellen. Zunächst wurde gemutmaßt, das Fehlen von Telomerase in den normalen Körperzellen sei ein evolutionärer Krebsschutz, doch das ist nicht der Grund. Tumorzellen entstehen nicht aus den fertig entwickelten Körperzellen, sondern in erster Linie aus ihren Vorläufern, den Stammzellen. Und diese verfügen über Telomerase (übrigens ähnlich wie die Zellen der Keimbahn, die unseren ganz individuellen Bauplan enthalten und die wir bei der Fortpflanzung weitergeben. Das ist tatsächlich eine konkrete Form der Unsterblichkeit). [Anmerkung: Heute kennen wir den Grund für die Zurückhaltung des Körpers, alle Zellen mit einem perfekten Reparaturmechanismus auszustatten. Es ist derselbe Grund, der den „behinderten“ Bakterien (wie im ersten Kapitel erwähnt) unter bestimmten Bedingungen einen Vorteil verschafft hat. Erinnern Sie sich? Es ging darum, dass alle Körperprozesse auch einen energetischen Aufwand bedeuten und so verhält es sich auch mit der Verlängerung der Telomere. Mit dem Vorhandensein des Enzyms ist es ja nicht getan. Der Prozess der stetigen Verlängerung bindet Ressourcen. Und so ist die Evolution auch hier einen Kompromiss eingegangen, einen Kompromiss zwischen dem Bestreben, den Körper jung zu erhalten, und dem Aufwand, der dafür erbracht werden muss. Die Natur könnte uns also auch über diesen Mechanismus (noch) langsamer altern lassen. Doch das wäre sehr aufwendig. Wenn wir als Individuum mehr wollen, müssen wir uns mit eigenem Aufwand selbst darum kümmern.]
Doch es sollte noch besser kommen. Weiterentwickelte Messmethoden fanden das Enzym nämlich auch in den übrigen Körperzellen, nur in weitaus geringerer Konzentration. Dennoch verrichtet es dort dieselbe Aufgabe – bloß mit entsprechend geringerem Erfolg. Und wie die weitere Forschung ergab, bleiben unsere Zellen so lange am Leben, bis der eher schwache Reparaturmechanismus den „Abnutzungsvorgängen“ nicht mehr trotzen kann. Je mehr Zellen in einem Organ irgendwann zu viele kurze Telomere haben, desto schneller altern das Organ und schließlich der ganze Organismus.
Je mehr verkürzte Telomere, desto höher ist auch das Risiko für Funktionsstörungen. Und die äußern sich dann in dem, was wir als Alterskrankheiten bezeichnen. Der Zusammenhang zwischen Krankheit und Telomerlänge wurde inzwischen für Diabetes, Herz-Kreislauf-Krankheiten, Lungenfibrose, psychische Störungen und andere Alterserscheinungen bis hin zur Gesamtsterblichkeit bestätigt. Welche Organe übrigens wie schnell altern, das hängt von der individuellen Genetik sowie von externen Faktoren ab. Und inzwischen kennen wir viele der Ursachen, die die Arbeit der wenigen Telomerase zur Sisyphusarbeit werden lassen und damit Zelltod und Störungen beschleunigen: Radikale, Fettleibigkeit, Rauchen (wobei Teer und Gase den Negativeffekt bewirken, nicht das Nikotin), nährstoffarme Ernährung, Bewegungsmangel, Stress, Vitamin-D-Mangel und noch so einiges mehr.
Doch wir brauchen uns nicht nur auf Vermeidung und Verzicht zu konzentrieren. Seitdem Telomere sehr genau vermessen werden können, hat die Forschung auch Faktoren identifiziert, mit Hilfe derer sich die Arbeit der Telomerase effektiv unterstützen lässt.
Unterstützung für Telomere
Für die folgenden Wirkstoffe wurde eine Schutzwirkung auf die Telomerlänge und damit auf die Funktionsfähigkeit und die Lebensdauer der Zellen nachgewiesen (im Tierversuch oder beim Menschen). Die Mengenangaben beziehen sich auf die Dosierung, die diesen Effekt garantiert. Teilweise sind es Dosierungen, die sich über die Ernährung erreichen lassen, teilweise ist dazu eine gezielte Nahrungsergänzung notwendig.
Читать дальше













