64 Gd 1Gadolinium 2157,25 7
65 TbTerbium 2158,9254 9
66 DyDysprosium 2162,50 10
67 HoHolmium 2164,9304
68 ErErbium 2167,26
69 TmThulium 2168,9342 13
70 YbYtterbium 2173,04 14
71 Lu 1Lutatium 2174,967 14
**) Actinoide
6 d7 s5 f
90 ThTho- 2
rium 2232,0381
91 PaProtacti- 1
nium 2231,03 2
92 UUran 1
2238,02 3
93 Np
Neptu- 1
nium 2
237,0482
94 PU
Plutonium 1
2
(244) 5
95 Am
Ameri- 1
cium 2
(243) 6
96 Cm
Curium 1
2
(247) 7
97Bk
Berke- 1
lium 2
(247) 8
98 Cf
Califor- 1
nium 2
(251) 9
99 Es
Einstein 1
ium 2
(252) 9
100 Fm
Fer 1
mium 2
(257) 11
101 Md
Mende- 1
levium 2
(258) 12
102 No
Nobelium 1
2
(259) 13
103 Lr
Lawren- 1
cium 2
(269) 14
Die in den einzelnen Gruppen unter dem Buchstaben a senkrecht stehenden Elemente sind die Hauptgruppenelemente
Die in den einzelnen Gruppen unter dem Buchstaben b senkrecht stehenden Elemente sind die Nebengruppenelemente
Die in Klammern angegebenen Massenzahlen gehören zu dem jeweiligen Isotop mit der größten Halbwertszeit


15
Aufbau des PSE
Im Periodensystem unterscheiden wir Pe-rioden (= waagrechte Reihen) und Grup-pen (= senkrechte Spalten). Es gibt im PSE 7 Perioden und 16 Gruppen (8 Hauptgrup-pen und 8 Nebengruppen).
Den Hauptgruppen werden Namen zu-geordnet:
1. Hauptgruppe: Alkalimetalle
2. Hauptgruppe: Erdalkalimetalle
3. Hauptgruppe: Erdmetalle oder Bor-gruppe
4. Hauptgruppe: Kohlenstoffgruppe
5. Hauptgruppe: Stickstoffgruppe
6. Hauptgruppe: Chalkogene oder Erz-bildner
7. Hauptgruppe: Halogene oder Salzbild-ner
8. Hauptgruppe: Edelgase
Die Haupt- und Nebengruppen werden oft mit römischen Ziffern bezeichnet (I bis VIII).
Die Elemente der gleichen Haupt-gruppe haben gleiche oder ähnliche Eigenschaften.
Die Nummer der Hauptgruppe gibt die Anzahl der Elektronen auf der äußers-ten Schale an.
Die Nummer der Periode gibt die An-zahl der Elektronenschalen an.
Beispiele:
a) Fluor (2. Periode, 7. Hauptgruppe) hat 2 Elektronenschalen; auf der 2. Schale (äußerste Schale) sind 7 Elektronen.
b) Kalium (4. Periode, 1. Hauptgruppe) hat 4 Elektronenschalen; auf der 4. Schale (äußerste Schale) ist 1 Elektron.
Ausnahme: Helium (1. Periode, 8. Haupt-gruppe) hat auf seiner einzigen und deshalb äußersten Elektronenschale keine 8, son-dern nur 2 Elektronen.
Die Gründe, warum das Helium trotzdem zur 8.Hauptgruppe zählt, sind:
Die 1. Schale ist bereits mit 2 Elektronen abgesättigt. Die Atome der Elemente der 8. Hauptgruppe haben alle eine abgesät-tigte Außenschale, d.h. die äußerste Scha-le ist mit 8 Elektronen voll besetzt. Helium zeigt „Edelgaseigenschaften“ z.B. äußerste Reaktionsträgheit.
Nebengruppen
Es gibt 8 Nebengruppen.
Die 8. Nebengruppe enthält in jeder Periode 3 Elemente, alle andern Nebengruppen ent-halten in jeder Periode 1 Element.
Alle Nebengruppenelemente sind Metalle. Die Zahl der Außenelektronen ist bei den Nebengruppenelementen gering (meist 2 Elektronen) und nicht (wie bei den Haupt-gruppen) an der Nebengruppennummer zu erkennen.
Besonderheit bei der Elektronenschalen-besetzung: Die äußerste Schale wird erst mit wenigen Elektronen (meist 2) angefüllt, bevor die darunter liegende, innere Schale aufgefüllt wird. Man spricht auch von der inneren Schalenbesetzung. Bei den Ato-men der Hauptgruppenelemente werden dagegen ausschließlich die äußersten Scha-len aufgefüllt.
Beispiel:
Zink (Zn) Die 4. Schale (Außenschale) wird mit 2 Elektronen angefüllt, bevor die darunter liegende, innere Schale um 10 Elektronen auf 18 Elektronen (max. Elek-tronenzahl der 3. Schale) aufgefüllt wird.

Periodensystem

16

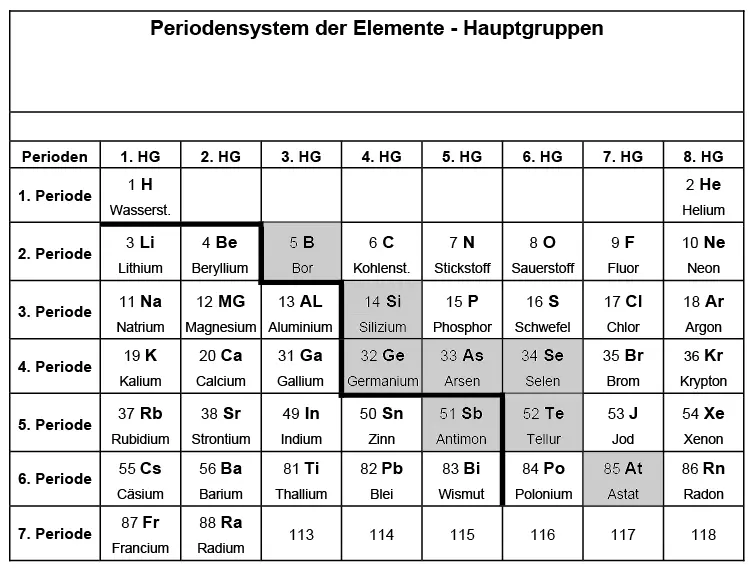
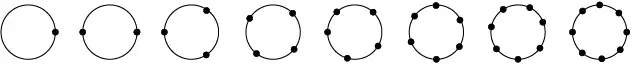
Gesetzmäßigkeiten im PSE
Das kleine Periodensystem der Elemente. Es sind nur die Hauptgruppen aufge-führt. Die Elemente links unten der Diagonale sind Metalle, die Elemente rechts oben der Diagonale sind Nichtmetalle. Die Elemente ganz rechts (8. HG) sind Edelgase. Die Elemente in den grauen Feldern sind Halbmetalle. Es sind nur die Hauptgruppen aufgeführt
Atomradien
Innerhalb einer Hauptgruppe nimmt der Atomradius von oben nach unten zu!
Begründung:
Die Anzahl der Schalen nimmt von oben nach unten zu. Die Abstände der Außen-elektronen vom Atomkern werden größer, so dass die Kernanziehungskraft auf die Außenelektronen (von oben nach unten) sinkt. Die Atome der unten stehenden Ele-mente geben sehr bereitwillig ihre Außen-elektronen ab. ⇒ Die Reaktionsfreudigkeit der Elemente steigt von oben nach unten.
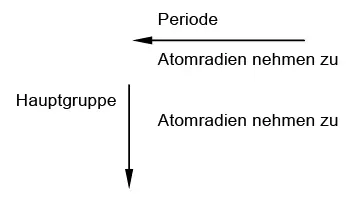
Verlauf der Atomradien im PSE bei den Hauptgruppenelementen

Periodensystem


17
Innerhalb einer Periode nimmt der Atomradius von rechts nach links zu.
Begründung:
Die Schalenanzahl ist zwar gleich, die Pro-
tonenzahl nimmt aber von rechts nach links ab. Daher wird die Anziehungskraft der Atomkerne auf die Elektronenhülle immer schwächer.
Metall-/Nichtmetallcharakter
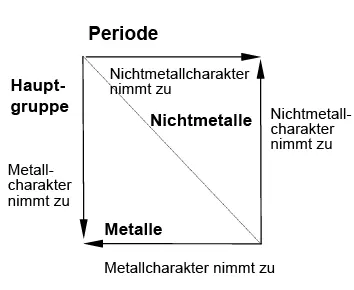
Metalle und Nichtmetalle im PSE der Hauptgruppenelemente
Wenn man durch das PSE eine Diagonale von links oben nach rechts unten zieht, so stellt man fest, dass die Elemente links un-ten von dieser Diagonale Metalleigenschaf-ten haben und zwar umso mehr
- je weiter unten sie stehen,
- je weiter links sie stehen.
Die Elemente, die im PSE eher rechts oben stehen, haben diese Metalleigenschaften nicht. Man nennt sie daher auch Nicht-metalle. Die Elemente auf oder in unmit-telbarer Nähe der Diagonale haben einige metallische und einige nichtmetallische Eigenschaften. Man nennt sie daher auch Halbmetalle (B, Si, Ge, As, Se, Sb, Te, At).
Читать дальше




















