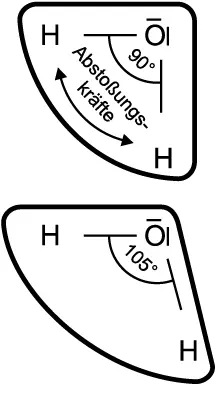
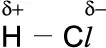Beim Wassermolekül liegt noch eine wei-tere Besonderheit vor: Die beiden (partiell positiv geladenen) H-Atome stoßen sich gegenseitig ab. Dadurch vergrößert sich der Winkel zwischen ihnen von 90° auf 105°. Eine weitere Molekülspreizung verhindern die beiden freien ungepaarten Elektronen-paare des Sauerstoff-Atoms.
Entstehung des Winkels von 105° im Wassermolekül
Wiederholungsfragen
1. Erklären Sie die Entstehung der kova-lenten Atombindung am Beispiel F2!
2. Was ist der Grund dafür, dass unedle Gase immer molekular vorliegen?
3. Schreiben Sie die chemische Formel des Ammoniaks (NH3) in den vier Formel-schreibweisen!
4. Erklären Sie die Entstehung eines Dipols am Beispiel des Wassermoleküls!
5. Welches Molekül ist stärker polarisiert: H2O oder H2S?
(Siehe Tabelle 2.1 Elektronegativitäten von Hauptgruppenelementen)
Das Molekül hat einen positiven und einen negativen Pol. Man nennt es deshalb ein Di-pol-Molekül, weil räumlich 2 verschiedene Ladungsschwerpunkte vorhanden sind.
z.B.
Je größer die Differenz zwischen den Elek-tronegativitäten (∆EN) der an der Atombin-dung beteiligten Atome ist, desto stärker ist der Dipolcharakter des Moleküls oder man sagt auch: desto stärker ist die Atombindung polarisiert.
z.B. H-F: F: EN = 4,0
H: EN = 2,1
∆EN = 1,9
Man ermittelt die Elektronegativitätsdiffe-renz (∆EN), indem der kleinere EN-Wert vom größeren EN-Wert subtrahiert wird. (siehe Tabelle 2.1)
z.B. H-Br Br: EN: = 2,8
H : EN: = 2,1
∆EN: = 0.7
Das HF-Molekül ist also stärker polarisiert als das HBr-Molekül, da es eine höhere Elektronegativitätsdifferenz (∆EN) auf-weist.
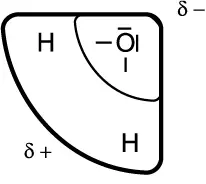
Auch das Wassermolekül stellt einen Dipol dar:
Wasser als Dipol: Die Elektronen befinden sich mehr im oberen Teil des Mo-leküls als im unteren.
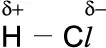

Chemische Bindungen


23
Ionenbindung
Entstehung
Diese Bindung kommt durch Reaktion von Metallatomen mit Nichtmetallatomen zustande. Metallatome haben nur wenige Außenelektronen, Nichtmetalle dagegen viele. Gleichzeitig herrscht zwischen Metallen und Nichtmetallen eine große Elektronegativitätsdifferenz (∆EN > 1,7).
Beispiel:
Natrium: 1 Außenelektron EN = 0,9
Chlor: 7 Außenelektronen EN = 3,0
∆ EN = 2,1
Bei der Reaktion von Metallatomen mit Nichtmetallatomen ziehen die Nichtmetall-Atome (hohe EN) die Bindungselektronen ganz auf ihre Seite. Man sagt auch:
Die Metallatome (geringe EN) geben an die Nichtmetallatome (hohe EN) Außenelektro-nen ab. Die Metallatome werden dadurch zu positiv geladenen Ionen, die Nichtmetalla-tome zu negativ geladenen Ionen.
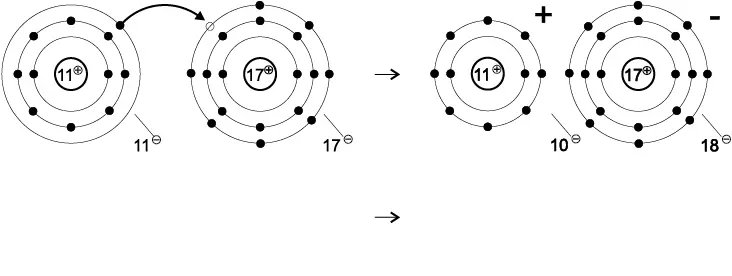
Entstehung der Ionenbindung zwischen Natrium und Chlor: Das Natriumatom gibt ein Elektron an das Chloratom ab.

Das Chloratom hat sieben Außenelektronen; es muss ein Außenelektron vom Natrium-atom erhalten, um die Edelgaskonfiguration zu erreichen. Es hat dann 17 Protonen und insgesamt 18 Elektronen und ist somit ne-gativ geladen.
Das Natriumatom hat ein Außenelektron; es gibt dieses an das Chloratom ab, um eine vollbesetzte Außenschale zu erreichen. Es hat nun elf Protonen und insgesamt zehn Elektronen und ist somit positiv geladen. Die entstandenen elektrisch geladenen Teilchen (Na+, Cl-) nennt man Ionen. Positiv geladene Teilchen heißen Kationen negative geladene Teilchen Anionen.
Die Ionenladungszahl wird durch hochge-stellte + oder - rechts oben am Elementsym-bol ersichtlich: z.B.
Na+ bedeutet: 1 Elektron weniger
(11 Protonen, 10 Elektronen)
Cl- bedeutet: 1 Elektron mehr
(17 Protonen, 18 Elektronen)
Mg2+ bedeutet: 2 Elektronen weniger
(12 Protonen, 10 Elektronen)
S2- bedeutet: 2 Elektronen mehr
(16 Protonen, 18 Elektronen)
Al3+ bedeutet: 3 Elektronen weniger
(13 Protonen, 10 Elektronen)
P3- bedeutet: 3 Elektronen mehr
(15 Protonen, 18 Elektronen)
Chemische Bindungen
Natriumatom Chloratom Natrium-Ion Chlorid-Ion
(positiv geladen) (negativ geladen)
Na + Cl Na+ + Cl-
1. Beispiel: Reaktion zwischen Natrium und Chlor

24

Formelschreibweisen für Ionenbindungen am Beispiel von Natriumchlorid:
a) Na+ Cl -
(ohne Verbindungsstrich, denn es existiert kein gemeinsames Elektrodenpaar)
b) Na+Cl-
c) Na Cl
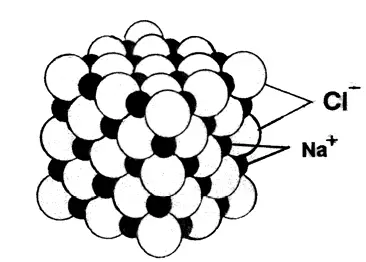
Aus der Elektrostatik ist bekannt, dass sich elektrisch entgegengesetzt geladene Teil-chen anziehen. Das positiv geladene Metal-lion übt demzufolge eine Anziehungskraft auf alle negativ geladenen Nichtmetallionen in seiner Umgebung aus und umgekehrt.
Dies hat zur Folge, dass sich die Ionen zu ei-nem Gitter anordnen, bei dem sich positive und negative Ionen direkt gegenüber liegen. Je nach Größe der negativ und positiv gela-denen Ionen kann das Gitter verschiedene Formen haben. (Es entsteht immer dasje-nige Gitter, das die größte Packungsdichte ermöglicht). In Abb. 3.5 wird das Gitter des Natriumchlorids gezeigt. In diesem Gitter sind jedem Natrium-Ion 6 Chlorid-Ionen benachbart und jedem Chlorid-Ion 6 Natrium-Ionen.
Die positiven oder negativen Ionen oder beide können auch aus verschiedenen Ato-men bestehen, die durch Atombindungen aneinander gebunden sind. Es entsteht dann ein Gitter aus diesen beiden Einheiten. Bei Ionen, die aus mehreren Atomen bestehen, z.B. SO42-, gilt die Ionenladungszahl für das gesamte Ion (und nicht für einzelne Atome des Ions).
Ionengitter des Calciumsulfats. Das Sulfat-Ion besteht aus mehreren Ato-men, die durch Atombindung aneinander gebunden sind.
Читать дальше