



Das Natrium-Ion zieht alle Chlorid-Ionen in seiner Umgebung an.
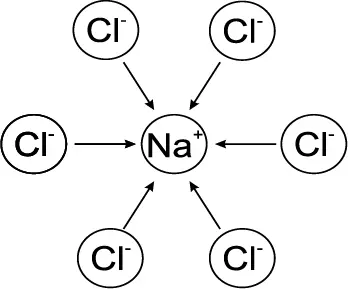

Ionengitter des Natriumchlorids


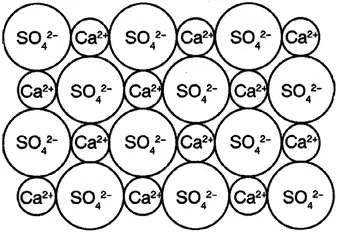
Chemische Bindungen
Cl-
Na+


25
Anwendung
Die Ionenbindung ist die typische Bin-dungsart bei Salzen oder salzartigen Stoffen. Die Ionenbindung bewirkt ihre typischen Eigenschaften:
a) Es sind Stoffe mit hohem Schmelzpunkt (z.B. NaCl 801°C) und hohem Siede-punkt (z.B. NaCl 1461°C).
b) Sie sind hart und spröde.
c) Als Schmelze oder als Lösung leiten sie den elektrischen Strom.
d) Es sind Feststoffe, die das Licht an den glatten Flächen der Kristalle reflektieren (sie glitzern).
Wiederholungsfragen
1. Welcher grundsätzliche Unterschied besteht zwischen Atombindung und Ionenbindung?
2. Was ist der Unterschied zwischen einem Dipol und einem Ion?
3. Welche der folgenden Ionen sind Kat-ionen, welche Anionen?
Na+ Cl- SO42- Ca2+ Al3+ OCl-?
4. Was ist der Unterschied zwischenhoch-gestellter Zahl z.B. in Mg2+ und tief gestellter Zahl Cl2?
5. Welche Eigenschaften haben Verbindun-gen mit Ionenbindungscharakter?
Hydratation, Dissoziation und Elektrolyse
Hydratation
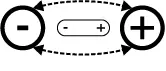
Im festen Zustand sind die Ionen des tro-ckenen Salzes fest im Gitter eingebaut. Sie können also nicht zur elektrischen Leitfä-higkeit beitragen. Im trockenen Zustand bestehen zwischen An- und Kationen so starke Kräfte (starker Pfeil), dass die Ionen an ihrem Platz gebunden sind, damit sind sie nicht frei beweglich.
Anziehungskräfte zwischen den Ionen eines trockenen Salzes
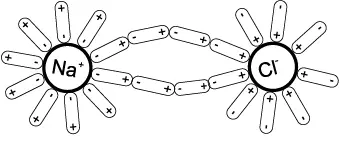
Gibt man Wasser hinzu, dann lagern sich polarisierte Wassermoleküle ( stark vereinfachte Darstellung des Wassers als Dipolmolekül) zwischen die Anionen und Kationen. Der positive Teil des Wassermo-leküls zeigt zum Anion der negative Teil zum Kation. Dadurch werden die Kräfte zwischen den Ionen herabgesetzt (gestri-chelter Pfeil).

Anziehungskräfte zwischen den Ionen eines feuchten Salzes
Dissoziation
Die Anziehungskräfte zwischen den Io-nen können so gering sein, dass sich die einzelnen Ionen vom Gitterverband lösen können. Bei ausreichender Wassermenge können sich positive und negative Ionen in der Lösung frei bewegen. Sie sind dabei von einer Hydrathülle (Wasserhülle) umgeben.




Das polarisierte Wassermolekül spaltet Ionenbindungen auf. Diesen Vorgang nennt man Dissoziation.
Chemische Bindungen

26

Je mehr Ionenbindungen getrennt werden, umso größer ist die Anzahl frei beweglicher Ionen, desto besser leitet die Lösung den elektrischen Strom.
Unter Dissoziation versteht man den Zerfall eines Stoffes (z.B. Salzes) in frei bewegliche Ionen.
In der Chemie wird die Dissoziation in Form von Gleichungen ausgedrückt. In der Mitte jeder Dissoziationsgleichung steht der Dissoziationspfeil (Doppelpfeil):
Bedeutung des Dissoziationspfeils:
1. Er ist das Symbol für eine Dissozi-ation.
2. In der Lösung liegen sowohl Ionen-Aggregate = undissoziierte Form (links vom Pfeil) als auch frei be-wegliche Ionen (rechts vom Pfeil) vor.
3. Die Summe der Ladungen ist auf beiden Seiten des Pfeils Null.
4. Er entspricht wie der Reaktionspfeil einem mathematischen Gleichheits-zeichen.
Aufstellung von Dissoziationsgleichun-gen
Vorgehensweise: Wir zerlegen die Io-nenverbindung gedanklich in Metall und Nichtmetall. Anschließend wird mit Hilfe des PSE die Ionenladungszahl bestimmt.
Beispiele:
1.) NaCl Na+ + Cl-
Lies: „Natriumchlorid (Kochsalz) disso-ziiert in die frei beweglichen Ionen Na+ und Cl-“.
Anmerkung: In den meisten Fällen ist das Lösungs-mittel Wasser. Falls ein anderes Lösungsmittel ver-wendet wird, gibt man das Lösungsmittel über dem Dissoziationspfeil an.

2) CaF2 Ca2+ + 2 F-
Calciumfluorid
3) Mg3P2 3 Mg2+ + 2 P3-
Magnesiumphosphid
4) K2SO4 2 K+ + SO42-
Kaliumsulfat
(Bei SO42- liegt ein zusammengestztes Ion vor!)
5) NaOCl Na+ + OCl-
Natriumhypochlorit
(Bei OCl- liegt ein zusammengesetztes Ion vor!)
Wiederholungsfragen
1. Unterscheiden Sie den Vorgang der Hydratation und der Dissoziation!
2. Welche Bedeutung hat der Dissoziati-onspfeil?
3. Stellen Sie die Dissoziationsgleichung auf für
a) Magnesiumchlorid
b) Aluminiumfluorid
c) Borsulfid (B2S3)!






Chemische Bindungen
Читать дальше




























