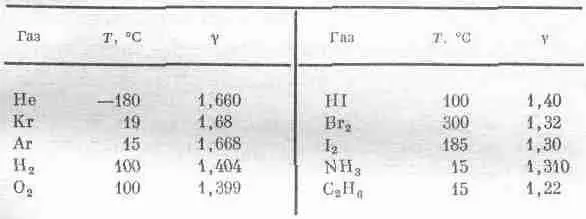
Таблица 40.1 · ИЗМЕРЕННЫЕ ЗНАЧЕНИЯ g ДЛЯ РАЗЛИЧНЫХ ГАЗОВ
Перейдем к двухатомным газам. Тут же обнаружится, что значение g для водорода, равное 1,404, не согласуется с теоретическим значением 1,286. Очень близкое значение дает и кислород, 1,399, но с теоретическим это снова не согласуется. Для йодистого водорода g равно просто 1,40. Начинает казаться, что мы нашли общий закон: для двухатомных молекул g равно 1,40. Но нет, поглядите дальше. Для брома мы получаем 1,32, а для иода 1,30. Поскольку 1,30 довольно близко к 1,286, то можно считать, что экспериментальное значение g для иода согласуется с теоретическим, а кислород представляет собой исключение. Это уже неприятно. То, что верно для одной молекулы, неверно для другой, и нам, по-видимому, надо проявить хитроумие, чтобы объяснить это.
Давайте рассмотрим еще более сложные молекулы, состоящие из большого числа частей, например С 2Н 6— этан. Молекула атома состоит из восьми разных атомов, и все они качаются и вращаются в самых разных комбинациях, так что полная величина внутренней энергии должна складываться из огромного числа kT , по крайней мере 12 kT только для одной кинетической энергии, поэтому g-1 должно быть очень близко к нулю, a g почти в точности равно единице. И действительно, значение g для этана меньше, чем в предыдущих случаях, но 1,22— не так
уж мало, во всяком случае, больше l 1/ 12, чему должно быть
равно g, если учесть только кинетическую энергию. Этого вообще нельзя понять!
Ну а дальше совсем плохо, ибо двухатомную молекулу нельзя рассматривать как абсолютно жесткую, даже в пределе. Даже если связь между атомами так сильна, что они не могут и пошевелиться, все равно нужно считать, что они колеблются. Колебательная энергия всегда равна kT , поскольку она не зависит от силы связи. Но если представить себе двухатомную молекулу абсолютно жесткой, остановить колебания и выбросить эту степень свободы, то мы получим U = 5/ 2 kT и g=1,40 для двухатомных газов. Казалось бы, это подходит и для Н 2, и для O 2. Но вопрос по-прежнему остается открытым, потому что g и для кислорода, и для водорода зависит от температуры! На фиг. 40.6 показаны результаты нескольких измерений. Для Н 2значение g изменяется от 1,6 при
-185°С до 1,3 при 2000°С. В случае водорода изменения g еще больше, но и в случае кислорода g явно стремится возрасти при падении температуры.
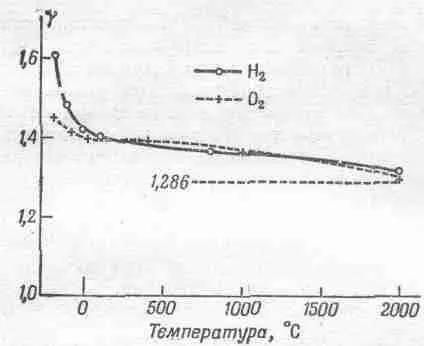
Фиг. 40.6. Экспериментальные значения g как функция температуры для водорода и кислорода.
Классическая теория предсказывает не зависящее от температуры значение g =1,28 6 .
§ 6 . Поражение классической физики
Итак, приходится сказать, что мы натолкнулись на трудности. Можно соединить атомы не пружинкой, а чем-нибудь другим, но оказывается, что это только увеличит значение g. Если пустить в ход другие виды энергии, то вопреки фактам g очень приблизится к единице. Все известное нам из классической теоретической физики только ухудшает положение. Нам известно, например, что каждый атом содержит электроны, и атомные спектры обязаны своим существованием внутренним движениям электронов; каждый электрон должен иметь по крайней мере l / 2 kT кинетической энергии и еще кое-что из потенциальной, а когда все это складывается, то g становится еще меньше. Просто смешно. И явно что-то не так.
Первая замечательная работа по динамической теории газов была сделана Максвеллом в 1859 г. Исходя из идей, с которыми мы только что познакомились, он сумел точно объяснить очень много известных явлений, таких, как закон Бойля, теорию диффузии, вязкость газов и другие вещи, о которых мы еще будем говорить в следующей главе. Подводя итог всем этим великим достижениям, он писал: «Наконец, установив необходимое соотношение между поступательным и вращательным движением несферических частиц (он имел в виду теорему о l / 2 kT ), мы доказали, что в системе из таких частиц не может выполняться известное соотношение между двумя теплоемкостями». Он говорит здесь о g (позднее мы увидим, что эта величина связана с двумя разными способами измерения удельной теплоемкости) и замечает, что никто не в состоянии дать верного ответа.
Читать дальше














