20 Kapitel 19Abb. 19.1 Schema der ebenen Oberfläche eines Kristalls. Dieses primitive Modell ...Abb. 19.2 Stufen und Ecken sind zwei der Arten von Fehlstellen, die auf ansonste...Abb. 19.3 Die am langsamsten wachsenden Seiten eines Kristalls bestimmen am Ende...Abb. 19.4 Selbstorganisierte Monolagen aus Alkylthiolen auf einer Goldoberfläche...Abb. 19.5 Die Rastertunnelmikroskopie (STM) beruht auf dem Tunnelstrom (Elektron...Abb. 19.6 Eine STM‐Aufnahme von „Bahnen“ aus Kupferatomen auf einer metallischen...Abb. 19.7 In der Rasterkraftmikroskopie (AFM) wird ein Laserstrahl eingesetzt, u...Abb. 19.8 Das XP‐Spektrum von Gold, an dessen Oberfläche eine Lage Quecksilber a...Abb. 19.9 Wenn ein Elektron aus einem Festkörper herausgeschlagen wird, kann (a)...Abb. 19.10 Schematische Darstellung einer LEED‐Apparatur. Die an den Oberflächen...Abb. 19.11 LEED‐Aufnahmen (a) einer sauberen FeS 2‐Oberfläche und (b) derselben O...Abb. 19.12 Die Struktur der (110)‐Oberfläche von Rhodium bei 300 K in der Nähe e...Abb. 19.13 Aus LEED‐Mustern lässt sich die Fehlstellendichte einer Oberfläche be...Abb. 19.14 Die schematische Anordnung eines Experiments zur Beobachtung der Ober...Abb. 19.15 Auftragung der Daten aus Beispiel 19.2. Wie gut zu sehen ist, sagt di...Abb. 19.16 Die Langmuir‐Isotherme für nicht‐dissoziative Adsorption für untersch...Abb. 19.17 Die Langmuir‐Isotherme für dissoziative Adsorption, A 2(g)  A(Oberf...Abb. 19.18 Die isostere Adsorptionsenthalpie kann aus der Steigung der Gerade be...Abb. 19.19 Die BET‐Isotherme für verschiedene Werte von c . Das Verhältnis
A(Oberf...Abb. 19.18 Die isostere Adsorptionsenthalpie kann aus der Steigung der Gerade be...Abb. 19.19 Die BET‐Isotherme für verschiedene Werte von c . Das Verhältnis 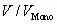 ste...Abb. 19.20 Man kann die BET‐Isotherme überprüfen und ihre Parameter bestimmen, i...Abb. 19.21 Der Verlauf der potenziellen Energie bei der dissoziativen Chemisorpt...Abb. 19.22 Die Adsorptionswahrscheinlichkeit von N 2an verschiedenen Flächen ein...Abb. 19.23 Das Desorptionsspektrum (TPD) von Wasserstoffgas, das sich von einer ...Abb. 19.24 Die Reaktionsprofile für katalysierte und unkatalysierte Reaktionen. ...Abb. 19.25 Die „Vulkankurve“ der katalytischen Aktivität entsteht, da die Reakta...Abb. A1 Eine schematische Darstellung der Anordnung der Si‐, Al‐ und O‐Atome in ...Abb. 19.26 Ein einfaches Modell für die Grenzfläche Elektrode‐Lösung. Die Grenzf...Abb. 19.27 Das Gouy‐Chapman‐Modell der elektrischen Doppelschicht beschreibt die...Abb. 19.28 Das Stern‐Modell der Grenzfläche zwischen Elektrode und Lösung. Es ko...Abb. 19.29 Die Gesamtstromdichte ist als Differenz der kathodischen und der anod...Abb. 19.30 Profile für die Variation der Freien Enthalpie zwischen den oxidierte...Abb. 19.31 Die Abhängigkeit der Stromdichte von der Überspannung für verschieden...Abb. 19.32 Die Abhängigkeit der anodischen (rot) bzw. kathodischen (blau) Stromd...Abb. 19.33 Mithilfe einer Tafel‐Auftragung lässt sich die Austauschstromdichte (...Abb. 19.34 Die Änderung der Potenzialdifferenz mit der Zeit (a) und die resultie...Abb. 19.35 (a) Die zeitabhängige Änderung der Potenzialdifferenz, die bei der Au...Abb. 19.36 Die zyklischen Voltammogramme zu Beispiel 19.6 für (a) eine geringe u...Abb. 19.37 Das zyklische Voltammogramm zu Selbsttest 19.6.Abb. A1 Eine einzelne Zelle einer Wasserstoff/Sauerstoff‐Brennstoffzelle. In de...Abb. 19.38 Die zweidimensionalen Gitter, die in Aufgabe S19.1.1 besprochen werde...Abb. 19.39 Das Voltammogramm zu Aufgabe S19.4.8.
ste...Abb. 19.20 Man kann die BET‐Isotherme überprüfen und ihre Parameter bestimmen, i...Abb. 19.21 Der Verlauf der potenziellen Energie bei der dissoziativen Chemisorpt...Abb. 19.22 Die Adsorptionswahrscheinlichkeit von N 2an verschiedenen Flächen ein...Abb. 19.23 Das Desorptionsspektrum (TPD) von Wasserstoffgas, das sich von einer ...Abb. 19.24 Die Reaktionsprofile für katalysierte und unkatalysierte Reaktionen. ...Abb. 19.25 Die „Vulkankurve“ der katalytischen Aktivität entsteht, da die Reakta...Abb. A1 Eine schematische Darstellung der Anordnung der Si‐, Al‐ und O‐Atome in ...Abb. 19.26 Ein einfaches Modell für die Grenzfläche Elektrode‐Lösung. Die Grenzf...Abb. 19.27 Das Gouy‐Chapman‐Modell der elektrischen Doppelschicht beschreibt die...Abb. 19.28 Das Stern‐Modell der Grenzfläche zwischen Elektrode und Lösung. Es ko...Abb. 19.29 Die Gesamtstromdichte ist als Differenz der kathodischen und der anod...Abb. 19.30 Profile für die Variation der Freien Enthalpie zwischen den oxidierte...Abb. 19.31 Die Abhängigkeit der Stromdichte von der Überspannung für verschieden...Abb. 19.32 Die Abhängigkeit der anodischen (rot) bzw. kathodischen (blau) Stromd...Abb. 19.33 Mithilfe einer Tafel‐Auftragung lässt sich die Austauschstromdichte (...Abb. 19.34 Die Änderung der Potenzialdifferenz mit der Zeit (a) und die resultie...Abb. 19.35 (a) Die zeitabhängige Änderung der Potenzialdifferenz, die bei der Au...Abb. 19.36 Die zyklischen Voltammogramme zu Beispiel 19.6 für (a) eine geringe u...Abb. 19.37 Das zyklische Voltammogramm zu Selbsttest 19.6.Abb. A1 Eine einzelne Zelle einer Wasserstoff/Sauerstoff‐Brennstoffzelle. In de...Abb. 19.38 Die zweidimensionalen Gitter, die in Aufgabe S19.1.1 besprochen werde...Abb. 19.39 Das Voltammogramm zu Aufgabe S19.4.8.
1 Kapitel 1 Tab. 1.1 Druckeinheiten. *) Tab. A1 Zusammensetzung der Erdatmosphäre. Tab. 1.2 Die (molare) Gaskonstante in verschiedenen Einheiten *). Tab. 1.3 Stoßquerschnitte. *) Tab. 1.4 Zweite Virialkoeffizienten, B /(cm 3mol −1). *) Tab. 1.5 Kritische Größen von Gasen. *) Tab. 1.6 Van-der-Waals-Koeffizienten. *) Tab. 1.7 Ausgewählte Zustandsgleichungen.
2 Kapitel 2 Tab. 2.1 Arten von Arbeit. *) Tab. 2.2. Temperaturabhängigkeit der molaren Wärmekapazität, C p,m/(J K –1mol –1) ... Tab. 2.3 Standardschmelz- und -verdampfungsenthalpien bei der jeweiligen Übergan... Tab. 2.4 Übergangsenthalpien. Tab. 2.5 Standardbildungs- und -verbrennungsenthalpien organischer Verbindungen ... Tab. 2.6 Standardbildungsenthalpien anorganischer Verbindungen bei 298 K. *) Tab. 2.7 Standardbildungsenthalpien organischer Verbindungen bei 298 K. *) Tab. A1 Thermochemische Daten einiger Brennstoffe. Tab. 2.8 Koeffizienten der thermischen Ausdehnung ( α ) und der isothermen Kompres... Tab. 2.9 Inversionstemperaturen ( T I), Schmelz- ( T Sm) und Siedepunkte ( T S) und Jo...
3 Kapitel 3 Tab 3.1 Standardentropien von Phasenübergängen bei der jeweiligen Übergangstempe... Tab 3.2 Standardverdampfungsenthalpien und ‐entropien verschiedener Flüssigkeite... Tab 3.3 Standardentropien bei 298 K nach dem Dritten Hauptsatz. *) Tab 3.4 Freie Standardbildungsenthalpien bei 298 K. *) Tab 3.5 Die Maxwell‐Beziehungen.
4 Kapitel 5 Tab. 5.1 Henry-Konstanten für Gase in Wasser bei 298 K. *) Tab. 5.2 Kryoskopische und ebullioskopische Konstanten. *)Tab. 5.3 Ionenstärke und Molalität, I = kb / b ⊖.Tab. 5.4 Mittlere Aktivitätskoeffizienten in Wasser bei 298 K. *)Tab. 5.5 Aktivitäten und Standardzustände. *)
5 Kapitel 6Tab. 6.1. Elektrodenarten.Tab. 6.2. Standardpotenziale bei 298 K. *)Tab. 6.3. Elektrochemische Spannungsreihe der Metalle. *)
6 Kapitel 7Tab 7.1 Die Hermite‐Polynome.Tab 7.2 Die Kugelflächenfunktionen.
7 Kapitel 8Tab. 8.1 Radiale Wellenfunktionen wasserstoffähnlicher Atome.Tab. 8.2 Effektive Kernladung. *)Tab. 8.3 Atomradien der Hauptgruppenelemente, r /pm.Tab. 8.4 Ionenradien *), r /pm. **)Tab. 8.5 Erste und zweite Ionisierungsenergien. *)Tab. 8.6 Elektronenaffinitäten, E Ea/(kJ mol −1). *)
8 Kapitel 9Tab. 9.1 Einige häufige Hybridisierungen.Tab. 9.2 Überlappungsintegrale zwischen Orbitalen wasserstoffähnlicher Atome.Tab. 9.3 Bindungslängen.*)Tab. 9.4 Bindungsdissoziationsenergien.*)Tab. 9.5 Pauling‐Elektronegativitäten.*)Tab. A.1. Ab ‐ initio ‐Berechnungen und spektroskopische Daten einiger linearer Pol...
9 Kapitel 10Tab. 10.1 Die Bezeichnung der Punktgruppen.*Tab. 10.2 Die Charaktertafel der Gruppe C 2v.*)Tab. 10.3 Die Charaktertafel der Gruppe C 3v.*)Tab. 10.4 Die Charaktertafel der Gruppe C 4.*)
10 Kapitel 11Tab. 11.1 Trägheitsmomente.*)Tab. 11.2 Eigenschaften zweiatomiger Moleküle.*)Tab. 11.3 Farbe, Frequenz und Energie von Licht.* )Tab. 11.4 Charakteristische Absorptionen einiger Gruppen und Moleküle. *)*Tab. 11.5 Eigenschaften von Laserstrahlung und ihre chemischen Anwendungen.
11 Kapitel 12Tab. 12.1 Kernaufbau und Kernspinquantenzahlen.*)Tab. 12.2 Eigenschaften von Kernen.*)Tab. 12.3 Hyperfeinkopplungskonstanten von Atomen, a /mT.*)
12 Kapitel 13Tab. 13.1 Rotationstemperaturen zweiatomiger Moleküle.*)Tab. 13.2 Symmetriezahlen ausgewählter Moleküle.*)Tab. 13.3 Schwingungstemperaturen zweiatomiger Moleküle.*)
13 Kapitel 14Tab. 14.1 Dipolmomente und Polarisierbarkeitsvolumina. *)Tab. 14.2 Wechselwirkungsenergien.Tab. 14.3 Lennard-Jones-(12,6)-Parameter.*)Tab. 14.4 Oberflächenspannungen von Flüssigkeiten bei 293 K.*)Tab. 14.5 Abhängigkeit der Gestalt von Mizellen vom Tensidparameter.
14 Kapitel 15Tab. 15.1 Die sieben Kristallsysteme. *)Tab. 15.2 Die Kristallstrukturen einiger Elemente. *)Tab. 15.3 Ionenradien, r /pm. *)Tab. 15.4 Madelung-Konstanten.Tab. 15.5 Gitterenthalpien bei 298 K. *)Tab. 15.6 Magnetische Suszeptibilitäten bei 298 K. *)
15 Kapitel 16Tab. 16.1 Transporteigenschaften von Gasen bei 1 atm. *)Tab. 16.2 Viskositäten von Flüssigkeiten bei 298 K. *)Tab. 16.3 Ionenbeweglichkeiten in Wasser bei 298 K. *)Tab. 16.4 Diffusionskoeffizienten bei 298 K. *)
Читать дальше

 A(Oberf...Abb. 19.18 Die isostere Adsorptionsenthalpie kann aus der Steigung der Gerade be...Abb. 19.19 Die BET‐Isotherme für verschiedene Werte von c . Das Verhältnis
A(Oberf...Abb. 19.18 Die isostere Adsorptionsenthalpie kann aus der Steigung der Gerade be...Abb. 19.19 Die BET‐Isotherme für verschiedene Werte von c . Das Verhältnis 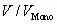 ste...Abb. 19.20 Man kann die BET‐Isotherme überprüfen und ihre Parameter bestimmen, i...Abb. 19.21 Der Verlauf der potenziellen Energie bei der dissoziativen Chemisorpt...Abb. 19.22 Die Adsorptionswahrscheinlichkeit von N 2an verschiedenen Flächen ein...Abb. 19.23 Das Desorptionsspektrum (TPD) von Wasserstoffgas, das sich von einer ...Abb. 19.24 Die Reaktionsprofile für katalysierte und unkatalysierte Reaktionen. ...Abb. 19.25 Die „Vulkankurve“ der katalytischen Aktivität entsteht, da die Reakta...Abb. A1 Eine schematische Darstellung der Anordnung der Si‐, Al‐ und O‐Atome in ...Abb. 19.26 Ein einfaches Modell für die Grenzfläche Elektrode‐Lösung. Die Grenzf...Abb. 19.27 Das Gouy‐Chapman‐Modell der elektrischen Doppelschicht beschreibt die...Abb. 19.28 Das Stern‐Modell der Grenzfläche zwischen Elektrode und Lösung. Es ko...Abb. 19.29 Die Gesamtstromdichte ist als Differenz der kathodischen und der anod...Abb. 19.30 Profile für die Variation der Freien Enthalpie zwischen den oxidierte...Abb. 19.31 Die Abhängigkeit der Stromdichte von der Überspannung für verschieden...Abb. 19.32 Die Abhängigkeit der anodischen (rot) bzw. kathodischen (blau) Stromd...Abb. 19.33 Mithilfe einer Tafel‐Auftragung lässt sich die Austauschstromdichte (...Abb. 19.34 Die Änderung der Potenzialdifferenz mit der Zeit (a) und die resultie...Abb. 19.35 (a) Die zeitabhängige Änderung der Potenzialdifferenz, die bei der Au...Abb. 19.36 Die zyklischen Voltammogramme zu Beispiel 19.6 für (a) eine geringe u...Abb. 19.37 Das zyklische Voltammogramm zu Selbsttest 19.6.Abb. A1 Eine einzelne Zelle einer Wasserstoff/Sauerstoff‐Brennstoffzelle. In de...Abb. 19.38 Die zweidimensionalen Gitter, die in Aufgabe S19.1.1 besprochen werde...Abb. 19.39 Das Voltammogramm zu Aufgabe S19.4.8.
ste...Abb. 19.20 Man kann die BET‐Isotherme überprüfen und ihre Parameter bestimmen, i...Abb. 19.21 Der Verlauf der potenziellen Energie bei der dissoziativen Chemisorpt...Abb. 19.22 Die Adsorptionswahrscheinlichkeit von N 2an verschiedenen Flächen ein...Abb. 19.23 Das Desorptionsspektrum (TPD) von Wasserstoffgas, das sich von einer ...Abb. 19.24 Die Reaktionsprofile für katalysierte und unkatalysierte Reaktionen. ...Abb. 19.25 Die „Vulkankurve“ der katalytischen Aktivität entsteht, da die Reakta...Abb. A1 Eine schematische Darstellung der Anordnung der Si‐, Al‐ und O‐Atome in ...Abb. 19.26 Ein einfaches Modell für die Grenzfläche Elektrode‐Lösung. Die Grenzf...Abb. 19.27 Das Gouy‐Chapman‐Modell der elektrischen Doppelschicht beschreibt die...Abb. 19.28 Das Stern‐Modell der Grenzfläche zwischen Elektrode und Lösung. Es ko...Abb. 19.29 Die Gesamtstromdichte ist als Differenz der kathodischen und der anod...Abb. 19.30 Profile für die Variation der Freien Enthalpie zwischen den oxidierte...Abb. 19.31 Die Abhängigkeit der Stromdichte von der Überspannung für verschieden...Abb. 19.32 Die Abhängigkeit der anodischen (rot) bzw. kathodischen (blau) Stromd...Abb. 19.33 Mithilfe einer Tafel‐Auftragung lässt sich die Austauschstromdichte (...Abb. 19.34 Die Änderung der Potenzialdifferenz mit der Zeit (a) und die resultie...Abb. 19.35 (a) Die zeitabhängige Änderung der Potenzialdifferenz, die bei der Au...Abb. 19.36 Die zyklischen Voltammogramme zu Beispiel 19.6 für (a) eine geringe u...Abb. 19.37 Das zyklische Voltammogramm zu Selbsttest 19.6.Abb. A1 Eine einzelne Zelle einer Wasserstoff/Sauerstoff‐Brennstoffzelle. In de...Abb. 19.38 Die zweidimensionalen Gitter, die in Aufgabe S19.1.1 besprochen werde...Abb. 19.39 Das Voltammogramm zu Aufgabe S19.4.8.










