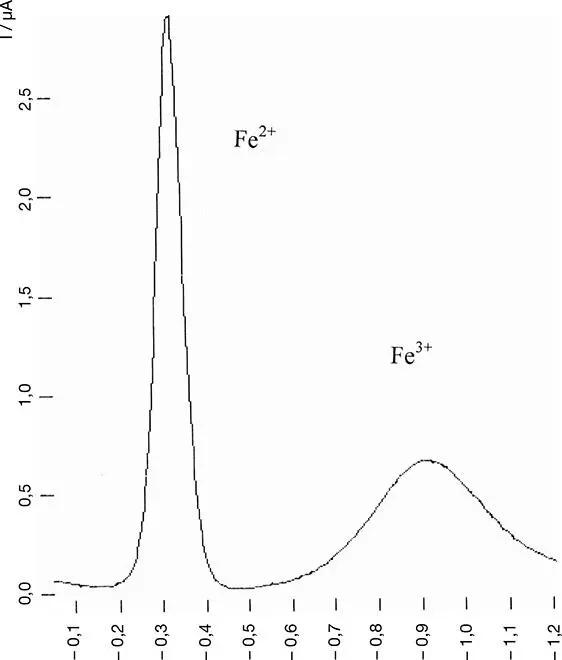
Abb. 1.3 Polarogramm einer Eisenlösung in Essigessenz mit Fe(II)- und Fe(III)-Ionen Methode: Differenzielle Pulse-Polarografie mit Quecksilbertropfelektrode, U(start): –50 mV, U(end) –1600 mV, Elektrolyt: 0,1 mol/l Na 4P 2O 7× 10 H 2O, pH 10,3.
D. Kalkwasser – zum Nachweis von Carbonat, Phosphat und Oxalat
| Materialien |
100 ml-Becherglas, 100 ml-Vorratsflasche, „Blitzzement“ (enthält Portlandzement und Calciumhydroxid ) |
| Herstellung |
20 g Blitzzement werden vorsichtig (H- und P-Sätze auf der Verpackung beachten) mit 50 ml Wasser im Becherglas angerührt. Nach 1–2 min Rühren lässt man den Hauptanteil des Feststoffes absitzen und filtriert die dekantierte überstehende Lösung in die Vorratsflasche. Aus 20 g Blitzzement und 50 ml Wasser werden etwa 25 ml Filtrat erhalten. ( Anregung : Anstelle des Kalkwassers kann auch ein Gipswasser , eine gesättigte Lösung von Calciumsulfat, zum Nachweis von vor allem Carbonaten verwendet werden.) |
| Erläuterung |
Im Reparaturmörtel ist Calciumoxid enthalten, das sich in Wasser zum Teil zu einer gesättigten Lösung an Calciumhydroxid (unter Freiwerden von Wärme) löst. |
| Verwendung |
Aufgrund der schwerlöslichen Calciumverbindungen Calciumcarbonat, Calciumoxalat und Calciumphosphat dient diese Lösung zum Nachweis der entsprechenden Anionen. (Rotkohlsaft – Reagenz A – färbt sich im Kalkwasser grün.) |
E. Seifenauflösung – ein historisches Reagenz
Historisches
Die „Seifenauflösung“ gehört zu den klassischen Reagenzien der „Probierkabinette“, die als Experimentkästen oder besser tragbare Laboratorien um 1800 gehandelt wurden ( Abb. 1.4). Autoren solcher Probierkabinette, die zahlreiche Reagenzien in Flaschen und ein Anleitungsbuch enthielten, waren der Jenaer Chemieprofessor Göttling (1755–1809) und der Pharmazeut Wiegleb (1732–1800). Goethe setzte einem solchen Probierkabinett in seinem Roman „Die Wahlverwandtschaften“ ein literarisches Denkmal. (s. in G. Schwedt: Goethes chemische Experimente, Köln 1999)
| Materialien |
100 ml-Becherglas, 100 ml-Vorratsflasche, Spiritus, Seife ohne EDTA und Etidronat (z. B. Palmolive Original ) |
| Herstellung |
Von der Seife wird Pulver mittels Abschaben im Becherglas mit Spiritus übergossen und einige Minuten durch Umrühren gelöst. Dann wird die Lösung in die Vorratsflasche filtriert. |
| Erläuterung |
Seife enthält Natriumsalze (engl. unter „Ingredients“ als sodium bezeichnet) von z. B. Palmkernöl (engl. sodium palm kernelate). Sie lösen sich zum Teil im Spiritus. |
| Verwendung |
Durch den Zusatz einer Säure bilden sich aus den Salzen schwerlösliche Fettsäuren, die eine milchige Trübung verursachen. Calcium- oder Magnesium- und andere Ionen ergeben schwerlösliche Salze, die in Form von Flocken ausfallen und gegen das Licht betrachtet infolge Lichtbrechung rötlich erscheinen. Mit der Seifenauflösung können somit sowohl freie Säuren als auch vor allem Calciumsalze nachgewiesen werden, welche die Härte des Wassers verursachen (s. dazu Kap. 13). |

Abb. 1.4 Nachbau des chemischen Probierkabinetts von Göttling aus Jena von 1790 – aus der Werkstatt des Instituts für Anorganische und Analytische Chemie der TU Clausthal.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «ЛитРес».
Прочитайте эту книгу целиком, купив полную легальную версию на ЛитРес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.














