Моделируя структуру Na 2He, необходимо учитывать тот факт, что 3d 10подуровень для натрия останется полностью свободным, следовательно количество треугольников в атомах Na составит 17—10+2=9, где 17 – полное число треугольников для натрия Na, а 10 – количество потенциальных ям, расположенных на незаполненном 3d 10подуровне. Аналогичным образом возможно вычесть 6 из 9: 9—6—2=1, поскольку заполнение электронами оболочек атомов натрия может остановиться на 3s 2 подуровне, где 6 – количество потенциальных ям, находящихся на свободной 3p 6 орбитали. Таким образом, на одном уровне при заполнении частицами подуровней s и p происходит конкуренция. С орбитали 4s 2 могут спускаться электроны на оболочку атома для заполнения свободных потенциальных ям (треугольников), однако, частицы также способны подниматься на более высокий уровень. По факту в структуре Na 2He электроны заполнят 4s 2подуровень, следовательно в выражении, полученном для вычисления количества треугольников, необходимо дополнительно учесть коэффициент, принимающий в расчёт две свободно блуждающие частицы.
При изменении внутренней энергии u в кристалле или в молекуле решение уравнения Шрёдингера преобразует свой вид. Вместе с тем происходит перераспределение потенциальных ям в пространстве химического соединения. После чего некоторые атомы могут занять промежуточные положения относительно наиболее компактной структуры, перемещаясь под действием кулоновских сил. В случае, когда пространство синусоидальной функции стабилизируется, тогда атомы вновь заполнят те или иные потенциальные ямы. В результате квантовая система примет стабильное состояние, отвечающее требованиям компактности и симметрии полученной структуры.
Пример 4.2. CaF 2He
Количество треугольников для фтора можно определить из выражения:
F=14-6-9+2=1
где 14 – количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=2.
6 – количество электронов, находящихся на уровне h=1, в трёхкратном увеличении.
9 – порядковый номер фтора F.
2 – номер последнего химического элемента, расположенного на предыдущем уровне h=1.
Количество треугольников для кальция составит: Ca=48-30-20+10=8, Электрон с 4s 2подуровня спустится на 3-й уровень, тогда Ca=7;
где 48 – количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=3.
30 – количество электронов, находящихся на предыдущих оболочках куба (атома) уровней h=1 и h=2, в трёхкратном увеличении.
20 – порядковый номер, определяемый согласно таблице Менделеева для кальция Ca.
10 – номер последнего химического элемента, находящегося на предыдущем уровне h=2.
Вычислим количество крестиков:
Ca=48—7=41; F=14—1=13.
Расчётные параметры для гелия He были определены в примере 4.1.
Перейдём к построению кристаллической структуры CaF 2He.
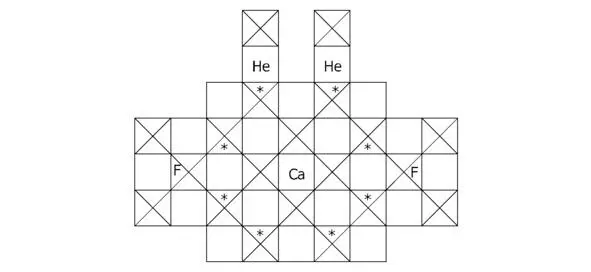
Рисунок 4.3 Вид «спереди» для структуры CaF 2He.
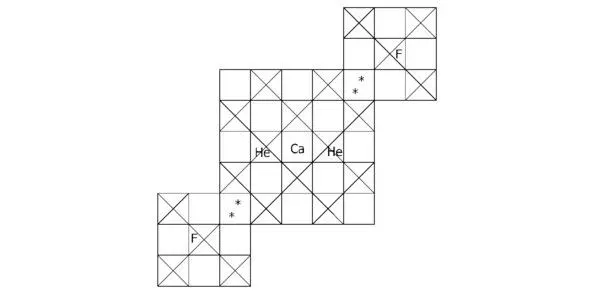
Рисунок 4.4 Вид «сверху» для структуры CaF 2He.
CaF 2He представляет собой слоистый материал с соединением каждого из слоёв по типу рисунка 3.4.
Пример 4.3. MgF 2He
Аналогично кристаллу CaF 2He, можно построить структуру MgF 2He.
Количество треугольников для магния составит:
Mg=48-30-12+10—10=6. Вместе с тем в атомах исследуемого химического элемента 4s 2подуровень будет заполнен одним электроном, тогда Mg=7.
где 48 – количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=3.
30 – количество электронов, находящихся на предыдущих оболочках куба (атома) уровней h=1 и h=2, в трёхкратном увеличении.
12 – порядковый номер, определяемый согласно таблице Менделеева для магния Mg.
10 – номер последнего химического элемента, находящегося на предыдущем уровне h=2.
– 10 – количество свободных потенциальных ям, расположенных на незаполненном 3d 10подуровне.
Вычислим количество крестиков:
Mg=48-7-10=31
Расчётные параметры для гелия He и фтора F были определены в примерах 4.1 и 4.2 соответственно.
MgF 2He является проводником электрического тока, поскольку в процессе поиска наиболее компактного вида структуры произошло заполнение электронами 4s 2подуровня.
Перейдём к изображению структуры MgF 2He на рисунках 4.5 и 4.6.
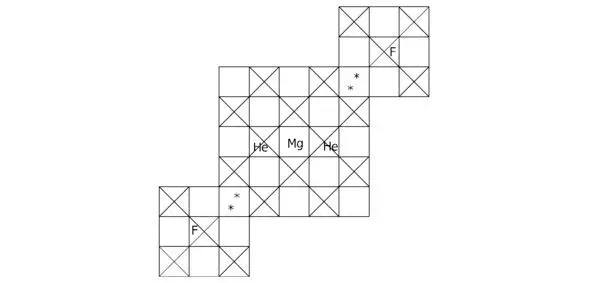
Рисунок 4.5 Вид «сверху» для MgF 2He.
Читать дальше















