На химическом жаргоне это называется плотная упаковка , но, если вы внимательно посмотрите на модель строения белого олова на рисунке 35 (речь о металлической форме), вы увидите, что она не в точности соответствует расположению апельсинов на рисунке 36. Это потому, что даже в металлическом олове присутствуют некоторые остаточные характеристики локализованных двухэлектронных связей серого олова, имеющего структуру алмаза. Металлы, которые точно соответствуют догме плотной упаковки, – это, например, магний и цинк.
Переход из металла в твердое вещество с атомной кристаллической решеткой должен протекать при 13 °C, то есть серое неметаллическое олово существует при более низких температурах – по крайней мере, так утверждает термодинамика. Однако термодинамика может лишь сказать нам, какие перемены в принципе возможны, но не дает представления об их скорости. На самом деле для металлического олова при температурах чуть ниже 13 °C эта реакция протекает бесконечно медленно.
Вы, наверное, задаетесь вопросом, почему вообще существует металлическая форма, если серое олово более стабильно и характеризуется меньшей энергией. Если подобное расположение атомов стабильно при 12 °C, то почему не при 14 °C?
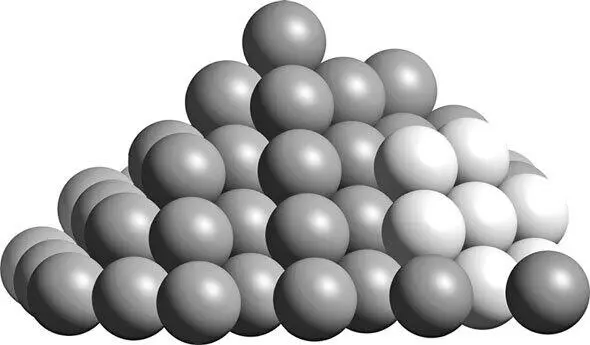
Рисунок 36.Модель расположения атомов в металле – способ упаковать апельсины (или атомы) наиболее плотно, сведя к минимуму пространство между ними. Семь светло окрашенных атомов справа показывают, как именно шесть атомов располагаются вокруг одного центрального атома в плоскости; еще три атома выше (не показаны на рисунке) и ниже составляют число ближайших соседей – 12 – в структуре с плотной упаковкой.
Можно поразмышлять об этом в категориях того, какая система наиболее вероятна. Возьмите большой «сухой бассейн» с пластиковыми шариками – в таких еще любят играть маленькие дети – и наполните его шариками примерно на три четверти. Отдельно взятый шарик, лежащий на бортике, уменьшит свою энергию и переместится в более стабильное термодинамическое состояние, упав обратно в бассейн. При этом общая энергия останется неизменной: потенциальная энергия шарика перейдет в тепловую при ударе о другие шарики. Обратный же процесс никогда не произойдет.
Однако если повысить температуру шариков, добавив туда маленьких детей, то наиболее вероятное состояние системы будет подразумевать нахождение довольно большого числа шариков за пределами бассейна. Нечто весьма похожее происходит и с атомами олова, и химики занимаются этой проблемой, численно оценивая вероятность, температуру и теплоту, выделяющуюся в результате протекания реакции, и выражая все это величиной, которую мы называем энергией Гиббса. Чтобы понять, сможет ли пройти реакция, мы рассчитываем изменения в энергии Гиббса до и после, и если она снижается, то реакция принципиально возможна [208] Часто, но не всегда происходящая реакция – та, при которой выделяется больше всего тепла. Формула для полного расчета – ΔG = ΔH – TΔS, где ΔH – выделившаяся теплота (отрицательное значение), Т – температура в Кельвинах (всегда положительная), а ΔS – изменение энтропии (высокая энтропия связана с меньшей упорядоченностью или, что то же самое, большей вероятностью состояния). Реакция возможна с термодинамической точки зрения, когда изменения в величине G, то есть ΔG, меньше нуля.
.
Переход олова начинает ускоряться при более низких температурах, с максимальными значениями скорости в температурном диапазоне от –20 °C до –40 °C, и существует множество задокументированных случаев «оловянной чумы», особенно заметных в органных трубах церквей Северной Европы. История об армии Наполеона, конечно, куда более эффектна и всегда очень нравилась учителям и авторам учебников, которые любят приправлять свои рассказы занятными деталями.
Так что, какой бы сомнительной ни была эта деталь, она все же попала в учебники по общей химии для школы и младших курсов, и обычно это сопровождается пометкой, что ее связь с реальной историей вызывает сомнения. Существуют также различные версии: например, одна из них гласит, что олово вместо меди использовали из экономии [209] Chang R. General Chemistry, 10th ed. McGraw-Hill, 2010.
; кроме того, некоторые авторы переименовывают битвы, так что бойня под Бородином превращается у них в «осаду Москвы» [210] Petrucci R., Harwood W.S., Madura J.D. General Chemistry: Principles and Modern Applications. Pearson/Prentice Hall, Upper Saddle River, 2007.
. Некоторые также пользуются возможностью пошутить, вставляя в текст описания французских солдат, которые пытаются сражаться одной рукой, второй придерживая штаны.
Читать дальше
Конец ознакомительного отрывка
Купить книгу













