К тому же если главная причина старения – в гиперфункции, а молекулярный мусор не так важен для продолжительности жизни, то системы, которые этот мусор производят, должны ускользать из-под контроля естественного отбора. В таком случае они должны производить все больше и больше мусора (потому что ломать гораздо дешевле, чем чинить) – пока поломок не станет так много, что они начнут сокращать жизнь наравне с гиперфункцией органов. Это тот же аргумент про бочку с вытекающей водой и короткой дощечкой, с которого я начала разговор о причинах старения: ни одна не может быть главной, все системы защиты от старости работают одинаково плохо.
У М. Благосклонного и на это находятся свои аргументы. Ни один человек, говорит он [633] Blagosklonny M. V. Aging and immortality: quasi-programmed senescence and its pharmacologic inhibition // Cell Cycle. 2006 Sep; 5 (18): 2087–2102.
, не умирает от накопления в клетках молекулярного мусора. А также от укорочения теломер, истощения клеточных запасов или износа тканей. Люди умирают от инфарктов, инсультов и опухолей – катастрофических событий внутри тела, когда те или иные органы перестают работать. А эти события, в свою очередь, напрямую вызваны гиперфункцией физиологических процессов: повышенным давлением, разрушением костей, ожирением и десятками других. Молекулярный мусор и поломки, безусловно, накапливаются в клетках и между ними, но не успевают привести организм к смерти, катастрофа случается раньше.
Старение клеток, согласно теории М. Благосклонного, тоже вызвано гиперфункцией, а точнее – гиперстимуляцией. Все начинается с того, что на клетку действует какой-то стрессовый фактор: повреждение ДНК, радиация, окислительный стресс, работа онкогенов и так далее. В клетке активируются белки р21 и р16 и приостанавливают деление клетки, давая ей возможность побыть в покое и разобраться с происходящим.
В этот момент клетка еще способна вернуться к полноценной жизни: она временно перестала делиться, но сможет продолжить, как только справится со стрессом. Однако если даже в покое она все еще получает сигнал к размножению, то продолжает расти и производить токсичные продукты обмена, на которые снова реагируют р21 и р16 – и окончательно останавливают деление клетки, она становится сенесцентной. Так гиперстимуляция клетки, то есть гиперфункция программы роста, приводит к старению. В некотором смысле клетка повторяет судьбу организма в целом: чем быстрее она растет и размножается, тем меньше она живет. И наоборот: чем медленнее ее обмен веществ и чем дольше цикл деления, тем выше шанс не состариться.
Глубинный механизм роста, тот самый главный рубильник, который включает квазипрограмму старения на клеточном уровне, давно известен: его имя TOR. Сходство с богом Тором здесь случайно, название белка – это аббревиатура: Target Of Rapamycin, то есть "мишень действия рапамицина" – лекарства, о котором нам еще предстоит поговорить. В клетках млекопитающих TOR входит [634] Kapahi P. et al. With TOR, less is more: a key role for the conserved nutrient-sensing tor pathway in aging // Cell Metabolism. 2010 Jun; 11 (6): 453–465.
в состав двух комплексов с другими белками – mTORc1 и mTORc2, – но для простоты мы их будем называть общим именем mTOR. Оба комплекса напрямую отвечают за рост и развитие клеток: стимулируют работу генов и производство белков, усиливают обмен веществ, заставляют клетку расти и запасать энергию, но в то же время подавляют аутофагию (самопереваривание) и репарацию (ремонт ДНК). Мутации в mTOR приводят к остановке роста, и такие организмы нежизнеспособны.
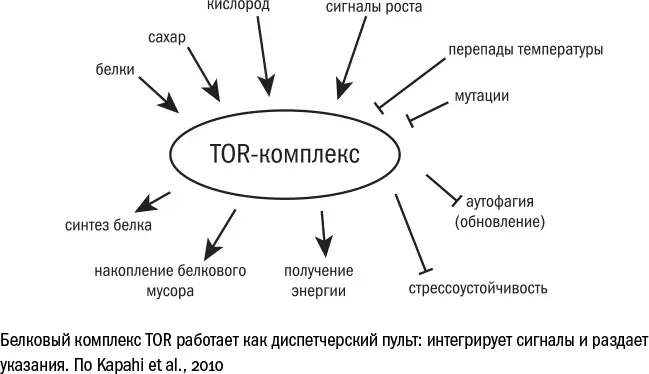
Комплекс mTOR служит в некотором роде центром принятия [635] Valvezan A. J. & Manning B. D. Molecular logic of mTORC1 signalling as a metabolic rheostat // Nature Metabolism. 2019 Mar; 1: 321–333.
клеточных решений. К нему стекается информация о сигналах извне и состоянии клетки изнутри, и, взвешивая все за и против, он либо стимулирует рост, либо тормозит его. Основные два его информанта – это факторы роста (снаружи) и питательные вещества (изнутри). Первых обычно недостаточно, чтобы запустить работу mTOR, вторые же справляются, но не в полной мере. И только совместное действие внешних и внутренних стимулов раскручивает маховик mTOR на максимальную мощность.
В первую очередь mTOR реагирует [636] См. п. 205.
на присутствие в клетке аминокислот: если их достаточно, значит, есть из чего построить белки и mTOR активен, если мало, то он "молчит". Кроме того, работа mTOR зависит [637] Wiley C. D. & Campisi J. From ancient pathways to aging cells – connecting metabolism and cellular senescence // Cell Metabolism. 2016 Jun; 23 (6): 1013–1021.
от количества АТФ (энергетической "валюты" клетки): если АТФ недостаточно, действие mTOR ослабевает. Есть и другие условия, которые заставляют mTOR усмирить свой пыл: это гипоксия (дефицит кислорода), поломки в ДНК, отравление токсинами, перепады температуры и прочие стрессовые факторы. А судьба клетки зависит от суммы этих факторов: если, несмотря на стресс (который тормозит mTOR), в ней все равно много энергии, а снаружи – факторов роста (которые активируют mTOR), главный рубильник остается активен, подстегивает синтез белков, тормозит репарацию и приближает старение.
Читать дальше
Конец ознакомительного отрывка
Купить книгу













