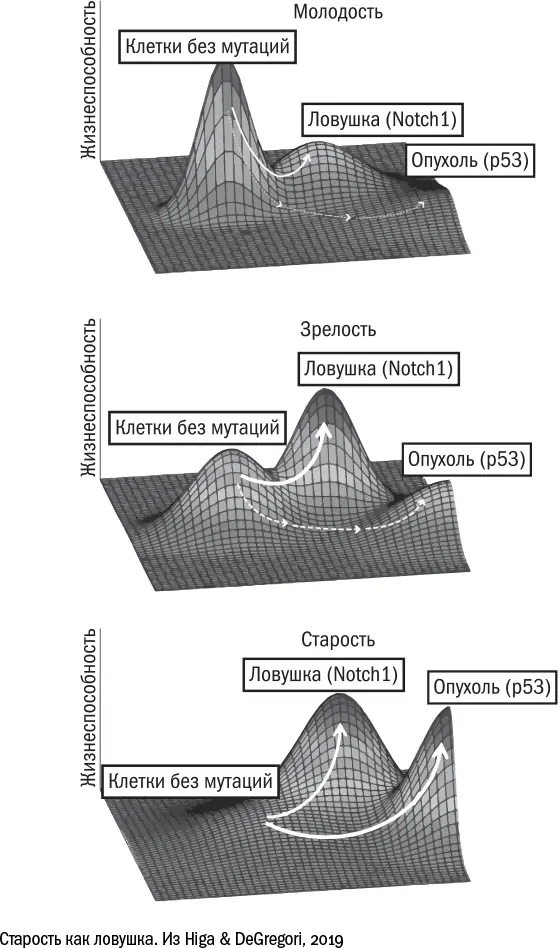
На первый взгляд может показаться, что рак и старость воюют на одной стороне – против долгой жизни человека. На деле же они конкурируют друг с другом, тем самым изрядно усложняя нам задачу. Победив рак, мы столкнемся лицом к лицу с проблемой сенесцентных клеток. Избавившись от старения, мы останемся наедине с нерешенной проблемой рака.
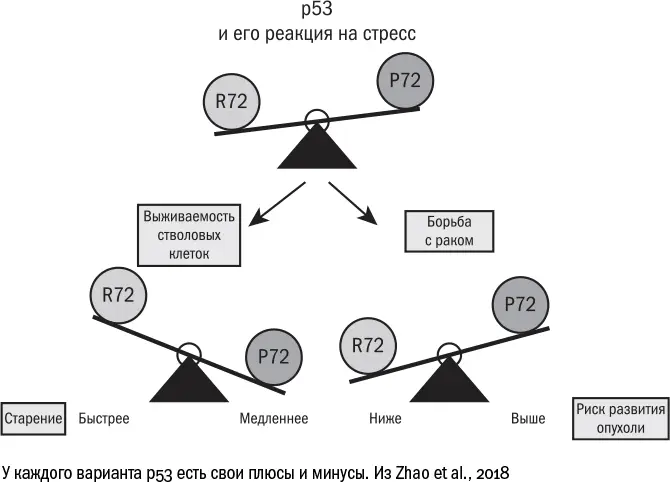
Каждый человек на самом деле уже находится на той или другой стороне этих весов. Дело в том, что у нас встречается два варианта белка р53, которые различаются всего лишь одной аминокислотой, 72-й по счету. Вариант R72 работает лучше: более прочно связывается со своими мишенями и, следовательно, эффективнее запускает в клетках старение и апоптоз. Вариант Р72 действует слабее, а его носители, по некоторым данным [544] Van Heemst D. et al. Variation in the human TP53 gene affects old age survival and cancer mortality // Experimental Gerontology. 2005 Jan – Feb; 40 (1–2): 11–15.
, чаще страдают от опухолей. Зато среди долгожителей в разных популяциях [545] Zhao Y. et al. A polymorphism in the tumor suppressor p53 affects aging and longevity in mouse models // eLife. 2018 Mar; 7: e34701.
(хотя и не во всех [546] См. п. 110.
) людей с Р72 оказывается больше, чем с R72.
Оба варианта чем-то выгодны. С одной стороны, можно иметь активный белок р53 и не страдать от онкологических болезней. Но тогда суровый охранник-р53 будет останавливать деление во всех клетках, которые покажутся ему сколько-то подозрительными, и к старости в организме останется меньше клеток, способных делиться и обновлять ткани, и жизнь окажется короче. С другой стороны, можно иметь более толерантную версию р53 и повышенный риск рака. Но если человек как-то со своей опухолью справляется, то жизнь его оказывается дольше, потому что сенесцентных клеток накапливается меньше. Как говорилось в пьесе Леонида Филатова, "но какие выживают – те до старости живут". А вот заполучить одновременно и долгую жизнь, и низкий риск развития рака, кажется, невозможно. Придется выбирать.
Коль скоро старение клеток в борьбе с раком неизбежно, есть только один способ противостоять им одновременно – убивать сенесцентные клетки, которые представляют собой тупиковую ветвь клеточного развития. От них не приходится ждать, что они "исправятся" или вернутся к прежней жизни. А вот проблем доставляют немало: выделяют провоспалительные белки, разрушают матрикс и заражают старостью соседей.
Первый механизм избирательного отстрела старых клеток придумал [547] Baker D. J. et al. Clearance of p16Ink4a-positive senescent cells delays ageing-associated disorders // Nature. 2011 Nov; 479 (7372): 232–236.
геронтолог Джеймс Киркленд. Вместе с коллегами он создал трансгенных мышей INK-ATTAC. Во всех сенесцентных клетках активна область ДНК под названием INK. Киркленд встроил после нее ген АТТАС , который кодирует одну из каспаз – белков, запускающих апоптоз. Таким образом, все сенесцентные клетки в такой трансгенной мыши производили эту каспазу. А запустить ее работу можно было с помощью специального препарата – АР20187, – тогда клетка умирала посредством апоптоза.
Так у Киркленда с коллегами получился первый сенолитик – лекарство, которое уничтожает только старые клетки. Модельные мыши INK-ATTAC под действием сенолитика прожили [548] Baker D. J. et al. Naturally occurring p16Ink4a-positive cells shorten healthy lifespan // Nature. 2016 Aug; 530 (7589): 184–189.
в среднем на треть больше контрольных животных. Для достижения этого эффекта оказалось достаточно уничтожить лишь треть сенесцентных клеток в их тканях. Позже оказалось, что сенолитик помогает мышам справиться с нарушениями [549] Palmer A. K. et a. Targeting senescent cells alleviates obesity‐induced metabolic dysfunction // Aging Cell. 2019 Mar; 18 (3): e12950.
обмена веществ при ожирении и возрастной атрофией [550] Patil P. et al. Systemic clearance of p16INK4a ‐positive senescent cells mitigates age‐associated intervertebral disc degeneration // Aging Cell. 2019 Mar; 18 (3): e12927.
межпозвоночных дисков, то есть борется с возрастными болезнями.
Вдохновившись этими результатами, ученые начали искать природные сенолитики, которые действовали бы не только на модельных трансгенных животных, но и на обычных, и в перспективе – на человека. Группа Киркленда предложила [551] Zhu Y. et al. The Achilles' heel of senescent cells: from transcriptome to senolytic drugs // Aging Cell. 2015 Mar; 14 (4): 644–658.
искать их среди противоопухолевых лекарств. Коль скоро сенесцентные клетки – это "недоделанные" раковые, то они должны поддаваться действию тех же препаратов, но в меньшей концентрации. И Киркленд оказался прав: подавляющее большинство известных на настоящий момент сенолитиков – это противоопухолевые лекарства, только применяются они в небольших дозировках.
Читать дальше
Конец ознакомительного отрывка
Купить книгу














