В § 1 мы видели, что связь двух различных ионов посредством одного электрона чаще всего оказывается весьма слабой. При двухэлектронной связи это не так. Представим, что два протона на фиг. 8.4 мы заменили любой парой ионов (с замкнутыми внутренними электронными оболочками и единичным ионным зарядом) и что энергии связи электрона в этих двух ионах различны. Энергии состояний | 1 > и | 2 > по-прежнему будут равны друг другу, потому что в каждом из этих состояний имеется по одному электрону на каждый ион. Поэтому у нас всегда будет расщепление, пропорциональное А. Двухэлектронная связь поистине вездесуща — это самая обычная валентная связь. Химическая связь, как правило, предполагает эту игру в «туда-сюда», в которую играют два электрона. Хотя пара атомов может быть связана только одним электроном, это случается сравнительно редко, потому что требует надлежащих условий.
Наконец, надо заметить, что если энергия притяжения электрона к одному ядру намного больше, чем к другому, то уже нельзя говорить, будто можно игнорировать другие мыслимые состояния. Пусть ядро а (это может быть и положительный ион) притягивает электрон намного сильнее, чем ядро b . Это сильное притяжение может более чем компенсировать взаимное отталкивание двух электронов. И если это так, то низшее энергетическое состояние может обладать большой амплитудой того, что оба электрона окажутся возле а (образуя отрицательный ион), и малой амплитудой того, что хотя бы один из них обнаружится возле b . Состояние выглядит как отрицательный ион рядом с положительным ионом. Именно это и случается в «ионных» молекулах наподобие NaCl. Вы видите, что мыслимы любые градации между ковалентной связью и ионной связью.
Теперь вы ясно видите, что многие химические факты на квантовомеханическом языке удается очень отчетливо понять.
§ 4. Молекула бензола
Для изображения сложных органических молекул химики изобрели изящные диаграммы. Мы хотим теперь поговорить об одной из самых интересных молекул — о молекуле бензола, диаграмма которой приведена на фиг. 8.6.
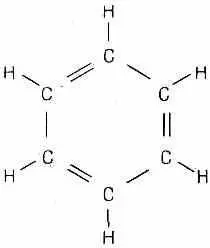
Фиг . 8 . 6. Молекула бензола С 6 Н 6 .
В нее входят по шести весьма симметрично расположенных атомов углерода и водорода. Каждая черточка на диаграмме представляет пару электронов с противоположными спинами, пляшущих танец ковалентной связи. Каждый атом водорода вводит в игру по одному электрону, а каждый атом углерода — по четыре, образуя в общей сложности систему из 30 участвующих в игре электронов. (В углероде ближе к ядру есть еще два электрона, образующих первую, или К, оболочку. Они не показаны, поскольку их связь столь тесна, что сколько-нибудь заметной важности для ковалентной связи они не представляют.) Итак, каждая черточка на рисунке представляет связь, или пару электронов, а двойные связи означают, что между чередующимися парами атомов углерода имеются по две пары электронов.
С молекулой бензола связана одна загадка. Можно подсчитать, какая энергия должна потребоваться на образование этого химического соединения, потому что химики измерили энергии различных соединений, включающих части кольца; к примеру, изучая этилен, они узнали энергию двойной связи и т. д. Поэтому мы можем подсчитать полную энергию, которую должна была бы иметь молекула бензола. Однако истинная энергия бензольного кольца намного меньше, чем получается при таком подсчете: кольцо связано куда крепче, чем полагается обычной системе «ненасыщенных двойных связей». Как правило, система двойных связей, не образующая подобного кольца, весьма легко поддается химическим атакам: ее энергия сравнительно высока, и, добавляя лишние атомы водорода, двойные связи удается легко разрывать. Не то у бензола — кольцо его почти нерушимо: сломать его нелегко. Иными словами, энергия бензола намного ниже, чем дает подсчет по картине двойных связей.
Имеется еще и другая загадка. Пусть мы заменили два смежных водорода атомами брома, образуя орто -дибромбензол. Это можно сделать двумя путями. Атомы брома могут быть на противоположных концах двойной связи (фиг. 8.7, а) или могут быть на противоположных концах одинарной связи (фиг. 8.7, б).
Читать дальше













