Auf den verschiedenen Schalen kann sich nur eine begrenzte Zahl von Elektronen-bewegen.
Man bezeichnet die Schalen mit Großbuch-

Der Atomaufbau
Flugbahnen der a-Teilchen
Goldatomkerne


Atomkern
Elektronenhülle


Atomkern
K - Schale (1. Schale)
L - Schale (2. Schale)
M - Schale (3. Schale)
N - Schale (4. Schale)



Atomkern und Atomhülle
Die ersten 4 Elektronenschalen


9
Die Besetzung der Elektronenschalen erfolgt nach der Formel:
2 n2 (n = Schalenzahl)
Man erhält auf diese Weise die maximale Elektronenzahl.
1. Schale (K-Schale):
2 n2 n = 1 2 x 1 x 1 = 2 Elektronen (max. auf der 1. Schale)
2. Schale (L-Schale):
2 n2 n = 2 2 x 2 x 2 = 8 Elektronen (max. auf der 2.Schale)
3. Schale (M-Schale):
2 n2 n = 3 2 x 3 x 3 = 18 Elektronen (max. auf der 3. Schale)
4. Schale (N-Schale):
2 n2 n = 4 2 x 4 x 4 = 32 Elektronen (max. auf der 4. Schale)
Die errechnete maximale Elektronenzahl ist ab der 5. Schale ein rein theoretischer Wert, da es Atome mit so vielen Elektronen nicht gibt. Die 3. und die 4.Schale kann maxi-mal nur 18 bzw. 32 Elektronen aufnehmen, wenn es nicht die äußerste Schale, also eine innere Schale ist. (Anwendung bei den Ne-bengruppenelementen im PSE).
Die äußerste Schale kann maximal nur 8 Elektronen aufnehmen.
Ist dieser Zustand erreicht, spricht man auch von der Edelgaskonfiguration (Edel-gaszustand) eines Atoms, da bei Edelgasen (= Elemente der 8.Hauptgruppe im PSE, siehe auch Kapitel 2.1) die äußerste Scha-le grundsätzlich mit 8 Außenelektronen besetzt ist. Die Elektronen der äußersten Schale bezeichnet man auch oft als Außen-elektronen oder Valenzelektronen. (abge-leitet vom lat. valere: den Ausschlag geben, imstande sein; denn nur Außenelektronen sind an chemischen Reaktionen beteiligt).
Zum weiteren Verständnis des Bohr’schen Atommodells berufen wir uns auf Grundla-gen der Elektrotechnik. Alle elektrisch ge-ladenen Teilchen verhalten sich nach dem Grundgesetz der Elektrostatik:
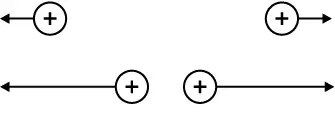
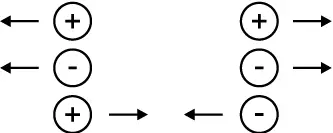
Gleichnamige Ladungen stoßen sich ab. Ungleichnamige Ladungen zie-hen sich an!
Gleichnamig geladene Teilchen sto-ßen sich ab. Ungleichnamige ziehen sich an.
Die Stärke der Abstoßungskraft nimmt mit zunehmendem Abstand ab.


Der Atomaufbau
Die Kraft der Anziehung bzw. der Absto-ßung lässt mit zunehmendem Abstand der geladenen Teilchen voneinander sehr stark nach.
Protonen und Elektronen ziehen sich also gegenseitig an. Warum fallen die Elekt-ronen dann nicht in den Atomkern zu den Protonen?
Begründung: Die elektrostatische Anzie-hungskraft zum Atomkern hin wird von ei-ner gleichgroßen Kraft vom Atomkern weg neutralisiert, der Zentrifugalkraft. Die um den Atomkern kreisenden Elektronen besit-zen eine bestimmte Energie, die verhindert, dass die Elektronen in den Kern stürzen.

10

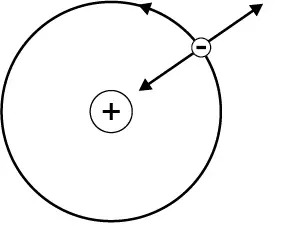
Die Zentrifugalkraft tritt überall dort auf, wo sich etwas auf seiner Kreisbahn um einen Mittelpunkt bewegt. Das Zusammentreffen von Anziehungskraft und Zentrifugalkraft bewirkt, dass der kreisende Teil weder auf den Mittelpunkt hin fällt noch ganz aus dem Kreis entweicht, sondern auf seiner Kreis-bahn bleibt.
Die Zentrifugalkraft wirkt der An-ziehungskraft entgegen und bewirkt, dass die Elektronen auf ihrer Kreisbahn bleiben
9,11 x 10-28g
Die Masse eines Elektrons ist daher für die Gesamtmasse eines Atoms fast ohne Bedeu-tung und für die Berechnung der Atommas-se zu vernachlässigen.
Die absolute Atommasse (Einheit g) setzt sich daher zusammen aus der Masse der Protonen und der Masse der Neutronen. Sie ist unvorstellbar klein. Ihre Werte bewegen sich zwischen
10-24g und 10-22g
Beispiele: Wasserstoffatom: 1,67 x 10-24 g (Das einfachste Wasserstoffatom hat im Atomkern nur 1 Proton. Die absolute Atom-masse des Wasserstoffs entspricht daher der Protonenmasse).
Kohlenstoffatom: 20 x 10-24g
Größenverhältnisse: Atomkern/Atomhülle
Atomkerne sind sehr klein. Der Durchmes-ser des Atomkerns (10-13 cm) ist mehr als 100.000-mal kleiner als der Durchmesser des gesamten Atoms.
Zum Vergleich:
Wäre der Atomkern so groß wie ein Steck-
nadelkopf von 2 mm Durchmesser, so würde der Durchmesser der Atomhülle 200 Meter betragen. Der sehr kleine Atomkern enthält aber fast die gesamte Masse eines Atoms, während die Elektronenhülle nahezu mas-seleer ist.
Wie schwer sind Atome?
Читать дальше