Janko Auerswald - Grundlagen der Funktionswerkstoffe für Studium und Praxis
Здесь есть возможность читать онлайн «Janko Auerswald - Grundlagen der Funktionswerkstoffe für Studium und Praxis» — ознакомительный отрывок электронной книги совершенно бесплатно, а после прочтения отрывка купить полную версию. В некоторых случаях можно слушать аудио, скачать через торрент в формате fb2 и присутствует краткое содержание. Жанр: unrecognised, на немецком языке. Описание произведения, (предисловие) а так же отзывы посетителей доступны на портале библиотеки ЛибКат.
- Название:Grundlagen der Funktionswerkstoffe für Studium und Praxis
- Автор:
- Жанр:
- Год:неизвестен
- ISBN:нет данных
- Рейтинг книги:5 / 5. Голосов: 1
-
Избранное:Добавить в избранное
- Отзывы:
-
Ваша оценка:
- 100
- 1
- 2
- 3
- 4
- 5
Grundlagen der Funktionswerkstoffe für Studium und Praxis: краткое содержание, описание и аннотация
Предлагаем к чтению аннотацию, описание, краткое содержание или предисловие (зависит от того, что написал сам автор книги «Grundlagen der Funktionswerkstoffe für Studium und Praxis»). Если вы не нашли необходимую информацию о книге — напишите в комментариях, мы постараемся отыскать её.
Grundlagen der Funktionswerkstoffe für Studium und Praxis — читать онлайн ознакомительный отрывок
Ниже представлен текст книги, разбитый по страницам. Система сохранения места последней прочитанной страницы, позволяет с удобством читать онлайн бесплатно книгу «Grundlagen der Funktionswerkstoffe für Studium und Praxis», без необходимости каждый раз заново искать на чём Вы остановились. Поставьте закладку, и сможете в любой момент перейти на страницу, на которой закончили чтение.
Интервал:
Закладка:
So wie das Magische Zifferblatt den Blick in ein verborgenes Uhrwerk freigibt, so möge Ihnen, liebe Leserin und lieber Leser, dieses Buch das Eintauchen in die faszinierende Welt der Funktionswerkstoffe erleichtern und als Inspirationsquelle für zukünftige Ideen dienen.
Luzern, am 24.08.2021
Janko Auerswald und Pius Portmann
Danksagung
Als federführender Autor danke ich meinem Co-Autor Pius Portmann für seine wertvollen Beiträge und dem Team des Verlags Wiley-VCH für die großartige Unterstützung. Ein ganz besonderer Dank gilt meiner wunderbaren Familie, die während des Verfassens dieses Buches so manchen Abend auf mich verzichten musste.
Janko Auerswald
1
Einführung und Grundlagen
Die Eigenschaften von Funktionswerkstoffen hängen eng mit ihrer chemischen Bindungsart und mit der atomaren oder molekularen Struktur zusammen. Daher liegt der Fokus zunächst auf den Bindungsarten und Strukturkonzepten von Metallen, Halbleitern, Keramiken und Polymeren. Aber auch die Begriffe der Tropie (Richtungsabhängigkeit der Eigenschaften), Polymorphie (Vielgestalt bzw. Wechsel der Kristallstruktur) und Phasen (homogenes und heterogene Gefüge) spielen für das Verständnis der Eigenschaften eine wichtige Rolle.
Werkstoffe werden aus Rohstoffen hergestellt. Deren Gewinnung, Handel, Verbrauch und Entsorgung stellen einen tiefen Eingriff in ökologische, ökonomische und soziale Systeme dar. Im Zeitalter von Globalisierung, Wirtschaftswachstum, übermäßigem Ressourcenverbrauch und Klimawandel ist es auch für die Werkstoffkunde an der Zeit, das Thema der ökologischen und sozialen Nachhaltigkeit in eine ganzheitliche Betrachtung aufzunehmen.
1.1 Bindungsarten
Die Art der chemischen Bindung zwischen den atomaren Bausteinen hat einen entscheidenden Einfluss auf die Eigenschaften von Funktionswerkstoffen. Eisenatome in metallischen Elektro- oder Stahlblechen tragen zur elektrischen Leitfähigkeit bei. Oxidkeramische Ferritmagneten hingegen enthalten Eisenionen und sind elektrische Isolatoren.
Die Metallbindung basiert auf einer Wolke frei beweglicher Außenelektronen. Sie umgibt die positiv geladenen Atomrümpfe des Kristallgitters und hält sie zusammen.
In einer Atombindung gehören gemeinsame Valenz-Elektronenpaare zu beiden Nachbaratomen zu gleichen Teilen, wenn die Bindung unpolar ist (z. B. in den reinen Halbleitern Silizium oder Diamant). Mit steigender Differenz der Elektronegativität beider Bindungspartner gehen die Valenz-Elektronen immer mehr zum Partner mit der höheren Elektronegativität über (polare Atombindung, z. B. in den Verbindungshalbleitern GaAs oder SiC).
Ist die Differenz der Elektronegativitäten in einer chemischen Verbindung aus Metallen und Nichtmetallen größer als 1.7 (siehe Periodensystem, Abb. 1.1), spricht man von Ionenbindung . Die Außenelektronen gehören dann komplett zum Partner mit der höheren Elektronegativität (z. B. zum Chlor in Natriumchlorid). Der Einfachheit halber kann man alle Oxidkeramiken und oxidischen Gläser dieser Gruppe zuordnen, auch wenn manche die Differenz der Elektronegativitäten von 1.7 nicht ganz erreichen.
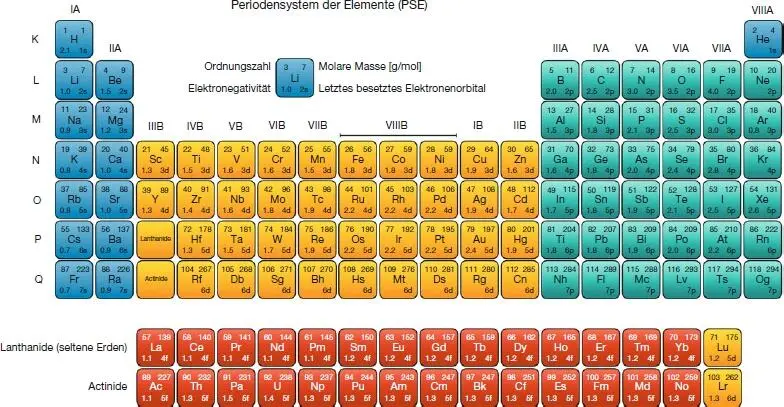
Abb. 1.1 Das Periodensystem der Elemente mit Ordnungszahlen, molaren Atommassen, Elektronegativitäten und Farbgebung gemäß einer idealen Elektronenkonfiguration.
Zwischenmolekulare Bindungen sind festigkeitsbestimmend in Werkstoffen, die aus Molekülen oder großen Makromolekülen bestehen. Dazu gehören die Kunststoffe und Silikone.
Abbildung 1.1zeigt das Periodensystem der Elemente. Die Farben der ElementeTafeln korrelieren mit dem Typ des letzten besetzten Elektronenorbitals gemäß einer idealen Elektronenkonfiguration. Bei den blau markierten Elementen (I. und II. Hauptgruppe) wäre dies theoretisch ein s-Orbital, bei den türkisgrünen (III.-VIII. Hauptgruppe) ein p-, bei den gelben (Nebengruppenelemente) ein d- und bei den roten (Lanthanide bzw. seltene Erden, Actinide) ein f-Orbital. In der Praxis gibt es jedoch Abweichungen vor allem bei den Nebengruppenelementen (gelb) sowie den Lanthaniden und Actiniden (rot). So wird bei Lanthan (La) anstelle des 4f 1-Orbitals zuerst der 5d 1-Orbital besetzt, weshalb Lanthan häufig den gelb markierten Elementen der III. Nebengruppe statt den seltenen Erden zugerechnet wird. Das eigentlich an dieser Stelle stehende Lutetium (Lu) hat mit allen 14 besetzten 4f-Orbitalen und einem besetzten 5d 1-Orbital die ideale Elektronenkonfiguration einesElements der III. Nebengruppe in der 6. Periode, wird aber im Gegenzug häufig den rot markierten seltenen Erden bzw. Lanthaniden zugerechnet.
Nähere Erläuterungen zur Besetzung der Orbitale finden sich im Kapitel Magnetwerkstoffe. Die Besetzung der Orbitale mit Elektronen hat einen wichtigen Einfluss auf die magnetischen, aber auch auf die elektrischen und optischen Eigenschaften von Werkstoffen.
1.2 Werkstoffklassen und Strukturmodelle
Aufgrund der atomaren Bausteine und der chemischen Bindung lassen sich die Werkstoffe in verschiedene Klassen einteilen: Metalle, Halbleiter, Keramiken (sowie Gläser und anorganische Bindemittel wie Zement) und Kunststoffe. Die Kombination von Materialien aus verschiedenen Klassen führt zu den Verbundwerkstoffen.
Metalle werden durch die Metallbindung zusammengehalten. Sie kommen oft in Form von Legierungen zum Einsatz, seltener in ihrer reinen Form. Durch Legieren mit anderen chemischen Elementen werden die Eigenschaften gezielt verändert. Verglichen mit Kunststoffen ist ihre Bindungskraft (der Elastizitätsmodul oder E-Modul) hoch, jedoch in der Regel etwas kleiner als bei Keramiken. Sie sind gut plastisch verformbar. Reine Metalle sind elektrisch und thermisch gute Leiter. Viele Metalle und Legierungen sind korrosionsempfindlich.
Metalle haben relativ einfache, dichtgepackte Kristallgitterstrukturen, die durch Elementarzellen beschrieben werden ( Abb. 1.2). Eine Elementarzelle ist eine kleine geometrische Einheit, die den gesamten Kristall komplett beschreibt. Metalle werden als Funktionswerkstoffe eingesetzt für mechanische Konstruktionsteile, für Leiter (Kabel und Leiterbahnen), Widerstände, Kontaktwerkstoffe, Gehäuse und andere Konstruktionsbauteile, Lötlegierungen (Sn-Pb und bleifrei), Sensoren (Thermoelemente), Aktuatoren (Formgedächtnislegierungen), weichmagnetische Induktivitäten (Spulenkerne) oder (Bio-)Sensoroberflächen.

Abb. 1.2 Typische Gitterstrukturen von Metallen. (a) kubisch-flächenzentrierte Elementarzelle (kfz), (b) kubisch-raumzentrierte Elementarzelle (krz), (c) Elementarzelle der hexagonal dichtesten Packung (hdp)
Anorganische Halbleiter bestehen aus Elementen der oberen IV. Hauptgruppe wie Silizium oder Germanium oder als Verbindungshalbleiter aus einer Kombination von Elementen aus verschiedenen Hauptgruppen (IV-IV, III-V, II-VI). Sie werden in der Regel dotiert und beruhen auf Atombindung (gemeinsame Elektronenpaare). Im Gegensatz zu Metallen (Kaltleiter) leiten Halbleiter besser bei höheren Temperaturen (Heißleiter). Sie sind spröde. Halbleiter der Hauptgruppen IV und III-V basieren auf der Diamant- bzw. Zinkblendestruktur ( Abb. 1.3).
Halbleiter werden eingesetzt als Dioden (p-n-Übergang), Transistoren (mehrere p-n-Übergänge), Leuchtdioden (LED), Laserdioden, Photodioden und Solarzellen. Des Weiteren kommen sie als Sensoren und Aktuatoren zum Einsatz (Transducer, z. B. Peltier-Elemente).
Читать дальшеИнтервал:
Закладка:
Похожие книги на «Grundlagen der Funktionswerkstoffe für Studium und Praxis»
Представляем Вашему вниманию похожие книги на «Grundlagen der Funktionswerkstoffe für Studium und Praxis» списком для выбора. Мы отобрали схожую по названию и смыслу литературу в надежде предоставить читателям больше вариантов отыскать новые, интересные, ещё непрочитанные произведения.
Обсуждение, отзывы о книге «Grundlagen der Funktionswerkstoffe für Studium und Praxis» и просто собственные мнения читателей. Оставьте ваши комментарии, напишите, что Вы думаете о произведении, его смысле или главных героях. Укажите что конкретно понравилось, а что нет, и почему Вы так считаете.












