10 Kapitel 9Abb. 9.1 VB‐Wellenfunktionen darzustellen ist sehr schwierig, da sie sich immer ...Abb. 9.2 Orbitalüberlappung und Spinpaarung zweier Elektronen in kollinearen p‐O...Abb. 9.3 Eine π ‐Bindung entsteht durch Überlappung und Spinpaarung zweier p‐Orbi...Abb. 9.4 Die Bindungssituation in N 2: Es gibt eine σ‐ und zwei π ‐Bindungen. Die ...Abb. 9.5 Eine erste Annäherung an die VB‐Beschreibung der Bindung im H 2O‐Molekül...Abb. 9.6 Ein sp 3‐Hybridorbital, das aus der Superposition von s‐ und p‐Orbitalen...Abb. 9.7 Jedes sp 3‐Hybridorbital geht eine σ‐Bindung durch Überlappung mit einem...Abb. 9.8 (a) Die drei äquivalenten sp 2‐Hybridorbitale, die aus der Mischung eine...Abb. 9.9 Die Doppelbindung im Ethen; nur die π ‐Bindung ist explizit gezeigt.Abb. 9.10 Die Dreifachbindung im Ethin; nur die π ‐Bindungen sind explizit gezeig...Abb. 9.11 (a) Die Amplitude des bindenden Molekülorbitals im Wasserstoffmolekül‐...Abb. 9.12 Die Einhüllenden mit konstanter Amplitude, die sich aus der Wellenfunk...Abb. 9.13 Die Einhüllenden mit konstanter Amplitude, die sich aus der Wellenfunk...Abb. 9.14 Die Elektronenverteilung, die man aus dem Quadrat der Wellenfunktion a...Abb. 9.15 Die Abhängigkeit der Integrale (a) S , (b) j und k vom Kernabstand, jew...Abb. 9.16 Die berechnete Potenzialkurve eines Wasserstoffmolekül‐Ions zeigt die ...Abb. 9.17 Eine Darstellung der konstruktiven Interferenz bei der Überlappung zwe...Abb. 9.18 Eine Darstellung der destruktiven Interferenz bei der Überlappung zwei...Abb. 9.19 (a) Die Amplitude des antibindenden Molekülorbitals in 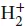 in einer Eben...Abb. 9.20 Die Elektronendichte, die man aus dem Quadrat der in Abb. 9.19 gezeigt...Abb. 9.21 Eine teilweise Erklärung der Ursache für bindende und antibindende Eff...Abb. 9.22 Die Parität eines Orbitals ist gerade (g), wenn seine Amplitude bei ei...Abb. 9.23 Ein MO‐Energieniveaudiagramm für die Orbitale, die aus der Überlappung...Abb. 9.24 Die Grundzustandskonfiguration des hypothetischen Vierelektronenmolekü...Abb. 9.25 In der MO‐Theorie werden σ‐Orbitale aus allen vorhandenen Atomorbitale...Abb. 9.26 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.27 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.28 (a) Wenn zwei Orbitale zu weit voneinander entfernten Atomen gehören, ...Abb. 9.29 Die Variation des Überlappungsintegrals S zwischen zwei Wasserstofforb...Abb. 9.30 In dieser Orientierung ist die Überlappung des p‐Orbitals mit dem s‐Or...Abb. 9.31 Wie im Text erwähnt, ist die Energieseparation der 1 π u‐ und 1 π g‐Orbita...Abb. 9.32 Das MO‐Energieniveaudiagramm für homoatomare zweiatomige Moleküle. Die...Abb. 9.33 Die Variation der Orbitalenergien von homoatomaren zweiatomigen Molekü...Abb. 9.34 Ein alternatives MO‐Energieniveaudiagramm für homoatomare zweiatomige ...Abb. 9.35 Das ankommende Photon trägt die Energie h ν , eine Energie I iwird benöt...Abb. 9.36 Ein Photoelektronenspektrometer besteht aus einer Quelle für ionisiere...Abb. 9.37 Das UV‐Photoelektronenspektrum von N 2, das mithilfe von He(I)‐Strahlun...Abb. 9.38 Die Elektronendichte in einem HF‐Molekül, das mithilfe einer der in Ab...Abb. 9.39 Illustration der Vorgehensweise zur Abschätzung des Coulomb‐Integrals ...Abb. 9.40 Die näherungsweise bestimmten Energien für die Coulomb‐Integrale α im ...Abb. 9.41 Die Abhängigkeit der Energien von Molekülorbitalen von der Energiediff...Abb. A1 Das MO‐Energieniveaudiagramm von NO.Abb. 9.42 Die Hückel‐MO‐Energieniveaus von Ethen. Im Grundzustand besetzen zwei ...Abb. 9.43 Die Hückel‐MO‐Energieniveaus von Butadien und die Draufsicht auf die z...Abb. 9.44 Das Gerüst der σ‐Bindungen in Benzol entsteht durch die Überlappung de...Abb. 9.45 Die Hückel‐π‐Orbitale von Benzol sowie die zugehörigen Energieniveaus....Abb. 9.46 Das Produkt zweier Gaußfunktionen (rote Linien) ist selbst wieder eine...Abb. 9.47 Verschiedene Darstellungen einer Fläche gleicher Elektronendichte von ...Abb. 9.48 Elektrostatische Potenzialfläche von Ethanol. Das Molekül hat dieselbe...
in einer Eben...Abb. 9.20 Die Elektronendichte, die man aus dem Quadrat der in Abb. 9.19 gezeigt...Abb. 9.21 Eine teilweise Erklärung der Ursache für bindende und antibindende Eff...Abb. 9.22 Die Parität eines Orbitals ist gerade (g), wenn seine Amplitude bei ei...Abb. 9.23 Ein MO‐Energieniveaudiagramm für die Orbitale, die aus der Überlappung...Abb. 9.24 Die Grundzustandskonfiguration des hypothetischen Vierelektronenmolekü...Abb. 9.25 In der MO‐Theorie werden σ‐Orbitale aus allen vorhandenen Atomorbitale...Abb. 9.26 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.27 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.28 (a) Wenn zwei Orbitale zu weit voneinander entfernten Atomen gehören, ...Abb. 9.29 Die Variation des Überlappungsintegrals S zwischen zwei Wasserstofforb...Abb. 9.30 In dieser Orientierung ist die Überlappung des p‐Orbitals mit dem s‐Or...Abb. 9.31 Wie im Text erwähnt, ist die Energieseparation der 1 π u‐ und 1 π g‐Orbita...Abb. 9.32 Das MO‐Energieniveaudiagramm für homoatomare zweiatomige Moleküle. Die...Abb. 9.33 Die Variation der Orbitalenergien von homoatomaren zweiatomigen Molekü...Abb. 9.34 Ein alternatives MO‐Energieniveaudiagramm für homoatomare zweiatomige ...Abb. 9.35 Das ankommende Photon trägt die Energie h ν , eine Energie I iwird benöt...Abb. 9.36 Ein Photoelektronenspektrometer besteht aus einer Quelle für ionisiere...Abb. 9.37 Das UV‐Photoelektronenspektrum von N 2, das mithilfe von He(I)‐Strahlun...Abb. 9.38 Die Elektronendichte in einem HF‐Molekül, das mithilfe einer der in Ab...Abb. 9.39 Illustration der Vorgehensweise zur Abschätzung des Coulomb‐Integrals ...Abb. 9.40 Die näherungsweise bestimmten Energien für die Coulomb‐Integrale α im ...Abb. 9.41 Die Abhängigkeit der Energien von Molekülorbitalen von der Energiediff...Abb. A1 Das MO‐Energieniveaudiagramm von NO.Abb. 9.42 Die Hückel‐MO‐Energieniveaus von Ethen. Im Grundzustand besetzen zwei ...Abb. 9.43 Die Hückel‐MO‐Energieniveaus von Butadien und die Draufsicht auf die z...Abb. 9.44 Das Gerüst der σ‐Bindungen in Benzol entsteht durch die Überlappung de...Abb. 9.45 Die Hückel‐π‐Orbitale von Benzol sowie die zugehörigen Energieniveaus....Abb. 9.46 Das Produkt zweier Gaußfunktionen (rote Linien) ist selbst wieder eine...Abb. 9.47 Verschiedene Darstellungen einer Fläche gleicher Elektronendichte von ...Abb. 9.48 Elektrostatische Potenzialfläche von Ethanol. Das Molekül hat dieselbe...
11 Kapitel 10Abb. 10.1 Einige Symmetrieelemente eines Würfels. Die zweizähligen, dreizähligen...Abb. 10.2 (a) Ein NH 3-Molekül enthält eine dreizählige Achse ( C 3), (b) ein H 2O-M...Abb. 10.3 Das H 2O-Molekül enthält zwei Spiegelebenen. Beide sind vertikal (d. h....Abb. 10.4 Diederebenen (σ d) liegen in der Winkelhalbierenden zwischen den zur Ha...Abb. 10.5 Ein regelmäßiges Oktaeder enthält ein Inversionszentrum i .Abb. 10.6 (a) Ein CH 4-Molekül besitzt eine vierzählige Drehspiegelachse S 4: Das ...Abb. 10.7 Schema zur Bestimmung der Punktgruppe eines Moleküls. Man beginnt oben...Abb. 10.8 Eine Zusammenfassung der Formen, die den unterschiedlichen Punktgruppe...Abb. 10.9 Die Existenz einer zweizähligen Achse und einer horizontalen Spiegeleb...Abb. 10.10 (a) Tetraedrische, (b) oktaedrische und (c) ikosaedrische Moleküle si...Abb. 10.11 Strukturen, die zu den Punktgruppen (a) T und (b) O führen. Die Exist...Abb. 10.12 Die Form eines Objekts, das zur Gruppe T hgehört.Abb. 10.13 Manche Symmetrieelemente folgen aus anderen Symmetrieelementen der Gr...Abb. 10.14 Zwei Spiegelungen an zueinander senkrechten Spiegelebenen σ vund 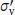 si...Abb. 10.15 Symmetrieoperationen der gleichen Klasse stehen durch Symmetrieoperat...Abb. 10.16 (a) Wenn die Symmetrieoperationen
si...Abb. 10.15 Symmetrieoperationen der gleichen Klasse stehen durch Symmetrieoperat...Abb. 10.16 (a) Wenn die Symmetrieoperationen 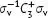 nacheinander in der Reihenfolge
nacheinander in der Reihenfolge 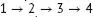 ...Abb. 10.17 Die fünf p-Orbitale (drei davon liegen am Schwefelstom und je eines a...Abb. 10.18 Zwei symmetrieadaptierte Linearkombinationen der Basisorbitale von Sa...Abb. 10.19 Ein p x-Orbital am Zentralatom eines C 2v-Moleküls und die Symmetrieele...Abb. 10.20 Die gezeigten Orbitale besitzen unterschiedliche Symmetrie bezüglich ...Abb. 10.21 Die drei H1s-Orbitale, die in einem C 3v-Molekül wie NH 3zur Konstrukt...Abb. 10.22 Eine symmetrieadaptierte Linearkombination der beiden O2p x-Orbitale i...Abb. 10.23 Eine quadratische Vertiefung kann der Punktgruppe C 4zugeordnet werde...Abb. 10.24 (a) Nur wenn der Integrand bei jeder Symmetrieoperation einer Gruppe ...Abb. 10.25 Das Integral der Funktion f = x, y über den gelb schattierten Bereich...Abb. 10.26 Die beiden O2p x-Atomorbitale in NO 2(Punktgruppe C 2v) können als Basi...Abb. 10.27 Die drei H1s-Atomorbitale in NH 3(Punktgruppe C 3v) können als Basis z...
...Abb. 10.17 Die fünf p-Orbitale (drei davon liegen am Schwefelstom und je eines a...Abb. 10.18 Zwei symmetrieadaptierte Linearkombinationen der Basisorbitale von Sa...Abb. 10.19 Ein p x-Orbital am Zentralatom eines C 2v-Moleküls und die Symmetrieele...Abb. 10.20 Die gezeigten Orbitale besitzen unterschiedliche Symmetrie bezüglich ...Abb. 10.21 Die drei H1s-Orbitale, die in einem C 3v-Molekül wie NH 3zur Konstrukt...Abb. 10.22 Eine symmetrieadaptierte Linearkombination der beiden O2p x-Orbitale i...Abb. 10.23 Eine quadratische Vertiefung kann der Punktgruppe C 4zugeordnet werde...Abb. 10.24 (a) Nur wenn der Integrand bei jeder Symmetrieoperation einer Gruppe ...Abb. 10.25 Das Integral der Funktion f = x, y über den gelb schattierten Bereich...Abb. 10.26 Die beiden O2p x-Atomorbitale in NO 2(Punktgruppe C 2v) können als Basi...Abb. 10.27 Die drei H1s-Atomorbitale in NH 3(Punktgruppe C 3v) können als Basis z...
12 Kapitel 11Abb. 11.1 Bei der Raman‐Spektroskopie wird ein einfallendes Photon von einem Mol...Abb. 11.2 (a) Wenn ein 1s-Elektron in ein 2s-Orbital übergeht, findet eine sphär...Abb. 11.3 Zur Herleitung des Lambert-Beer'schen Gesetzes stellen wir uns die Pro...Abb. 11.4 Der integrale Absorptionskoeffizient eines Übergangs ist gleich der Fl...Abb. 11.5 Die Gaußform einer Doppler-verbreiterten Spektrallinie spiegelt die Ma...Abb. T1Abb. 11.6 Ein typisches Absorptionsspektrometer. Der Strahl läuft abwechselnd du...Abb. 11.7 Ein Synchrotronspeicherring. Die aus dem Linearbeschleuniger über das ...Abb. 11.8 Ein polychromatischer Lichtstrahl wird durch ein Beugungsgitter in die...Abb. 11.9 Ein Michelson-Interferometer. Der Strahlteiler zerlegt den einfallende...Abb. 11.10 Dieses Interferogramm entsteht durch die Veränderung der Weglängendif...Abb. 11.11 Das Interferogramm, das aus den in Beispiel 11.2 gegebenen Daten bere...Abb. 11.12 Die Fourier-Transformation des Interferogramms aus Abb. 11.11. Die Os...Abb. 11.13 Das Interferogramm, das aus den in Selbsttest 11.2 gegebenen Daten be...Abb. 11.14 Eine typische Anordnung für die Raman-Spektroskopie. Ein Laserstrahl ...Abb. A1 Das Rotationsspektrum des Orionnebels mit den spektralen Fingerabdrücken...Abb. 11.15 Die Definition des Trägheitsmoments. In diesem Molekül sind drei iden...Abb. 11.16 Die Rotationsniveaus eines linearen oder sphärischen Kreisels. Der Ab...Abb. 11.17 Die Bedeutung der Quantenzahl K . (a) Für 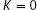 besitzt das Molekül keinen...Abb. 11.18 Die Bedeutung der Quantenzahl
besitzt das Molekül keinen...Abb. 11.18 Die Bedeutung der Quantenzahl 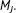 (a) Wenn
(a) Wenn 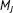 nahe dem Maximalwert J ist...Abb. 11.19 Der Einfluss der Rotation auf ein Molekül. Die Zentrifugalkraft aufgr...Abb. 11.20 Für einen stationären Beobachter erscheint ein rotierendes polares Mo...Abb. 11.21 Wenn ein Photon von einem Molekül absorbiert wird, bleibt der Drehimp...Abb. 11.22 Der Einfluss eines elektrischen Felds auf das Energieniveau mit J = 7...Abb. 11.23 Die Rotationsniveaus eines linearen Kreisels, die durch die Auswahlre...Abb. 11.24 Ein elektrisches Feld ℰ bewirkt eine Verzerrung eines Moleküls, welch...Abb. 11.25 Die von einem elektrischen Feld in einem Molekül induzierte Verzerrun...Abb. 11.26 Die Rotationsniveaus eines linearen Kreisels und die nach der Auswahl...Abb. 11.27 Die Symmetrie von Rotationswellenfunktionen (aus Gründen der Anschaul...Abb. 11.28 Das Raman-Rotationsspektrum eines zweiatomigen Moleküls aus zwei iden...Abb. 11.29 Die Vertauschung zweier identischer Fermionen-Kerne führt zu einem Vo...Abb. 11.30 In der Nähe des Minimums lässt sich die Potenzialkurve eines Moleküls...Abb. 11.31 Die Kraftkonstante ist ein Maß für die Krümmung der potenziellen Ener...Abb. 11.32 Die Dissoziationsenergie
nahe dem Maximalwert J ist...Abb. 11.19 Der Einfluss der Rotation auf ein Molekül. Die Zentrifugalkraft aufgr...Abb. 11.20 Für einen stationären Beobachter erscheint ein rotierendes polares Mo...Abb. 11.21 Wenn ein Photon von einem Molekül absorbiert wird, bleibt der Drehimp...Abb. 11.22 Der Einfluss eines elektrischen Felds auf das Energieniveau mit J = 7...Abb. 11.23 Die Rotationsniveaus eines linearen Kreisels, die durch die Auswahlre...Abb. 11.24 Ein elektrisches Feld ℰ bewirkt eine Verzerrung eines Moleküls, welch...Abb. 11.25 Die von einem elektrischen Feld in einem Molekül induzierte Verzerrun...Abb. 11.26 Die Rotationsniveaus eines linearen Kreisels und die nach der Auswahl...Abb. 11.27 Die Symmetrie von Rotationswellenfunktionen (aus Gründen der Anschaul...Abb. 11.28 Das Raman-Rotationsspektrum eines zweiatomigen Moleküls aus zwei iden...Abb. 11.29 Die Vertauschung zweier identischer Fermionen-Kerne führt zu einem Vo...Abb. 11.30 In der Nähe des Minimums lässt sich die Potenzialkurve eines Moleküls...Abb. 11.31 Die Kraftkonstante ist ein Maß für die Krümmung der potenziellen Ener...Abb. 11.32 Die Dissoziationsenergie 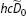 eines Moleküls und die Energie
eines Moleküls und die Energie 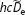 am Minimu...Abb. 11.33 Das Morse-Potenzial gibt den allgemeinen Verlauf einer typischen Pote...Abb. 11.34 Die Dissoziationsenergie ist die Summe aller Abstände der Schwingungs...Abb. 11.35 Die Fläche unter der Auftragung der Wellenzahl der Übergänge gegen di...Abb. 11.36 Die Birge-Sponer-Auftragung zu Beispiel 11.8. Die Fläche wird durch A...Abb. 11.37 Ein hochaufgelöstes Rotationsschwingungsspektrum von HCl. Die Linien ...Abb. 11.38 Die Entstehung des P-, Q- und R-Zweigs in einem Rotationsschwingungss...Abb. 11.39 Das Verfahren der Kombinationsdifferenzen verwendet die Tatsache, das...Abb. 11.40 Die Entstehung des O-, Q- und S-Zweigs im Raman-Rotationsschwingungss...Abb. 11.41 Die Struktur einer Bande im Raman-Schwingungsspektrum (die Stokes-Lin...Abb. 11.42 (a) Zur Angabe der Orientierung eines linearen Moleküls sind zwei Win...Abb. 11.43 Die vier Normalschwingungen von CO 2. Die Frequenzen der beiden senkre...Abb. 11.44 Die drei Normalschwingungen von H 2O. Die Schwingung
am Minimu...Abb. 11.33 Das Morse-Potenzial gibt den allgemeinen Verlauf einer typischen Pote...Abb. 11.34 Die Dissoziationsenergie ist die Summe aller Abstände der Schwingungs...Abb. 11.35 Die Fläche unter der Auftragung der Wellenzahl der Übergänge gegen di...Abb. 11.36 Die Birge-Sponer-Auftragung zu Beispiel 11.8. Die Fläche wird durch A...Abb. 11.37 Ein hochaufgelöstes Rotationsschwingungsspektrum von HCl. Die Linien ...Abb. 11.38 Die Entstehung des P-, Q- und R-Zweigs in einem Rotationsschwingungss...Abb. 11.39 Das Verfahren der Kombinationsdifferenzen verwendet die Tatsache, das...Abb. 11.40 Die Entstehung des O-, Q- und S-Zweigs im Raman-Rotationsschwingungss...Abb. 11.41 Die Struktur einer Bande im Raman-Schwingungsspektrum (die Stokes-Lin...Abb. 11.42 (a) Zur Angabe der Orientierung eines linearen Moleküls sind zwei Win...Abb. 11.43 Die vier Normalschwingungen von CO 2. Die Frequenzen der beiden senkre...Abb. 11.44 Die drei Normalschwingungen von H 2O. Die Schwingung 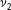 ist hauptsächli...Abb. 11.45 Die Definition der Ebenen, die zur Bestimmung des Depolarisationsgrad...Abb. A1 Die rote Linie zeigt die (hypothetische) Intensität der von der Erde in ...Abb. A2 Durchschnittliche Änderung der Oberflächentemperatur der Erde von 1850 b...Abb. 11.46 Die Verschiebungen der Atome in H 2O und die Symmetrieelemente, die zu...Abb. 11.47 Die Normalschwingungsmoden von BF 3.Abb. 11.48 Elektronische Absorptionsspektren im sichtbaren Bereich. (a) Das Spek...Abb. 11.49 Das Symbol + (symmetrisch) oder − (antisymmetrisch) an einem Termsymb...Abb. 11.50 In einem linearen Molekül hängt das Molekülorbital vom Azimutalwinkel...Abb. 11.51 Die Kopplung von Spin- und Bahndrehimpulsen in einem linearen Molekül...Abb. 11.52 d–d-Übergänge sind paritätsverboten, da es sich dabei um g–g-Übergäng...Abb. 11.53 Nach dem Franck-Condon-Prinzip findet der intensivste Übergang aus de...Abb. 11.54 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.55 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.56 Der Franck-Condon-Faktor für die Anordnung aus Beispiel 11.12.Abb. 11.57 Die Modellwellenfunktionen aus Selbsttest 11.12.Abb. 11.58 Wenn sich die Rotationskonstanten eines zweiatomigen Moleküls in den ...Abb. 11.59 Die Klassifikation der d-Orbitale in einer oktaedrischen Umgebung. Di...Abb. 11.60 Das elektronische Absorptionsspektrum von [Ti(OH 2) 6] 3+in wässriger L...Abb. 11.61 Eine C=C-Doppelbindung ist ein Chromophor. Einer ihrer wichtigen Über...Abb. 11.62 Eine Carbonylgruppe (>C=O) ist ein Chromophor, da ein Elektron aus ei...Abb. 11.63 Die empirische Unterscheidung zwischen Fluoreszenz und Phosphoreszenz...Abb. 11.64 Der Mechanismus der Fluoreszenz. Nach der Anregung werden die angereg...Abb. 11.65 Ein Absorptionsspektrum (blaue Linie) zeigt eine Schwingungsstruktur,...Abb. 11.66 Das Lösungsmittel kann das Fluoreszenzspektrum relativ zum Absorption...Abb. 11.67 Der Mechanismus der Phosphoreszenz. Der entscheidende Schritt ist das...Abb. 11.68 Ein Jablonski-Diagramm (hier für Naphthalin) ist eine vereinfachte Da...Abb. 11.69 Wenn ein Übergang in ungebundene Zustände des elektronisch angeregten...Abb. 11.70 Wenn sich die Potenzialkurven eines gebundenen und eines dissoziative...Abb. 11.71 Die Übergänge in einem Vier-Niveau-Laser. Der Laserübergang endet in ...Abb. 11.72 Die Übergänge in einem Neodym-Laser.Abb. Z1 Die Abhängigkeit der drei Komponenten des Dipolmoments von den Winkeln θ ...Abb. Z2 Die Orientierung der Komponenten des Dipolmoments μx , μy und μz in Relat...Abb. 11.73 Die parabolische Kurve zu Aufgabe L11.1.8b.Abb. 11.74 Das elektronische Absorptionsspektrum von Azomethan (zu Aufgabe S11.1...Abb. 11.75 Das Photoelektronenspektrum von HBr (zu Aufgabe S11.6.5).Abb. 11.76 Die UV-Vis-Absorptionsspektren einiger Aminosäuren (zu Aufgabe S11.6....Abb. 11.77 Das Fluoreszenzspektrum (A) von Benzophenon und das Phosphoreszenzspe...Abb. 11.78 Das UV-Absorptionsspektrum von SO 2(zu Aufgabe A11.11).
ist hauptsächli...Abb. 11.45 Die Definition der Ebenen, die zur Bestimmung des Depolarisationsgrad...Abb. A1 Die rote Linie zeigt die (hypothetische) Intensität der von der Erde in ...Abb. A2 Durchschnittliche Änderung der Oberflächentemperatur der Erde von 1850 b...Abb. 11.46 Die Verschiebungen der Atome in H 2O und die Symmetrieelemente, die zu...Abb. 11.47 Die Normalschwingungsmoden von BF 3.Abb. 11.48 Elektronische Absorptionsspektren im sichtbaren Bereich. (a) Das Spek...Abb. 11.49 Das Symbol + (symmetrisch) oder − (antisymmetrisch) an einem Termsymb...Abb. 11.50 In einem linearen Molekül hängt das Molekülorbital vom Azimutalwinkel...Abb. 11.51 Die Kopplung von Spin- und Bahndrehimpulsen in einem linearen Molekül...Abb. 11.52 d–d-Übergänge sind paritätsverboten, da es sich dabei um g–g-Übergäng...Abb. 11.53 Nach dem Franck-Condon-Prinzip findet der intensivste Übergang aus de...Abb. 11.54 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.55 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.56 Der Franck-Condon-Faktor für die Anordnung aus Beispiel 11.12.Abb. 11.57 Die Modellwellenfunktionen aus Selbsttest 11.12.Abb. 11.58 Wenn sich die Rotationskonstanten eines zweiatomigen Moleküls in den ...Abb. 11.59 Die Klassifikation der d-Orbitale in einer oktaedrischen Umgebung. Di...Abb. 11.60 Das elektronische Absorptionsspektrum von [Ti(OH 2) 6] 3+in wässriger L...Abb. 11.61 Eine C=C-Doppelbindung ist ein Chromophor. Einer ihrer wichtigen Über...Abb. 11.62 Eine Carbonylgruppe (>C=O) ist ein Chromophor, da ein Elektron aus ei...Abb. 11.63 Die empirische Unterscheidung zwischen Fluoreszenz und Phosphoreszenz...Abb. 11.64 Der Mechanismus der Fluoreszenz. Nach der Anregung werden die angereg...Abb. 11.65 Ein Absorptionsspektrum (blaue Linie) zeigt eine Schwingungsstruktur,...Abb. 11.66 Das Lösungsmittel kann das Fluoreszenzspektrum relativ zum Absorption...Abb. 11.67 Der Mechanismus der Phosphoreszenz. Der entscheidende Schritt ist das...Abb. 11.68 Ein Jablonski-Diagramm (hier für Naphthalin) ist eine vereinfachte Da...Abb. 11.69 Wenn ein Übergang in ungebundene Zustände des elektronisch angeregten...Abb. 11.70 Wenn sich die Potenzialkurven eines gebundenen und eines dissoziative...Abb. 11.71 Die Übergänge in einem Vier-Niveau-Laser. Der Laserübergang endet in ...Abb. 11.72 Die Übergänge in einem Neodym-Laser.Abb. Z1 Die Abhängigkeit der drei Komponenten des Dipolmoments von den Winkeln θ ...Abb. Z2 Die Orientierung der Komponenten des Dipolmoments μx , μy und μz in Relat...Abb. 11.73 Die parabolische Kurve zu Aufgabe L11.1.8b.Abb. 11.74 Das elektronische Absorptionsspektrum von Azomethan (zu Aufgabe S11.1...Abb. 11.75 Das Photoelektronenspektrum von HBr (zu Aufgabe S11.6.5).Abb. 11.76 Die UV-Vis-Absorptionsspektren einiger Aminosäuren (zu Aufgabe S11.6....Abb. 11.77 Das Fluoreszenzspektrum (A) von Benzophenon und das Phosphoreszenzspe...Abb. 11.78 Das UV-Absorptionsspektrum von SO 2(zu Aufgabe A11.11).
Читать дальше

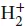 in einer Eben...Abb. 9.20 Die Elektronendichte, die man aus dem Quadrat der in Abb. 9.19 gezeigt...Abb. 9.21 Eine teilweise Erklärung der Ursache für bindende und antibindende Eff...Abb. 9.22 Die Parität eines Orbitals ist gerade (g), wenn seine Amplitude bei ei...Abb. 9.23 Ein MO‐Energieniveaudiagramm für die Orbitale, die aus der Überlappung...Abb. 9.24 Die Grundzustandskonfiguration des hypothetischen Vierelektronenmolekü...Abb. 9.25 In der MO‐Theorie werden σ‐Orbitale aus allen vorhandenen Atomorbitale...Abb. 9.26 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.27 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.28 (a) Wenn zwei Orbitale zu weit voneinander entfernten Atomen gehören, ...Abb. 9.29 Die Variation des Überlappungsintegrals S zwischen zwei Wasserstofforb...Abb. 9.30 In dieser Orientierung ist die Überlappung des p‐Orbitals mit dem s‐Or...Abb. 9.31 Wie im Text erwähnt, ist die Energieseparation der 1 π u‐ und 1 π g‐Orbita...Abb. 9.32 Das MO‐Energieniveaudiagramm für homoatomare zweiatomige Moleküle. Die...Abb. 9.33 Die Variation der Orbitalenergien von homoatomaren zweiatomigen Molekü...Abb. 9.34 Ein alternatives MO‐Energieniveaudiagramm für homoatomare zweiatomige ...Abb. 9.35 Das ankommende Photon trägt die Energie h ν , eine Energie I iwird benöt...Abb. 9.36 Ein Photoelektronenspektrometer besteht aus einer Quelle für ionisiere...Abb. 9.37 Das UV‐Photoelektronenspektrum von N 2, das mithilfe von He(I)‐Strahlun...Abb. 9.38 Die Elektronendichte in einem HF‐Molekül, das mithilfe einer der in Ab...Abb. 9.39 Illustration der Vorgehensweise zur Abschätzung des Coulomb‐Integrals ...Abb. 9.40 Die näherungsweise bestimmten Energien für die Coulomb‐Integrale α im ...Abb. 9.41 Die Abhängigkeit der Energien von Molekülorbitalen von der Energiediff...Abb. A1 Das MO‐Energieniveaudiagramm von NO.Abb. 9.42 Die Hückel‐MO‐Energieniveaus von Ethen. Im Grundzustand besetzen zwei ...Abb. 9.43 Die Hückel‐MO‐Energieniveaus von Butadien und die Draufsicht auf die z...Abb. 9.44 Das Gerüst der σ‐Bindungen in Benzol entsteht durch die Überlappung de...Abb. 9.45 Die Hückel‐π‐Orbitale von Benzol sowie die zugehörigen Energieniveaus....Abb. 9.46 Das Produkt zweier Gaußfunktionen (rote Linien) ist selbst wieder eine...Abb. 9.47 Verschiedene Darstellungen einer Fläche gleicher Elektronendichte von ...Abb. 9.48 Elektrostatische Potenzialfläche von Ethanol. Das Molekül hat dieselbe...
in einer Eben...Abb. 9.20 Die Elektronendichte, die man aus dem Quadrat der in Abb. 9.19 gezeigt...Abb. 9.21 Eine teilweise Erklärung der Ursache für bindende und antibindende Eff...Abb. 9.22 Die Parität eines Orbitals ist gerade (g), wenn seine Amplitude bei ei...Abb. 9.23 Ein MO‐Energieniveaudiagramm für die Orbitale, die aus der Überlappung...Abb. 9.24 Die Grundzustandskonfiguration des hypothetischen Vierelektronenmolekü...Abb. 9.25 In der MO‐Theorie werden σ‐Orbitale aus allen vorhandenen Atomorbitale...Abb. 9.26 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.27 Schematische Darstellung der Zusammensetzung von bindenden und antibin...Abb. 9.28 (a) Wenn zwei Orbitale zu weit voneinander entfernten Atomen gehören, ...Abb. 9.29 Die Variation des Überlappungsintegrals S zwischen zwei Wasserstofforb...Abb. 9.30 In dieser Orientierung ist die Überlappung des p‐Orbitals mit dem s‐Or...Abb. 9.31 Wie im Text erwähnt, ist die Energieseparation der 1 π u‐ und 1 π g‐Orbita...Abb. 9.32 Das MO‐Energieniveaudiagramm für homoatomare zweiatomige Moleküle. Die...Abb. 9.33 Die Variation der Orbitalenergien von homoatomaren zweiatomigen Molekü...Abb. 9.34 Ein alternatives MO‐Energieniveaudiagramm für homoatomare zweiatomige ...Abb. 9.35 Das ankommende Photon trägt die Energie h ν , eine Energie I iwird benöt...Abb. 9.36 Ein Photoelektronenspektrometer besteht aus einer Quelle für ionisiere...Abb. 9.37 Das UV‐Photoelektronenspektrum von N 2, das mithilfe von He(I)‐Strahlun...Abb. 9.38 Die Elektronendichte in einem HF‐Molekül, das mithilfe einer der in Ab...Abb. 9.39 Illustration der Vorgehensweise zur Abschätzung des Coulomb‐Integrals ...Abb. 9.40 Die näherungsweise bestimmten Energien für die Coulomb‐Integrale α im ...Abb. 9.41 Die Abhängigkeit der Energien von Molekülorbitalen von der Energiediff...Abb. A1 Das MO‐Energieniveaudiagramm von NO.Abb. 9.42 Die Hückel‐MO‐Energieniveaus von Ethen. Im Grundzustand besetzen zwei ...Abb. 9.43 Die Hückel‐MO‐Energieniveaus von Butadien und die Draufsicht auf die z...Abb. 9.44 Das Gerüst der σ‐Bindungen in Benzol entsteht durch die Überlappung de...Abb. 9.45 Die Hückel‐π‐Orbitale von Benzol sowie die zugehörigen Energieniveaus....Abb. 9.46 Das Produkt zweier Gaußfunktionen (rote Linien) ist selbst wieder eine...Abb. 9.47 Verschiedene Darstellungen einer Fläche gleicher Elektronendichte von ...Abb. 9.48 Elektrostatische Potenzialfläche von Ethanol. Das Molekül hat dieselbe...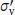 si...Abb. 10.15 Symmetrieoperationen der gleichen Klasse stehen durch Symmetrieoperat...Abb. 10.16 (a) Wenn die Symmetrieoperationen
si...Abb. 10.15 Symmetrieoperationen der gleichen Klasse stehen durch Symmetrieoperat...Abb. 10.16 (a) Wenn die Symmetrieoperationen 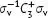 nacheinander in der Reihenfolge
nacheinander in der Reihenfolge 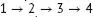 ...Abb. 10.17 Die fünf p-Orbitale (drei davon liegen am Schwefelstom und je eines a...Abb. 10.18 Zwei symmetrieadaptierte Linearkombinationen der Basisorbitale von Sa...Abb. 10.19 Ein p x-Orbital am Zentralatom eines C 2v-Moleküls und die Symmetrieele...Abb. 10.20 Die gezeigten Orbitale besitzen unterschiedliche Symmetrie bezüglich ...Abb. 10.21 Die drei H1s-Orbitale, die in einem C 3v-Molekül wie NH 3zur Konstrukt...Abb. 10.22 Eine symmetrieadaptierte Linearkombination der beiden O2p x-Orbitale i...Abb. 10.23 Eine quadratische Vertiefung kann der Punktgruppe C 4zugeordnet werde...Abb. 10.24 (a) Nur wenn der Integrand bei jeder Symmetrieoperation einer Gruppe ...Abb. 10.25 Das Integral der Funktion f = x, y über den gelb schattierten Bereich...Abb. 10.26 Die beiden O2p x-Atomorbitale in NO 2(Punktgruppe C 2v) können als Basi...Abb. 10.27 Die drei H1s-Atomorbitale in NH 3(Punktgruppe C 3v) können als Basis z...
...Abb. 10.17 Die fünf p-Orbitale (drei davon liegen am Schwefelstom und je eines a...Abb. 10.18 Zwei symmetrieadaptierte Linearkombinationen der Basisorbitale von Sa...Abb. 10.19 Ein p x-Orbital am Zentralatom eines C 2v-Moleküls und die Symmetrieele...Abb. 10.20 Die gezeigten Orbitale besitzen unterschiedliche Symmetrie bezüglich ...Abb. 10.21 Die drei H1s-Orbitale, die in einem C 3v-Molekül wie NH 3zur Konstrukt...Abb. 10.22 Eine symmetrieadaptierte Linearkombination der beiden O2p x-Orbitale i...Abb. 10.23 Eine quadratische Vertiefung kann der Punktgruppe C 4zugeordnet werde...Abb. 10.24 (a) Nur wenn der Integrand bei jeder Symmetrieoperation einer Gruppe ...Abb. 10.25 Das Integral der Funktion f = x, y über den gelb schattierten Bereich...Abb. 10.26 Die beiden O2p x-Atomorbitale in NO 2(Punktgruppe C 2v) können als Basi...Abb. 10.27 Die drei H1s-Atomorbitale in NH 3(Punktgruppe C 3v) können als Basis z...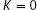 besitzt das Molekül keinen...Abb. 11.18 Die Bedeutung der Quantenzahl
besitzt das Molekül keinen...Abb. 11.18 Die Bedeutung der Quantenzahl 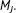 (a) Wenn
(a) Wenn 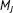 nahe dem Maximalwert J ist...Abb. 11.19 Der Einfluss der Rotation auf ein Molekül. Die Zentrifugalkraft aufgr...Abb. 11.20 Für einen stationären Beobachter erscheint ein rotierendes polares Mo...Abb. 11.21 Wenn ein Photon von einem Molekül absorbiert wird, bleibt der Drehimp...Abb. 11.22 Der Einfluss eines elektrischen Felds auf das Energieniveau mit J = 7...Abb. 11.23 Die Rotationsniveaus eines linearen Kreisels, die durch die Auswahlre...Abb. 11.24 Ein elektrisches Feld ℰ bewirkt eine Verzerrung eines Moleküls, welch...Abb. 11.25 Die von einem elektrischen Feld in einem Molekül induzierte Verzerrun...Abb. 11.26 Die Rotationsniveaus eines linearen Kreisels und die nach der Auswahl...Abb. 11.27 Die Symmetrie von Rotationswellenfunktionen (aus Gründen der Anschaul...Abb. 11.28 Das Raman-Rotationsspektrum eines zweiatomigen Moleküls aus zwei iden...Abb. 11.29 Die Vertauschung zweier identischer Fermionen-Kerne führt zu einem Vo...Abb. 11.30 In der Nähe des Minimums lässt sich die Potenzialkurve eines Moleküls...Abb. 11.31 Die Kraftkonstante ist ein Maß für die Krümmung der potenziellen Ener...Abb. 11.32 Die Dissoziationsenergie
nahe dem Maximalwert J ist...Abb. 11.19 Der Einfluss der Rotation auf ein Molekül. Die Zentrifugalkraft aufgr...Abb. 11.20 Für einen stationären Beobachter erscheint ein rotierendes polares Mo...Abb. 11.21 Wenn ein Photon von einem Molekül absorbiert wird, bleibt der Drehimp...Abb. 11.22 Der Einfluss eines elektrischen Felds auf das Energieniveau mit J = 7...Abb. 11.23 Die Rotationsniveaus eines linearen Kreisels, die durch die Auswahlre...Abb. 11.24 Ein elektrisches Feld ℰ bewirkt eine Verzerrung eines Moleküls, welch...Abb. 11.25 Die von einem elektrischen Feld in einem Molekül induzierte Verzerrun...Abb. 11.26 Die Rotationsniveaus eines linearen Kreisels und die nach der Auswahl...Abb. 11.27 Die Symmetrie von Rotationswellenfunktionen (aus Gründen der Anschaul...Abb. 11.28 Das Raman-Rotationsspektrum eines zweiatomigen Moleküls aus zwei iden...Abb. 11.29 Die Vertauschung zweier identischer Fermionen-Kerne führt zu einem Vo...Abb. 11.30 In der Nähe des Minimums lässt sich die Potenzialkurve eines Moleküls...Abb. 11.31 Die Kraftkonstante ist ein Maß für die Krümmung der potenziellen Ener...Abb. 11.32 Die Dissoziationsenergie 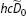 eines Moleküls und die Energie
eines Moleküls und die Energie 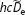 am Minimu...Abb. 11.33 Das Morse-Potenzial gibt den allgemeinen Verlauf einer typischen Pote...Abb. 11.34 Die Dissoziationsenergie ist die Summe aller Abstände der Schwingungs...Abb. 11.35 Die Fläche unter der Auftragung der Wellenzahl der Übergänge gegen di...Abb. 11.36 Die Birge-Sponer-Auftragung zu Beispiel 11.8. Die Fläche wird durch A...Abb. 11.37 Ein hochaufgelöstes Rotationsschwingungsspektrum von HCl. Die Linien ...Abb. 11.38 Die Entstehung des P-, Q- und R-Zweigs in einem Rotationsschwingungss...Abb. 11.39 Das Verfahren der Kombinationsdifferenzen verwendet die Tatsache, das...Abb. 11.40 Die Entstehung des O-, Q- und S-Zweigs im Raman-Rotationsschwingungss...Abb. 11.41 Die Struktur einer Bande im Raman-Schwingungsspektrum (die Stokes-Lin...Abb. 11.42 (a) Zur Angabe der Orientierung eines linearen Moleküls sind zwei Win...Abb. 11.43 Die vier Normalschwingungen von CO 2. Die Frequenzen der beiden senkre...Abb. 11.44 Die drei Normalschwingungen von H 2O. Die Schwingung
am Minimu...Abb. 11.33 Das Morse-Potenzial gibt den allgemeinen Verlauf einer typischen Pote...Abb. 11.34 Die Dissoziationsenergie ist die Summe aller Abstände der Schwingungs...Abb. 11.35 Die Fläche unter der Auftragung der Wellenzahl der Übergänge gegen di...Abb. 11.36 Die Birge-Sponer-Auftragung zu Beispiel 11.8. Die Fläche wird durch A...Abb. 11.37 Ein hochaufgelöstes Rotationsschwingungsspektrum von HCl. Die Linien ...Abb. 11.38 Die Entstehung des P-, Q- und R-Zweigs in einem Rotationsschwingungss...Abb. 11.39 Das Verfahren der Kombinationsdifferenzen verwendet die Tatsache, das...Abb. 11.40 Die Entstehung des O-, Q- und S-Zweigs im Raman-Rotationsschwingungss...Abb. 11.41 Die Struktur einer Bande im Raman-Schwingungsspektrum (die Stokes-Lin...Abb. 11.42 (a) Zur Angabe der Orientierung eines linearen Moleküls sind zwei Win...Abb. 11.43 Die vier Normalschwingungen von CO 2. Die Frequenzen der beiden senkre...Abb. 11.44 Die drei Normalschwingungen von H 2O. Die Schwingung 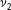 ist hauptsächli...Abb. 11.45 Die Definition der Ebenen, die zur Bestimmung des Depolarisationsgrad...Abb. A1 Die rote Linie zeigt die (hypothetische) Intensität der von der Erde in ...Abb. A2 Durchschnittliche Änderung der Oberflächentemperatur der Erde von 1850 b...Abb. 11.46 Die Verschiebungen der Atome in H 2O und die Symmetrieelemente, die zu...Abb. 11.47 Die Normalschwingungsmoden von BF 3.Abb. 11.48 Elektronische Absorptionsspektren im sichtbaren Bereich. (a) Das Spek...Abb. 11.49 Das Symbol + (symmetrisch) oder − (antisymmetrisch) an einem Termsymb...Abb. 11.50 In einem linearen Molekül hängt das Molekülorbital vom Azimutalwinkel...Abb. 11.51 Die Kopplung von Spin- und Bahndrehimpulsen in einem linearen Molekül...Abb. 11.52 d–d-Übergänge sind paritätsverboten, da es sich dabei um g–g-Übergäng...Abb. 11.53 Nach dem Franck-Condon-Prinzip findet der intensivste Übergang aus de...Abb. 11.54 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.55 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.56 Der Franck-Condon-Faktor für die Anordnung aus Beispiel 11.12.Abb. 11.57 Die Modellwellenfunktionen aus Selbsttest 11.12.Abb. 11.58 Wenn sich die Rotationskonstanten eines zweiatomigen Moleküls in den ...Abb. 11.59 Die Klassifikation der d-Orbitale in einer oktaedrischen Umgebung. Di...Abb. 11.60 Das elektronische Absorptionsspektrum von [Ti(OH 2) 6] 3+in wässriger L...Abb. 11.61 Eine C=C-Doppelbindung ist ein Chromophor. Einer ihrer wichtigen Über...Abb. 11.62 Eine Carbonylgruppe (>C=O) ist ein Chromophor, da ein Elektron aus ei...Abb. 11.63 Die empirische Unterscheidung zwischen Fluoreszenz und Phosphoreszenz...Abb. 11.64 Der Mechanismus der Fluoreszenz. Nach der Anregung werden die angereg...Abb. 11.65 Ein Absorptionsspektrum (blaue Linie) zeigt eine Schwingungsstruktur,...Abb. 11.66 Das Lösungsmittel kann das Fluoreszenzspektrum relativ zum Absorption...Abb. 11.67 Der Mechanismus der Phosphoreszenz. Der entscheidende Schritt ist das...Abb. 11.68 Ein Jablonski-Diagramm (hier für Naphthalin) ist eine vereinfachte Da...Abb. 11.69 Wenn ein Übergang in ungebundene Zustände des elektronisch angeregten...Abb. 11.70 Wenn sich die Potenzialkurven eines gebundenen und eines dissoziative...Abb. 11.71 Die Übergänge in einem Vier-Niveau-Laser. Der Laserübergang endet in ...Abb. 11.72 Die Übergänge in einem Neodym-Laser.Abb. Z1 Die Abhängigkeit der drei Komponenten des Dipolmoments von den Winkeln θ ...Abb. Z2 Die Orientierung der Komponenten des Dipolmoments μx , μy und μz in Relat...Abb. 11.73 Die parabolische Kurve zu Aufgabe L11.1.8b.Abb. 11.74 Das elektronische Absorptionsspektrum von Azomethan (zu Aufgabe S11.1...Abb. 11.75 Das Photoelektronenspektrum von HBr (zu Aufgabe S11.6.5).Abb. 11.76 Die UV-Vis-Absorptionsspektren einiger Aminosäuren (zu Aufgabe S11.6....Abb. 11.77 Das Fluoreszenzspektrum (A) von Benzophenon und das Phosphoreszenzspe...Abb. 11.78 Das UV-Absorptionsspektrum von SO 2(zu Aufgabe A11.11).
ist hauptsächli...Abb. 11.45 Die Definition der Ebenen, die zur Bestimmung des Depolarisationsgrad...Abb. A1 Die rote Linie zeigt die (hypothetische) Intensität der von der Erde in ...Abb. A2 Durchschnittliche Änderung der Oberflächentemperatur der Erde von 1850 b...Abb. 11.46 Die Verschiebungen der Atome in H 2O und die Symmetrieelemente, die zu...Abb. 11.47 Die Normalschwingungsmoden von BF 3.Abb. 11.48 Elektronische Absorptionsspektren im sichtbaren Bereich. (a) Das Spek...Abb. 11.49 Das Symbol + (symmetrisch) oder − (antisymmetrisch) an einem Termsymb...Abb. 11.50 In einem linearen Molekül hängt das Molekülorbital vom Azimutalwinkel...Abb. 11.51 Die Kopplung von Spin- und Bahndrehimpulsen in einem linearen Molekül...Abb. 11.52 d–d-Übergänge sind paritätsverboten, da es sich dabei um g–g-Übergäng...Abb. 11.53 Nach dem Franck-Condon-Prinzip findet der intensivste Übergang aus de...Abb. 11.54 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.55 (a) Wenn die Gleichgewichtsbindungslängen im elektronischen Grundzust...Abb. 11.56 Der Franck-Condon-Faktor für die Anordnung aus Beispiel 11.12.Abb. 11.57 Die Modellwellenfunktionen aus Selbsttest 11.12.Abb. 11.58 Wenn sich die Rotationskonstanten eines zweiatomigen Moleküls in den ...Abb. 11.59 Die Klassifikation der d-Orbitale in einer oktaedrischen Umgebung. Di...Abb. 11.60 Das elektronische Absorptionsspektrum von [Ti(OH 2) 6] 3+in wässriger L...Abb. 11.61 Eine C=C-Doppelbindung ist ein Chromophor. Einer ihrer wichtigen Über...Abb. 11.62 Eine Carbonylgruppe (>C=O) ist ein Chromophor, da ein Elektron aus ei...Abb. 11.63 Die empirische Unterscheidung zwischen Fluoreszenz und Phosphoreszenz...Abb. 11.64 Der Mechanismus der Fluoreszenz. Nach der Anregung werden die angereg...Abb. 11.65 Ein Absorptionsspektrum (blaue Linie) zeigt eine Schwingungsstruktur,...Abb. 11.66 Das Lösungsmittel kann das Fluoreszenzspektrum relativ zum Absorption...Abb. 11.67 Der Mechanismus der Phosphoreszenz. Der entscheidende Schritt ist das...Abb. 11.68 Ein Jablonski-Diagramm (hier für Naphthalin) ist eine vereinfachte Da...Abb. 11.69 Wenn ein Übergang in ungebundene Zustände des elektronisch angeregten...Abb. 11.70 Wenn sich die Potenzialkurven eines gebundenen und eines dissoziative...Abb. 11.71 Die Übergänge in einem Vier-Niveau-Laser. Der Laserübergang endet in ...Abb. 11.72 Die Übergänge in einem Neodym-Laser.Abb. Z1 Die Abhängigkeit der drei Komponenten des Dipolmoments von den Winkeln θ ...Abb. Z2 Die Orientierung der Komponenten des Dipolmoments μx , μy und μz in Relat...Abb. 11.73 Die parabolische Kurve zu Aufgabe L11.1.8b.Abb. 11.74 Das elektronische Absorptionsspektrum von Azomethan (zu Aufgabe S11.1...Abb. 11.75 Das Photoelektronenspektrum von HBr (zu Aufgabe S11.6.5).Abb. 11.76 Die UV-Vis-Absorptionsspektren einiger Aminosäuren (zu Aufgabe S11.6....Abb. 11.77 Das Fluoreszenzspektrum (A) von Benzophenon und das Phosphoreszenzspe...Abb. 11.78 Das UV-Absorptionsspektrum von SO 2(zu Aufgabe A11.11).










