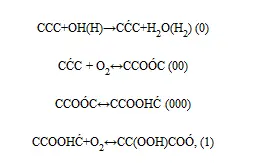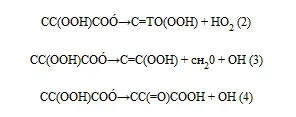4. Наблюдается ряд промежуточных продуктов конверсии топлива в зоне А – монооксид и диоксид углерода, этилен, ацетилен, метан, пропан, формальдегид и водород, профиль скорости образования и убыли которых не подвержен влиянию Т Это подтверждает справедливость предположения о зонном преобладании А и т механизмов в монофронте. Аналогичное подтверждение установлено при обнаружении ОтК в пределах монофронта разных топливных смесей.
5. Исходя из формы профиля концентрации атомов водорода (рис. 1 – 3) и кинетических данных работ [11-21] по низкотемпературному окислению углеводородов можно полагать, что механизмам А и т конверсии топлива в монофронте присущи разные по природе ведущие активные центры: у первого (автокатализ) это – радикал гидроксила, а у второго (тепловое автоускорение) – атомы водорода.
Рассмотрим далее в основных чертах химические основы механизма А предбифуркационных явлений (роста фактора S), привлекая установившееся в последнее время представление о механизме низкотемпературного окисления углеводородов [11 -21]. С ростом Р 0в диапазоне 0,001÷5 МПа стабилизируется равновесие:
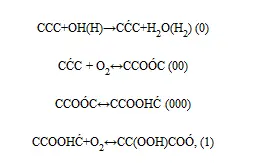
которое в зависимости от Р 0сопряжено в основных чертах со следующим продолжением:
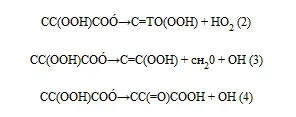
По данным работы [21] при Т 0≈ 700 К и Р 0= 10 3÷ 5МПа величина К возрастает от 10 11до 5 ∙ 10 1310 13см 3моль -1с -1. Однако при Р 0=0,1 МПа и росте температуры Т смеси от 700 до 1000 К К 1=10 13→ 5^ 10 7см 3моль -1с -1; К 2=310 5→ 5∙ 10 7см 3моль -1с -1; К 3=5∙ 10 10см 3моль -1с -1; К 4=5∙ 10 8→ 10 10см 3моль -1с -1.
Реакции (0) – (4) суммируют реакционные каналы, обуславливающие главное свойство механизма низкотемпературного окисления, который в полном виде представлен в [7-20]. Принимая во внимание, что на одной молекуле додекана размещается до пяти гидроксипероксидных групп [22] можно ожидать, что с удлинением углеродной цепи удельное количество актов разветвления может быть одним и тем же для молекул разной природы при заданной величине стехиометричного отношения а.
Температурная зависимость представленных выше кинетических параметров при 0,1 МПа, и в сумме реакций (0-000 и 1-4) обуславливает истоки отклика монофронта на изменение с 0, т 0, р и природу молекул топлива.
исходя из ОтК константы реакции (1) в диапазоне температур 700 К, , следует, что на уровне реакций (2) – (4) положительная зависимость от температуры усиливается в пределе двух порядков. Рост С 0смещает равновесия (0) – (000) и (1) в сторону перехода свободной валентности углерода на перекисный кислород, что способствует возрастанию скорости реакций (2-4) и росту температуры.
Сопоставляя температурную границу ОТК 700 К максимальной скорости убыли кислорода и пентана (рис. 4, 5 сообщении 1) и величину второго низкотемпературного максимума тепловыделения при Т 0= 344 К в пламени гексана (рис. 6) находим близкое значение 750 К. Это совпадает с наблюдениями в работе [15], в которой было установлено, что температура на выходе первого фронта в стадийных пламёнах эфира, гексана и Н-пентана одинакова и составляет 790 К. Температура Тz появления первого низкотемпературного максимума тепловыделения в пламени гексана составляет Тz1 = 450 К и близка к температуре холодного максимума в пламени пропана 520 К [2]. Принимая во внимание, что низкотемпературные максимумы в разных пламёнах одина- ково чувствительны к росту Т 0(см. табл. 1, 2 сообщение 1) и к добавкам ингибиторов можно заключить, что в случае бифронта гексана, этот максимум есть сформированный холодный монофронт, отдаленный от второго, более интенсивного. Наличие же слабого максимума тепловыделения в пропане [2] при а = 1,4 есть свидетельство зарождения и развития в этом пламени А-Т механизма.
В упомянутой выше работе Бабкин и Бунев [6] численным анализом стехиометрического пламени эфира установили, что при добавлении гидропероксида диметилового эфира (ДМЭ) в этиловый эфир, начиная с некоторого его количества возникает стадийность, что, следуя нашей терминологии, соответствует бифуркацией монофронта. С дальнейшим ростом добавки то- плива возрастает ширина разрыва, а максимум тепловыделения возрастает в первом пламени (зона А). При этом профили атомов водорода, гидроксила, атомов кислорода и оксида водорода (НО 2) одинаковы и имеют два максимума, соответственно двум стадиям. в отсутствии добавки в условиях одностадийности два максимума указанных радикалов различны.
Читать дальше