Как же взаимосвязаны изменение матрикса, нарушение работы цитоскелета и митохондрии?
Ангиотензин II вызывает изменения в процессе синтеза компонентов межклеточного матрикса, что влияет и на цитоскелет клетки. Известно, что если эндотелиальные клетки окружены более жестким матриксом, то их микротрубочки образуются дольше, правда, получаются в итоге более прочными. Клетки, находящиеся на менее жестком матриксе, образуют не такие прочные микротрубочки, но и растут они быстрее 95. Микротрубочки, в свою очередь, очень важны для функционирования митохондрий: при их «разборке» митохондрии теряют свою подвижность. Взаимодействие митохондрий с более прочными трубочками ухудшает их структуру и нарушает энергетическую систему в клетке 96.
Еще один из механизмов нарушения цитоскелета клетки, помимо действия ангиотензина II, – регуляция уже упомянутым цитокином TGF-β [16] Также TGF-β может вызывать нарушение работы митохондрий. Он останавливает рост эпителиальных клеток легких и «состаривает» их, снижая активность IV митохондриального комплекса – цитохром c-оксидазы. Цитохром с-оксидаза замыкает дыхательную цепь, перенося электроны на кислород. Снижение ее активности приводит к утечке электронов и образованию АФК. Окислительный стресс может быть потенциальной причиной некоторых старческих заболеваний 97 , 98 , 99 .
реорганизации актиновых филаментов. Вызывая перегруппировки актиновых филаментов, он влияет на рост и дифференцировку клеток, так как в ядре запускается действие определенных транскрипционных факторов 84, 85, 86(рис. 8).
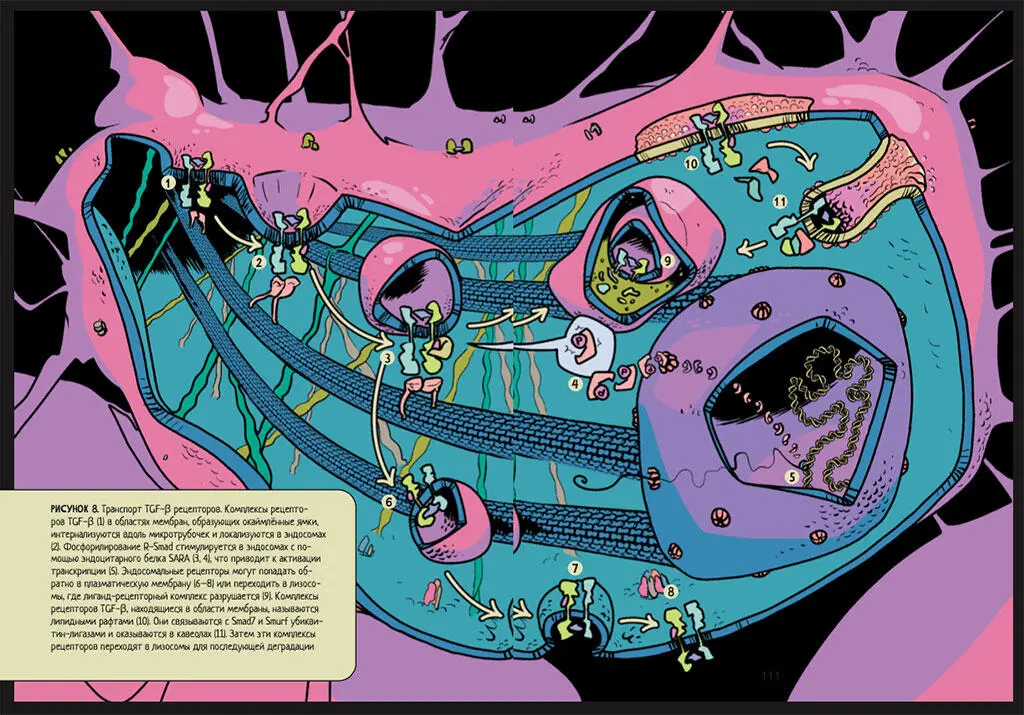
Рисунок 8.Транспорт TGF-β рецепторов. Комплексы рецепторов TGF-β (1) в областях мембран, образующих окаймленные ямки, интернализуются вдоль микротрубочек и локализуются в эндосомах (2). Фосфорилирование R-Smad стимулируется в эндосомах с помощью эндоцитарного белка SARA (3, 4), что приводит к активации транскрипции (5). Эндосомальные рецепторы могут попадать обратно в плазматическую мембрану (6–8) или переходить в лизосомы, где лиганд-рецепторный комплекс разрушается (9). Комплексы рецепторов TGF-β, находящиеся в области мембраны, называются липидными рафтами (10). Они связываются с Smad7 и Smurf убиквитин-лигазами и оказываются в кавеолах (11). Затем эти комплексы рецепторов переходят в лизосомы для последующей деградации.
Аиша Мелуан и ее коллеги показали, что белок SPARC [17] SPARC (Secreted Protein Acidic and Rich in Cysteine, «секретируемый кислый белок, богатый цистеином») также известен как остеонектин и представляет собой кальций-связывающий матриксно-клеточный гликопротеин 101 .
влияет одновременно и на изменения состава внеклеточного матрикса, и на функцию митохондрий в мышечных клетках 100.
В мышцах SPARC синтезируется при строительстве или заживлении мышечной ткани. Еще он обладает способностью связываться с коллагенами разных типов, за счет чего влияет на перестройку и формирование внеклеточного матрикса 102.
Что касается митохондрий, то этот белок влияет на их развитие путем взаимодействия с индуктором биогенеза митохондрий – белком AMPK (Adenosine Monophosphate-activated Protein Kinase, «протеинкиназой, активируемой аденозинмонофосфатом») 103. Таким образом, SPARC, как и ангиотензин II, и TGF-β, может выступать связующим звеном между работой митохондрий и процессами, протекающими в межклеточном матриксе.
Та же группа ученых представила еще один механизм взаимодействия митохондрий с матриксом при помощи SPARC 104. Схема их непростых взаимодействий представлена на рисунке 9.
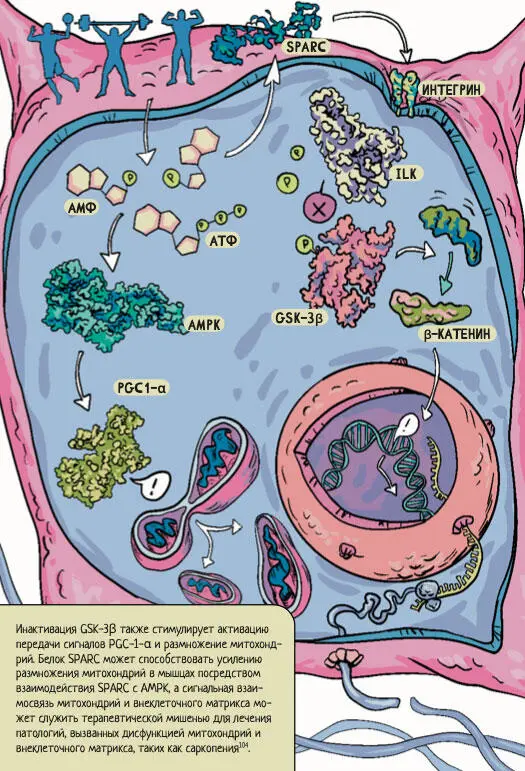
Рисунок 9.Влияние белка SPARC на экспрессию внеклеточного матрикса и на репликацию и транскрипцию митохондриальной ДНК. Физические упражнения вызывают активацию AMPK за счет увеличения соотношения аденозинмонофосфата к аденозинтрифосфату (AMФ/ATФ). Это, в свою очередь, индуцирует биогенез митохондрий посредством активации гамма-рецептора, активируемого пролифератором пероксисом коактиватора-1-альфа (PGC1-α), и повышает уровень экспрессии белка SPARC, что активирует интегрин-связанную киназу (ILK). Последняя фосфорилирует и инактивирует киназу гликогенсинтазы-3-бета (GSK-3ß), что приводит к стабилизации β-катенина и выработке белков мышечного внеклеточного матрикса. Инактивация GSK-3β также стимулирует активацию передачи сигналов PGC-1-α и размножение митохондрий. Белок SPARC может способствовать усилению размножения митохондрий в мышцах посредством взаимодействия SPARC с AMPK, а сигнальная взаимосвязь митохондрий и внеклеточного матрикса может служить терапевтической мишенью для лечения патологий, вызванных дисфункцией митохондрий и внеклеточного матрикса, таких как саркопения 104.
Читать дальше














