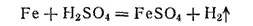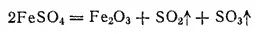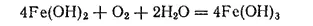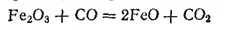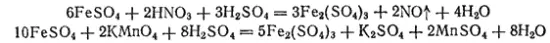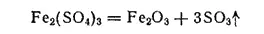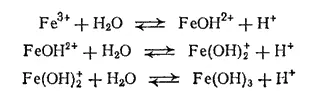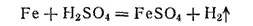
Сульфат железа(II) применяется для борьбы с вредителями растений, в производстве чернил и минеральных красок, при крашении тканей.
При нагревании железного купороса выделяется вода и получается белая масса безводной соли FeSO 4. При температурах выше 480°C безводная соль разлагается с выделением диоксида и триоксида серы; последний во влажном воздухе образует тяжелые белые пары серной кислоты:
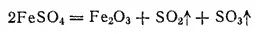
При взаимодействии раствора соли железа(II) со щелочью выпадает белый осадок гидроксида железа(II) Fe(OH) 2, который на воздухе вследствие окисления быстро принимает зеленоватую, а затем бурую окраску, переходя в гидроксид железа (III)
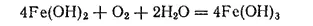
Безводный оксид железа(II) FeO можно получить в виде черного легко окисляющегося порошка восстановлением оксида железа(III) оксидом углерода(II) при 500°C:
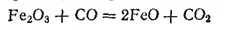
Карбонаты щелочных металлов осаждают из растворов солей железа(II) белый карбонат железа(II) FeCO 3. При действии воды, содержащей CO 2, карбонат железа, подобно карбонату кальция, частично переходит в более растворимую кислую соль Fe(HCO 3) 2. В виде этой соли железо содержится в природных железистых водах.
Соли железа (II) легко могут быть переведены в соли железа (III) действием различных окислителей — азотной кислоты, перманганата калия, хлора, например:
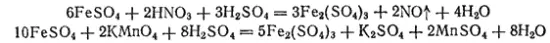
Ввиду способности легко окисляться, соли железа(II) часто применяются как восстановители.
- 669 -
Соединения железа (III).
Хлорид железа (III) FeCl 3представляет собой темно-коричневые с зеленоватым отливом кристаллы. Это вещество сильно гигроскопично; поглощая влагу из воздуха, оно превращается в кристаллогидраты, содержащие различное количество воды и расплывающиеся на воздухе. В таком состоянии хлорид железа (III) имеет буро-оранжевый цвет. В разбавленном растворе FeCl 3гидролизуется до основных солей. В парах хлорид железа (III) имеет структуру, аналогичную структуре хлорида алюминия (стр. 615) и отвечающую формуле Fe 2Cl 6; заметная диссоциация Fe 2Cl 6на молекулы FeCl 3начинается при температурах около 500°C.
Хлорид железа (III) применяют в качестве коагулянта при очистке воды, как катализатор при синтезах органических веществ, в текстильной промышленности.
Сульфат железа (III) Fe 2(SO 4) 3— очень гигроскопичные, расплывающиеся на воздухе белые кристаллы. Образует кристаллогидрат Fe 2(SO 4) 3·9H 2O (желтые кристаллы). В водных растворах сульфат железа (III) сильно гидролизован. С сульфатами щелочных металлов и аммония он образует двойные соли — квасцы, например железоаммонийные квасцы (NH 4)Fe(SO 4) 2·12H 2O — хорошо растворимые в воде светло-фиолетовые кристаллы. При прокаливании выше 500°C сульфат железа (III) разлагается в соответствии с уравнением:
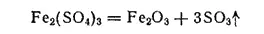
Сульфат железа (III) применяют, как и FeCl 3, в качестве коагулянта при очистке воды, а также для травления металлов. Раствор Fe 2(SO 4) 3способен растворять Cu 2S и CuS с образованием сульфата меди(II) это используется при гидрометаллургическом получении меди.
При действии щелочей на растворы солей железа (III) выпадает красно-бурый гидроксид железа (III) Fe(OH) 3, нерастворимый в избытке щелочи.
Гидроксид железа (III) - более слабое основание, чем гидроксид железа (II) это выражается в том, что соли железа (III) сильно гидролизуются, а со слабыми кислотами (например, с угольной, сероводородной) Fe(OH) 3солей не образует. Гидролизом объясняется и цвет растворов солей железа (III): несмотря на то, что Fe 3+почти бесцветен, содержащие его растворы окрашены в желто-бурый цвет, что объясняется присутствием гидроксо-ионов железа или молекул Fe(OH) 3, которые образуются благодаря гидролизу:
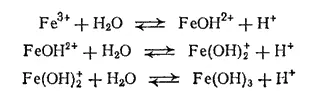
- 670 -
При нагревании окраска темнеет, а при прибавлении кислот становится более светлой вследствие подавления гидролиза.
Читать дальше
Конец ознакомительного отрывка
Купить книгу