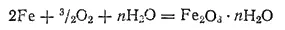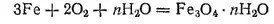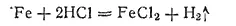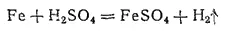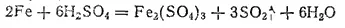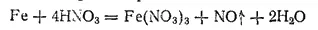Таким образом, в зависимости от условий кристаллизации, чугун может содержать углерод в виде цементита, графита или в виде их смеси. Форма образующегося графита также может быть различной.
Белый чугун содержит весь углерод в виде цементита. Он обладает высокой твердостью, хрупок и поэтому имеет ограниченное применение. В основном он выплавляется для передела в сталь.
В сером чугуне углерод содержится главным образом в виде пластинок графита. Серый чугун характеризуется высокими литейными свойствами (низкая температура кристаллизации, текучесть в жидком состоянии, малая усадка) и служит основным материалом для литья. Он широко применяется в машиностроении для отливки станин станков и механизмов, поршней, цилиндров. Кроме углерода, серый чугун всегда содержит другие элементы.
- 667 -
Важнейшие из них — это кремний и марганец. В большинстве марок серого чугуна содержание углерода лежит в пределах 2,4-3,8%, кремния 1-4% и марганца до 1,4%.
Высокопрочный чугун получают присадкой к жидкому чугуну некоторых элементов, в частности магния, под влиянием которого графит при кристаллизации принимает сферическую форму. Сферический графит улучшает механические свойства чугуна. Из высокопрочного чугуна изоговляют коленчатые валы, крышки цилиндров, детали прокатных станов, прокатные валки, насосы, вентили.
Ковкий чугун получают длительным нагреванием отливок из белого чугуна. Его применяют для изготовления детален, работающих при ударных и вибрационных нагрузках (например, картеры, задний мост автомобиля). Пластичность и прочность ковкого чугуна обусловлены тем, что углерод находится в нем в форме хлопьевидного графита.
242. Химические свойства железа. Соединения железа.
Чистое железо получают различными методами. Наибольшее значение имеют метод термического разложения пентакарбонила железа (см. § 193) и электролиз водных растворов его солей.
Во влажном воздухе железо быстро ржавеет, т. е. покрывается бурым налетом гидратированного оксида железа, который вследствие своей рыхлости не защищает железо от дальнейшего окисления. В воде железо интенсивно корродирует; при обильном доступе кислорода образуются гидратные формы оксида железа(III):
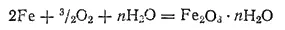
При недостатке кислорода или при его затрудненном доступе образуется смешанный оксид Fe 3O 4(FeO·Fe 2O 3):
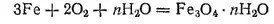
Железо растворяется в соляной кислоте любой концентрации:
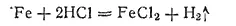
Аналогично происходит растворение в разбавленной серной кислоте:
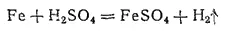
В концентрированных растворах серной кислоты железо окисляется до железа(III):
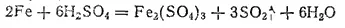
Однако в серной кислоте, концентрация которой близка к 100%, железо становится пассивным и взаимодействия практически не происходит.
В разбавленных и умеренно концентрированных растворах азотной кислоты железо растворяется:
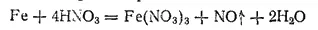
При высоких концентрациях HNO 3растворение замедляется и железо становится пассивным.
Для железа характерны два ряда соединений: соединения железа(II) и соединения железа(III). Первые отвечают оксиду железа (II), или закиси железа, FeO, вторые — оксиду железа(III), или окиси железа, Fe 2O 3.
- 668 -
Кроме того, известны соли железной кислоты H 2FeO 4, в которой степень окисленности железа равна +6.
Соединения железа(II).
Соли железа(II) образуются при растворении железа в разбавленных кислотах, кроме азотной. Важнейшая из них — сульфат железа(II), или железный купорос, FeSO 4·7H 2O, образующий светло-зеленые кристаллы, хорошо растворимые в воде. На воздухе железный купорос постепенно выветривается и одновременно окисляется с поверхности, переходя в желто-бурую основную соль железа(III).
Сульфат железа(II) получают путем растворения обрезков стали в 20—30%-ной серной кислоте:
Читать дальше
Конец ознакомительного отрывка
Купить книгу