dF = dU – TdS или Δ F = ΔU – TΔS
G = H – TS = U + pV – TS – свободная энергия Гиббса – изобарно-изотермический потенциал (Дж) – определяет направление и предел самопроизвольного протекания процесса в закрытой системе, находящейся в изобарно-изотермических условиях.
dG = dH – TdS или Δ G = ΔН – TΔS
ΔG = Σ(ν iG i) прод– Σ(ν iG i) исх
ΔG 0 = Σ(ν iΔG обр 0) прод– Σ(ν iΔG обр 0) исх
Условия самопроизвольного протекания процессов в закрытых системах
Изобарно-изотермические (Р = const, Т = const):
ΔG < 0, dG < 0
Изохорно-изотермические (V = const, Т = const):
ΔF < 0, dF < 0
Термодинамическим равновесием называется такое термодинамическое состояние системы с минимальной свободной энергией, которое при постоянстве внешних условий не изменяется во времени, причем эта неизменяемость не обусловлена каким-либо внешним процессом.
Условия термодинамического равновесия в закрытой системе
Изобарно-изотермические (Р = const, Т = const):
ΔG = 0, dG = 0, d 2G > 0
Изохорно-изотермические (V = const, Т = const):
ΔF = 0, dF = 0,d 2F > 0
Уравнения изотермы химической реакции:
Для реакции v 1A 1+ v 2A 2 + … =v′ 1B 1+ v′ 2B 2+ …
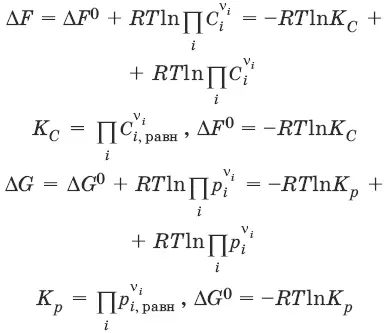
Здесь C i,p i – концентрации, давления реагирующих веществ в любой момент времени, отличный от состояния равновесия.
Влияние внешних условий на химическое равновесие
Принцип смещения равновесия Ле Шателье-Брауна
Если на систему, находящуюся в состоянии истинного равновесия, оказывается внешнее воздействие, то в системе возникает самопроизвольный процесс, компенсирующий данное воздействие.
Влияние температуры на положение равновесия
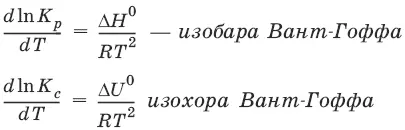
Экзотермические реакции: ΔН° < 0 ( ΔU° < 0). Повышение температуры уменьшает величину константы равновесия, т. е. смещает равновесие влево.
Эндотермические реакции: ΔН° > 0 ( ΔU° > 0). Повышение температуры увеличивает величину константы равновесия (смещает равновесие вправо).
Компонент – химически однородная составная часть системы, которая может быть выделена из системы и существовать вне ее. Число независимых компонентов системы равно числу компонентов минус число возможных химических реакций между ними.
Число степеней свободы – число параметров состояния системы, которые могут быть одновременно произвольно изменены в некоторых пределах без изменения числа и природы фаз в системе.
Правило фаз Дж. Гиббса:
Число степеней свободы равновесной термодинамической системы С равно числу независимых компонентов системы К минус число фаз Ф плюс число внешних факторов, влияющих на равновесие: С = К – Ф + n.
Для системы, на которую из внешних факторов влияют только температура и давление, можно записать: С = К – Ф + 2.
Принцип непрерывности – при непрерывном изменении параметров состояния все свойства отдельных фаз изменяются также непрерывно; свойства системы в целом изменяются непрерывно до тех пор, пока не изменится число или природа фаз в системе, что приводит к скачкообразному изменению свойств системы.
Согласно принципу соответствия, на диаграмме состояния системы каждой фазе соответствует часть плоскости – поле фазы. Линии пересечения плоскостей отвечают равновесию между двумя фазами. Всякая точка на диаграмме состояния (т. н. фигуративная точка) отвечает некоторому состоянию системы с определенными значениями параметров состояния.
2.1. Диаграмма состояния воды
К = 1. В системе возможны три фазовых равновесия: между жидкостью и газом (линия ОА), твердым телом и газом (линия ОВ), твердым телом и жидкостью (линия OC). Три кривые имеют точку пересечения О, называемую тройной точкой воды, – отвечают равновесию между тремя фазами и С = 0; три фазы могут находиться в равновесии лишь при строго определенных значениях температуры и давления (для воды тройная точка отвечает состоянию с Р = 6,1 кПа и Т = 273,16 К).
Читать дальше
Конец ознакомительного отрывка
Купить книгу

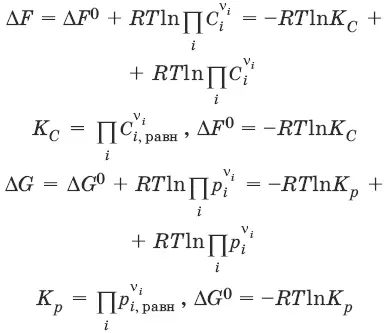
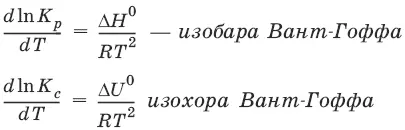







![Кирилл Рябов - Никто не вернётся [сборник litres]](/books/385781/kirill-ryabov-nikto-ne-vernetsya-sbornik-litres-thumb.webp)



