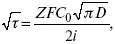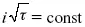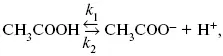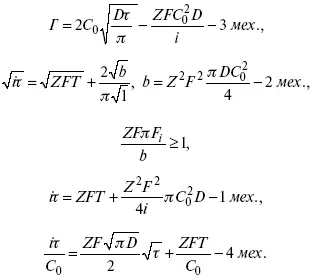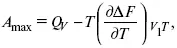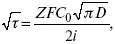
F – число Фарадея;
С 0– объемная концентрация ионов в растворе;
D – коэффициент диффузии.
В случае замедленной диффузии
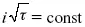
(зависит только от концентрации раствора) по угловому коэффициенту наклона прямой можно рассчитать коэффициент диффузии.

Знание зависимости переходного времени от i позволяет определить const скорости химической стадии и Кр; если электрохимическая реакция лимитируется замедленной предшествующей химической стадией то например: при катодном выделении Н 2
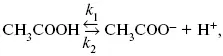
k 2 – const молизации, k р= k 1/k 2.

τ в химической стадии будет меньше ∑ τ на величину, определяемую const скорости замедленной химической стадии.

Кроме того, определение переходного времени позволяет графически находить адсорбцию веществ, участвующих в процессе. Количество электричества, определяемое длиной задержки на Е, t кривых, складывается из количества электричества, которое идет на протекание электрохимической реакции и может быть определено через долю τ , связанную с диффузией вещества к поверхности элект-рода и с адсорбцией вещества на электроде
iτ = iτ д+ iτ адс.
При высоких плотностях тока доля электричества, которое тратится на электрохимическое превращение диффундирующих частиц, → 0.
iτ ≈ iτ адс, iτ адс= Г
где Г – величина адсорбции.
Существует несколько механизмов протекания электрохимических реакций с участием адсорбированных частиц:
1) сначала в реакцию вступают частицы, адсорбированные на поверхности электрода, а потом те, которые подходят к поверхности за счет диффузии – «сначала адсорбат»;
2) «адсорбат потом» – сначала электрохимическому превращению подвергаются диффузионные частицы, а затем те, которые адсорбируются на поверхности;
3) выполняется в тех случаях, когда поверхностная концентрация реагирующих частиц и их концентрация у поверхности подчиняется уравнению линейной изотермы адсорбции;
4) когда соотношения скоростей восстановления адсорбированных частиц и частиц диффундирующих из объема раствора, их концентрация не зависит от времени:
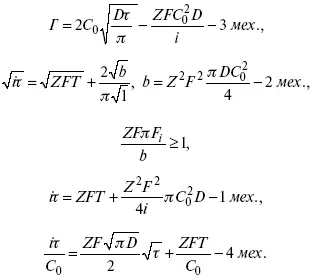

ЛЕКЦИЯ № 15. Третий закон термодинамики
Понятие химического сродства.Известно, что многие вещества реагируют друг с другом легко и быстро, другие вещества реагируют с трудом, а третьи – не реагируют. Исходя из этого, вывели предположение, что между веществами существует какое-то химическое сродство.
1-е предположение – мерой химического сродства была скорость реакции.
2-е предположение – М. Бертло и Х. Томсон высказали, что мерой химического сродства является тепловой эффект.
3-е предположение – max А (Вант-Гофф). Если max А > 0, то химическое сродство между веществами существует, и реакция протекает слева направо. Если А max < 0 →, то химического сродства между веществами нет, и реакция протекает справа налево. Если А max = 0, то реакция протекает и туда, и обратно. На основе этого создавался третий закон термодинамики; М. Бертло и Х. Томсон , изучая поведение термодинамических систем при низких температурах, в 1906 г. обнаружили, что при низких температурах между веществами существует так называемое химическое сродство, которое они определили как тепловой эффект, ими было установ-лено, что тепловой эффект Q v– А maxв конденсированных системах при низких температурах, где А max – максимальная работа.
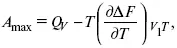
но на самом деле это не max, если исходить из уравнения Гельмгольца.
Читать дальше
Конец ознакомительного отрывка
Купить книгу