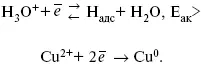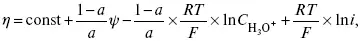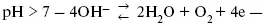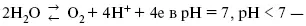В присутствии NaJ, NaCl происходит изменение хода электрокапиллярной кривой.
Кривые 2 и 3 – электрокапиллярные кривые, снятые в электролитах, содержащих ПА анионы: J -, Cl –. В области наиболее низких электродных потенциалов все три электрокапиллярные кривые совпадают, так как при указанных потенциалах наблюдается десорбция ПА анионов. В присутствии ПА катионов электрокапиллярные кривые имеют вид:
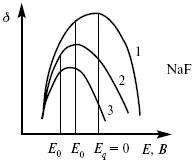
Рис. 13. Кривые 2, 3 в присутствии ПА катионов.
Наличие в элементе ПА органических веществ приводит к снижению max электрокапиллярной кривой (рис. 14).
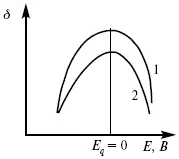
Рис. 14. Кривая 2 – с добавками ПАВ (поверхностно-авктивныхвеществ).
Молекулярный тип – не дипольные молекулы 2 – с добавками ПА органическими.
Электрокапиллярная кривая – исходная кривая, дифференцируя ее, определяем емкость ДЭС.
7. Электрохимическое перенапряжение (перенапряжение переноса заряда)
1. Вывод уравнения полной поляризационной кривой.
2. Перенапряжение при выделении Н 2.
3. Перенапряжение при выделении О 2.
Если на электроде замедлена стадия присоединения или отдачи электронов, то возникающее перенапряжение – перенапряжение переноса заряда (перенапряжение перехода – электрохимическое перенапряжение).
Теория разряжения для реакции выделения Н 2на катоде:
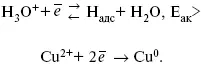
Стадия переноса электрона из-за построения новой кристаллической решетки затруднена.
8. Факторы, влияющие на перенапряжение водорода. Перенапряжение кислорода
Факторы, влияющие на η Н 2:
1) ρ тока (плотность тока). Зависимость от плотности тока описывается уравнением Тафеля;
2) природа материала катода – ряд по возрастанию η, η– перенапряжение.
В уравнении Тафеля const a характеризует зависимость η от природы материала катода, а константа b отражает зависимость от плотности тока.
В классическом варианте b – 0,12В, а – меняется в широких пределах, из-за разных металлов и разных катодных взаимодействий с Н 2.
а – 0,01…1,0 В, чем больше а, тем больше η Н 2. Большим η Н 2обладают: Hg, Pb, Zn, низким η Н 2– Pt, средним η Н 2– Fe, Co, Ni;
3) состав раствора. Наибольшее η в рН = 7, а в рН < 7 η меньше. В растворе могут быть ПАВ, они влияют на величину η , включаются в плотную часть ДЭС.
Уравнение η в присутствии ПАВ:
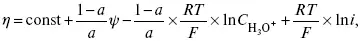
где ψ – потенциал плотной части ДЭС;
4) температура. С ростом температуры η уменьшается.
Перенапряжение кислорода
Кислород выделяется на аноде при потенциалах более положительных, чем равновесный.
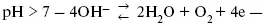
в щелочном растворе,
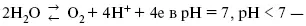
в нейтральном, кислом растворе.
Перенапряжение О 2зависит от ρ т(плотность тока), в соответствии с уравнением Тафеля. В ряду металлов, расположенных по мере возрастания перенапряжения Н 2, перенапряжение О 2, наоборот, уменьшается. При увеличении температуры η О 2снижается.
Когда на металле выделяется кислород, то он сразу же окисляет металл, и поэтому дальнейшее выделение кислорода уже проходит на окисленной поверхности.
ЛЕКЦИЯ № 14. Применение теоретической и прикладной электрохимии
1. Прикладная электрохимия
Прикладная электрохимия– часть электрохимии, которая рассматривает электрохимические реакции с точки зрения применения их для практических целей – получения электрической энергии, нанесения металлических покрытий или получения целевых продуктов.
По современным прогнозам, электрохимия должна играть важную роль в энергетике будущего. После овладения управляемой термоядерной реакцией возникает проблема разумного использования получаемой энергии, в связи с этим большое значение отводится водородной энергетике. Энергия термоядерных электростанций будет, в основном, расходоваться на разложение Н 2О. Получаемый таким путем Н 2может быть использован как экологически чистый теплоноситель для отопления городов, для приведения в движение автомобилей. Электрохимический метод используют для очистки сточных вод с выделением Cu, Zn, Ag и других, процесс электродиализа – для опреснения вод.
Читать дальше
Конец ознакомительного отрывка
Купить книгу