Ферменты делят на шесть классов:
1. Оксидоредуктазы. Это ферменты, катализирующие окислительно-восстановительные реакции. Примером оксидоредуктаз могут служить пируватдегидрогеназа, отнимающая водород от пировиноградной кислоты, каталаза, разлагающая пероксид водорода, и др.
2. Трансферазы. Трансферазы осуществляют перенос с одной молекулы на другую целых атомных групп. Они могут переносить группы СН3, СООН, Н2РО3 и др.
3. Гидролазы. Эти ферменты вызывают разрыв связей типа
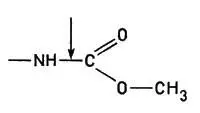
4. Гидролазы вызывают разрыв связей
и подобные им с последующим присоединением воды:
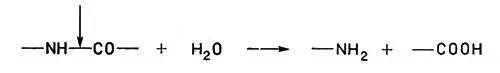
5. Гидролазы вызывают разрыв связей с последующим присоединением воды
К гидролазам относятся пищеварительные ферменты пепсин, химотрипсин и др., а также липазы, расщепляющие жиры.
6. Лиазы. Лиазы тоже расщепляют связи С-С, С-N, С=O и др., но без участия воды, т. е. негидролитическим путем.
7. Изомеразы. Эти ферменты способствуют частичной перестройке молекул субстрата.
8. Лигазы. Лигазы обеспечивают соединение молекул субстрата, причем энергия, необходимая для этого, доставляется аденозинтрифосфатом (АТФ).
Уже простое перечисление этих функций наводит на мысль, что ферменты действуют в клетках не в одиночку, а совместно, последовательно перекраивая молекулы пищевых веществ: разрывая одни связи, создавая другие, изменяя общий каркас молекулы, перенося на нее или отнимая от нее целые группы атомов и т. д. Ферменты, в отличие от большинства технических катализаторов, функционируют в составе сложных систем; работа их согласована так, что продукт деятельности одного фермента обязательно попадает в сферу влияния вполне определенного другого, и скорости превращений на всех стадиях химического конвейера клетки также строго согласованы и регулируются автоматически.
Клетка и организм располагают и средствами управления своими "химическими заводами", так как клетка не только пользуется ферментами, но и сама создает их. Если при данных условиях работу какой-либо цепочки ферментов необходимо прекратить, так как вырабатываемый ею продукт имеется в избытке, выключается синтез соответствующих ферментов или подавляется деятельность одного из них, и таким образом весь конвейер временно останавливается. Это значит, что ферментная система пространственно организована. Она организована также во времени, потому что ферменты активируются и даже появляются в большей концентрации в те моменты, когда клетка нуждается в их деятельности.
Молекулярная масса ферментов велика и измеряется десятками, сотнями тысяч и даже миллионами. Ниже (табл. 5) приведены молекулярные массы некоторых ферментов.
Изучение химического состава ферментов показало, что все они без исключений содержат белок. Белковая природа ферментов объяснила многие детали их синтеза в клетках, причины, по которым они легко фиксируются на мембранах. И вместе с тем появилась важная проблема в теории катализа — вопрос о механизме действия биологических катализаторов, которые, обладая очень сложной геометрической структурой, не являются вполне "жесткими", подобно кристаллическим оксидам или металлам, а могут изменяться уже в процессе каталитической реакции.
Таблица 5. Молекулярные массы ферментов (по X. Неттеру)
Фермент | Относительная молекулярная масса | Функция фермента
Рибонуклеаза | 1,4*10 4| Гидролиз рибонуклеиновой кислоты
Химотрипсин | 2,16*10 4| Гидролиз белков
Пепсин | 3,9*10 4| Гидролиз белков
Уреаза | 48*10 4| Разложение мочевины
Амилаза | 15*10 4| Гидролиз крахмала
Карбонангидраза | 3*10 4| Разложение гидрокарбонатов
На белковых молекулах ферментов имеются зоны или области, в которых и развивается каталитическая реакция. Можно, по аналогии с обычными катализаторами, называть эти зоны активными центрами. Активный центр ферментов, катализирующих некоторые окислительно-восстановительные реакции, в частности каталазы (разлагающей пероксид водорода), состоит из комплексного соединения железа с порфирином (замещенным порфином). Направленность действия фермента в значительной мере зависит от природы того белка, который входит в его состав.
В состав различных ферментов входят разные металлы. Так, марганец входит в состав аргиназы, разлагающей некоторые составные части белков, цинк — в карбон-ангидразу. Медь содержится в аскорбиноксидазе — ферменте, окисляющем витамин С. Во многих растениях содержится фермент пероксидаза. Он усиливает окисление органических веществ пероксидом водорода. Активная группа этого фермента состоит из комплексного иона железа такого же типа, что и в каталазе. Если добавить к ферменту раствор сероводорода, то железо прочно соединится с серой и фермент потеряет активность.
Читать дальше