24. Bern C, Ortega Y, Checkley W, Roberts JM, Lescano AG, Cabrera L, et al.Epidemiologic differences between cyclosporiasis and cryptosporidiosis in Peruvian children. Emerg Infect Dis. 2002 Jun;8(6):581-5.
25. Villegas S, Arango A.Presentación de casos. Cyclospora cayetanensis . Acta Med Colombia 2000;25:84-6.
26. Botero-Garcés J, Montoya-Palacio MN, Barguil JI, Castaño-González A.Brote epidémico por Cyclospora cayetanensis in Medellín, Colombia. Rev Salud Publ 2006;8:258-8.
27. Herwaldt BL, Ackers ML.An outbreak in 1996 of cyclosporiasis associated with imported raspberries. The Cyclospora Working Group. N Engl J Med. 1997 May 29;336(22):1548-56.
28. Herwaldt BL. Cyclospora cayetanensis : a review, focusing on the outbreaks of cyclosporiasis in the 1990s. Clin Infect Dis. 2000 Oct;31(4):1040-57.
29. Ho AY, Lopez AS, Eberhart MG, Levenson R, Finkel BS, da Silva AJ, et al.Outbreak of cyclosporiasis associated with imported raspberries, Philadelphia, Pennsylvania, 2000. Emerg Infect Dis. 2002 Aug;8(8):783-8.
30. Hoge CW, Shlim DR, Ghimire M, Rabold JG, Pandey P, Walch A, et al.Placebo-controlled trial of co-trimoxazole for Cyclospora infections among travellers and foreign residents in Nepal. Lancet. 1995 Mar 18;345(8951):691-3.
31. Verdier RI, Fitzgerald DW, Johnson WD Jr, Pape JW.Trimethoprim-sulfamethoxazole compared with ciprofloxacin for treatment and prophylaxis of Isospora belli and Cyclospora cayetanensis infection in HIV-infected patients. A randomized, controlled trial. Ann Intern Med. 2000 Jun 6;132(11):885-8.
32. Fox LM, Saravolatz LD.Nitazoxanide: a new thiazolide antiparasitic agent. Clin Infect Dis. 2005 Apr 15;40(8):1173-80.
Esta tercera coccidiosis ha tomado importancia en los últimos años por ser oportunista en pacientes inmunodeficientes, en los cuales causa enfermedad. Aunque es poco diagnosticada en algunas regiones, la cistoisosporiasis se encuentra cada vez que se busca en los exámenes coprológicos, aunque su prevalencia es baja. Se transmite por ingestión de ooquistes eliminados en materias fecales. Produce inflamación intestinal y eosinofilia. El tratamiento es con trimetoprima-sulfametoxazol.
Agente causal. Cystoisospora belli es un protozoo de la subclase Coccidia, para el cual el hombre es el único huésped definitivo. Habita en el intestino delgado, donde tiene reproducción sexual y asexual. Se elimina con las materias fecales en forma de ooquiste, de color blanco transparente, con membrana delgada y oval. Mide aproximadamente 23 por 13 µm. En el momento de la eliminación contiene una masa granulosa llamada esporoblasto ( figuras 3-23). Cuando se hace la tinción de Ziehl-Neelsen se observa el esporoblasto de color rojo, pero si el paciente está en tratamiento se ve una coloración defectuosa ( figura 3-24). El esporoblasto se divide en dos en el medio ambiente, cada uno de los cuales produce una membrana para constituir dos esporoquistes ( figura 3-25). En el interior de cada esporoquiste se forman cuatro esporozoítos fusiformes. 1
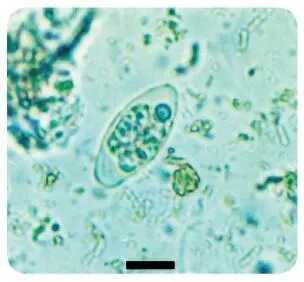
Figura 3-23. Cystoisospora belli.Ooquiste con un solo esporoblasto en un examen en fresco de materias fecales. (La barra de la foto mide 10 micras).
Cortesía: OMS.
Tabla 3-1. Diferencias en la epidemiología y en la sintomatología de ciclosporiasis y criptosporidiosis.
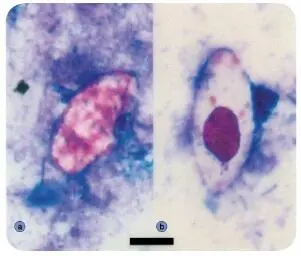
Figura 3-24. Cystoisospora belli.Ooquiste inmaduro con coloración Ziehl-Neelsen. a. Lado izquierdo, es atípico, así se ve cuando está el paciente con tratamiento; b. Lado derecho, ooquiste típico con esporoblasto de color rojo. (La barra de la foto mide 10 micras).
Cortesía: OMS.
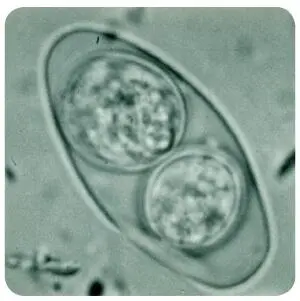
Figura 3-25. Cystoisospora belli.Ooquiste maduro con dos esporoquistes de pared gruesa. Contraste de fase.
Cortesía: Miguel F. Torres, Departamento de microbiología, Escuela de Química Biológica, USAC, Guatemala.
Ciclo de vida.La transmisión se hace por vía oral al ingerir ooquistes maduros ( figura 3-25). En la región duodenoyeyunal se produce desenquistación y se liberan los esporozoítos que invaden las células epiteliales (enterocitos), donde se reproducen asexualmente para formar merozoítos que infectan nuevas células. Algunos merozoítos están determinados para iniciar la reproducción sexual para lo cual se convierten en gametocitos macho y hembra que, a su vez, pasan a micro y macrogametos con capacidad de fertilización. La unión de estas células origina un zigoto que se transforma en ooquiste y constituye la forma que se observa en el examen coprológico. Este ooquiste madura en el medio ambiente para formar, en su interior, dos esporoquistes. Este estado es la forma infectante. 2
Patología y patogenia.Los parásitos se localizan dentro de las células epiteliales del intestino delgado, las cuales se destruyen con producción de reacción inflamatoria y abundantes eosinófilos. La mucosa intestinal puede aplanarse y sufrir algún grado de necrosis. La invasión puede llegar a la lámina propia y al intestino grueso. Existe un caso con invasión a ganglios linfáticos mesentéricos y traqueobronquiales en un paciente con sida. 3Otro caso correspondió a un linfoma no Hodgkin con presencia de Cystoisospora en los tejidos. 4Se publicó, igualmente, un caso de colecistitis calculosa con presencia de Cystoisospora en un paciente con sida. 5En los pacientes con sida, las lesiones intestinales son más intensas y de mayor duración. Dentro de las células intestinales se encuentran los merozoítos, los gametocitos y los ooquistes en desarrollo. En las vellosidades se describe acortamiento y en las criptas hiperplasia e infiltrado eosinofílico. 6
Manifestaciones clínicas.Debe diferenciarse la clínica en personas con estado inmunitario normal y en aquellas con inmunodeficiencias. En las primeras, la cistoisosporiasis es generalmente autolimitada y puede ser asintomática; cuando hay sintomatología, consiste en dolor abdominal, náuseas, vómito y meteorismo, diarrea, anorexia y pérdida de peso; en algunos casos hay fiebre leve durante los primeros días. La presencia de hipereosinofilia circulante, usualmente de más del 15%, se presenta en un poco más de la mitad de los pacientes con esta parasitosis; es la única protozoosis intestinal con esta característica. 7En pacientes inmunocompetentes que viajan a países endémicos, esta parasitosis puede causar diarrea de los viajeros. 8,9En las segundas, las personas inmunocomprometidas, la sintomatología es más intensa y duradera; la diarrea es acuosa y muchas veces intensa, de duración prolongada o con recurrencias frecuentes; hay dolor abdominal severo, vómito (en algunas ocasiones) y síntomas generales como debilidad, anorexia y enflaquecimiento. 10Se ha informado parasitemia en un paciente con sida. 11
Читать дальше















