Der Aufbau der Zunge ist weitaus komplexer als er im Rahmen dieses Glossars beschrieben werden kann. Deshalb ist es nicht verwunderlich, dass es zu Abweichungen von der normalen Anatomie kommen kann. Diese Variationen müssen keinen Krankheitswert besitzen, können aber neben einer pathologischen Veränderung auch Ausdruck allgemeinmedizinischer Erkrankungen sein 9. Therapeutische Ansätze, wie beispielsweise der Einsatz eines Zungenschabers ( Abb. 3aund b), sind oftmals symptombezogen oder bei exogen verursachenden Faktoren streng ursachenbezogen 2. Für detailliertere Ausführungen wird auf die Bücher von Filippi 5und Bork 10verwiesen.
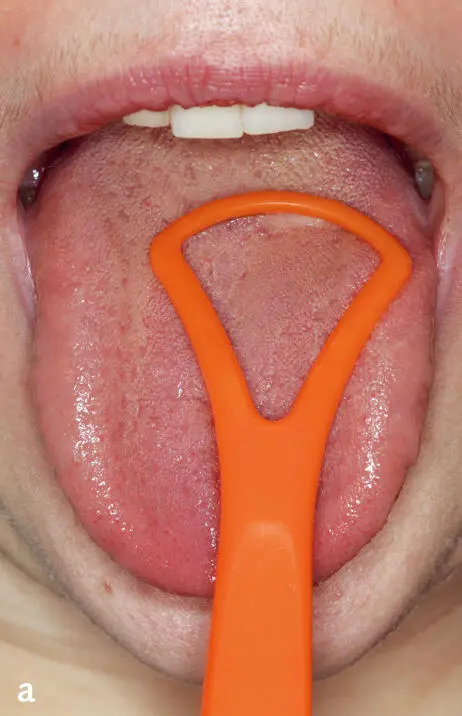

Abb. 3a und b Anwendung eines Zungenschabers auf dem Zungenrücken und exemplarische Einzeldarstellung.
1. Quirynen M, Teughels W, van Steenberghe D. Impact of antiseptics on one-stage, full-mouth disinfection. J Clin Periodontol 2006;33:49–52.
2. Scharf S, Eickholz P. Glossar der Grundbegriffe für die Praxis: Halitosis. Parodontologie 2014;25:461–467 (s. Beitrag 18 in diesem Buch).
3. Filippi A. Halitosis – Professionelle Behandlung von Mundgeruch in der zahnärztlichen Praxis. Berlin: Quintessenz, 2011.
4. Schünke M, Schulte E, Schumacher U. Prometheus Kopf, Hals und Neuroanatomie. Stuttgart: Thieme, 2012.
5. Filippi A, Hitz Lindenmüller I (Hrsg.). Die Zunge. Berlin: Quintessenz, 2016.
6. Chandrashekar J, Hoon MA, Ryba NJ, Zuker CS. The receptors and cells for mammalian taste. Nature 2006;444:288–294.
7. Naumova EA, Dierkes T, Sprang J, Arnold WH. The oral mucosal surface and blood vessels. Head Face Med 2013;9:8.
8. Shadan S. Molecular biology: A taste of umami. Nature 2009;457:160.
9. Petsos H, Aldiri T, Eickholz P. Glossar der Grundbegriffe für die Praxis: Die Zunge 2: Normvarianten und pathologische Veränderungen. Parodontologie 2018;29:71–77 (s. Beitrag 20 in diesem Buch).
10. Bork K., Burgdorf W., Hoede N. Mundschleimhaut- und Lippenkrankheiten: Klinik, Diagnostik und Therapie. Stuttgart: Schattauer, 2008.
Klinisch entzündungsfreie gesunde Gingiva hat eine feste Konsistenz, der Gingivarand verläuft girlandenförmig, die Papillen füllen die Interdentalräume aus und bluten bei Sondierung nicht. Bei hellhäutigen Menschen ist entzündungsfreie Gingiva rosa, bei dunkelhäutigen Menschen finden sich häufig melaninpigmentierte Areale ( Abb. 1). Histologisch stellt sich die Situation differenzierter dar. Bei völliger Entzündungsfreiheit finden sich keine bzw. nur vereinzelte Entzündungszeichen; man spricht von normaler Gingiva. Das Saumepithel haftet der Zahnoberfläche über Hemidesmosomen an. Auch bei normaler Gingiva finden sich im Saumepithel vereinzelte Leukozyten (neutrophile Granulozyten und Makrophagen) ( Abb. 2) 1. Histomorphometrisch setzt sich die völlig entzündungsfreie Gingiva zu etwa 30 % aus oralem Epithel, zu etwa 10 % aus Saumepithel und zu 60 % aus Bindegewebe zusammen. Ein solcher völlig entzündungsfreier Zustand erfordert allerdings eine perfekte Plaquekontrolle, die fast nur unter experimentellen Bedingungen, wenn die individuelle Mundhygiene über mehrere Wochen durch häufige professionelle Zahnreinigungen unterstützt wird, erreicht werden kann. Deshalb ist er selbst bei Personen mit effektiver individueller Mundhygiene, die vereinzelt immer noch geringe Mengen von bakterieller Plaque auf den Zähnen aufweisen, nicht zu finden. Bei effektiver individueller Mundhygiene zeigt die Gingiva ebenfalls keine klinischen, aber bereits histologische Entzündungszeichen; man spricht von klinisch gesunder Gingiva. Das histologische Erscheinungsbild der klinisch gesunden Gingiva entspricht in etwa dem Bild der initialen Läsion 2.
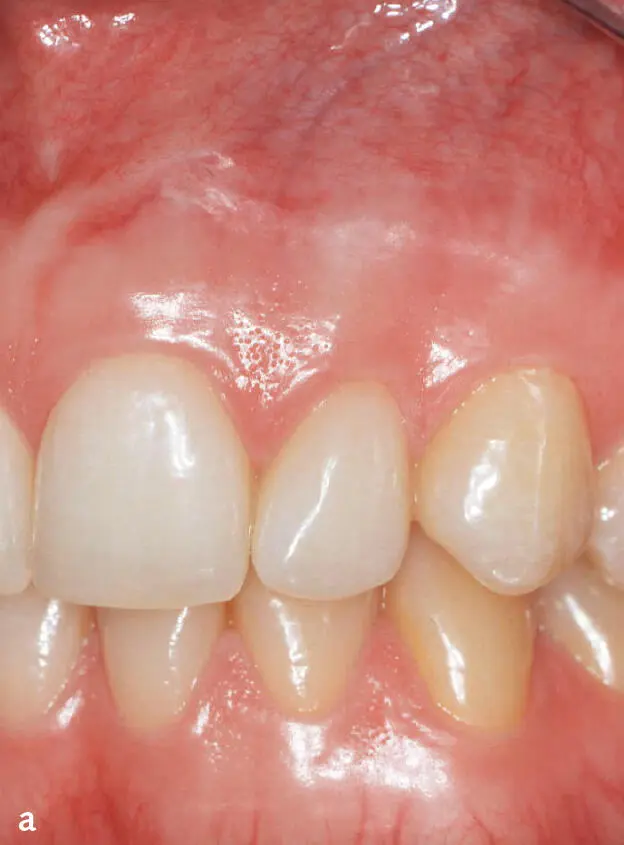
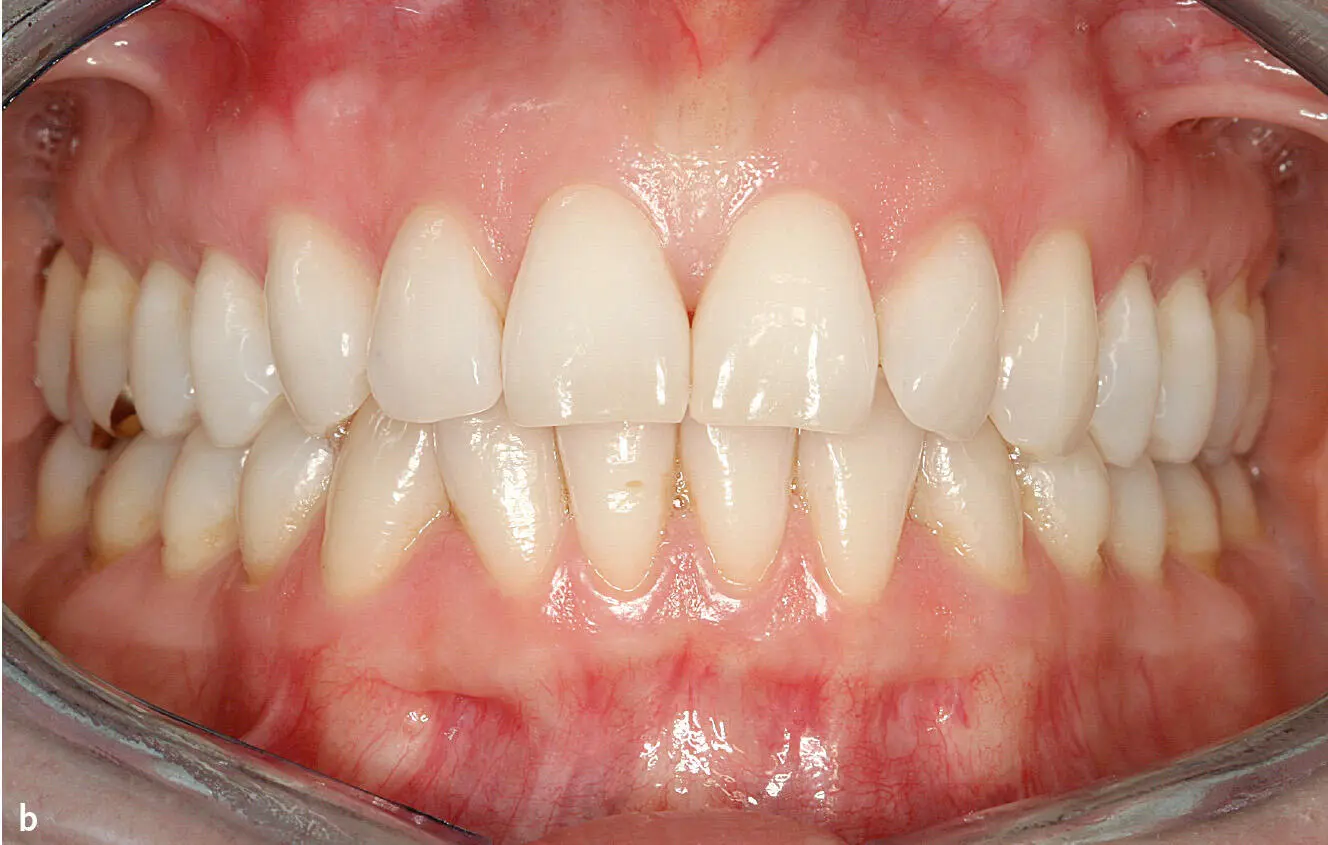
Abb. 1a und b Klinisch entzündungsfreie Gingiva: a) Frau im Alter von 24 Jahren, b) Frau im Alter von 41 Jahren.
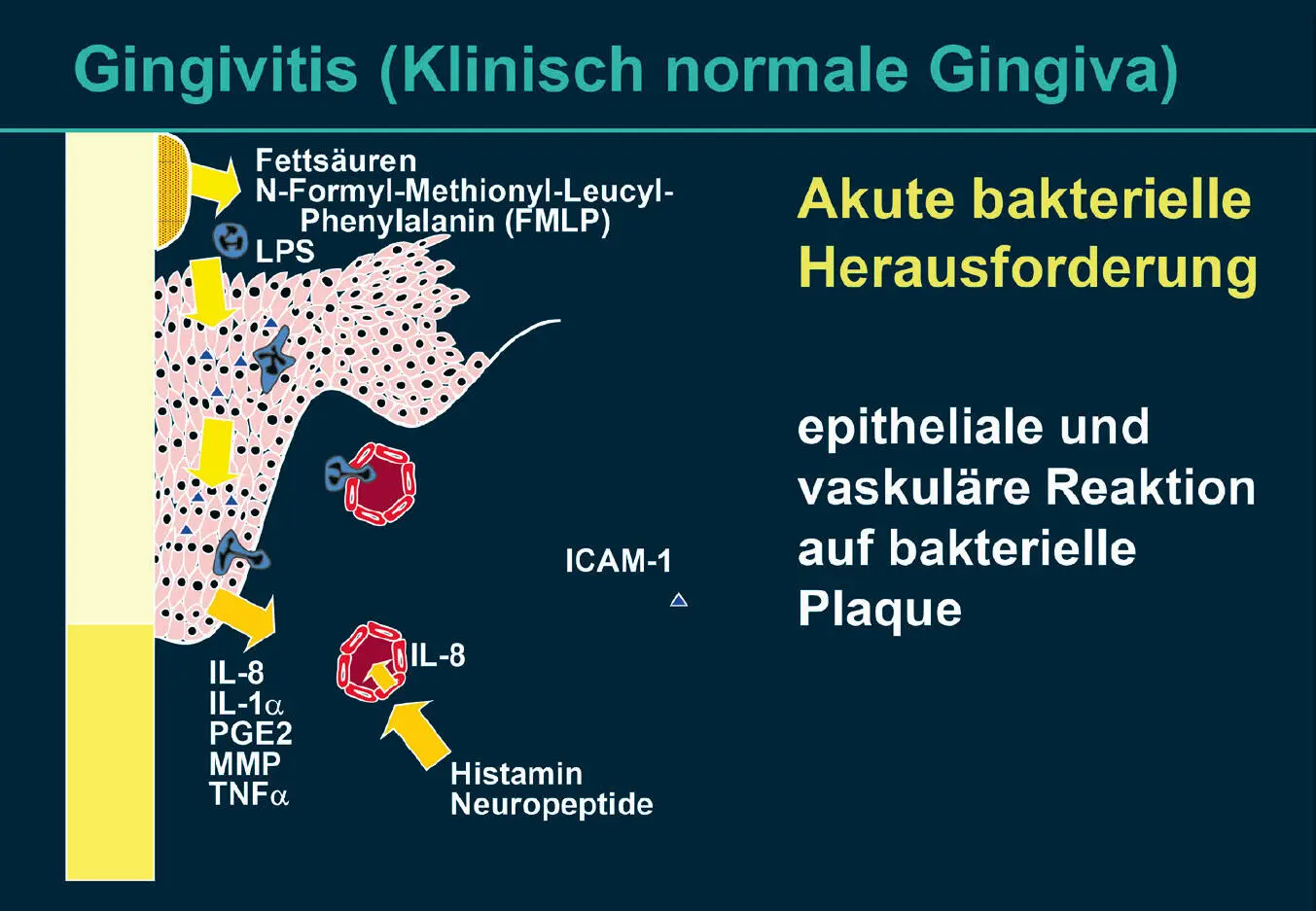
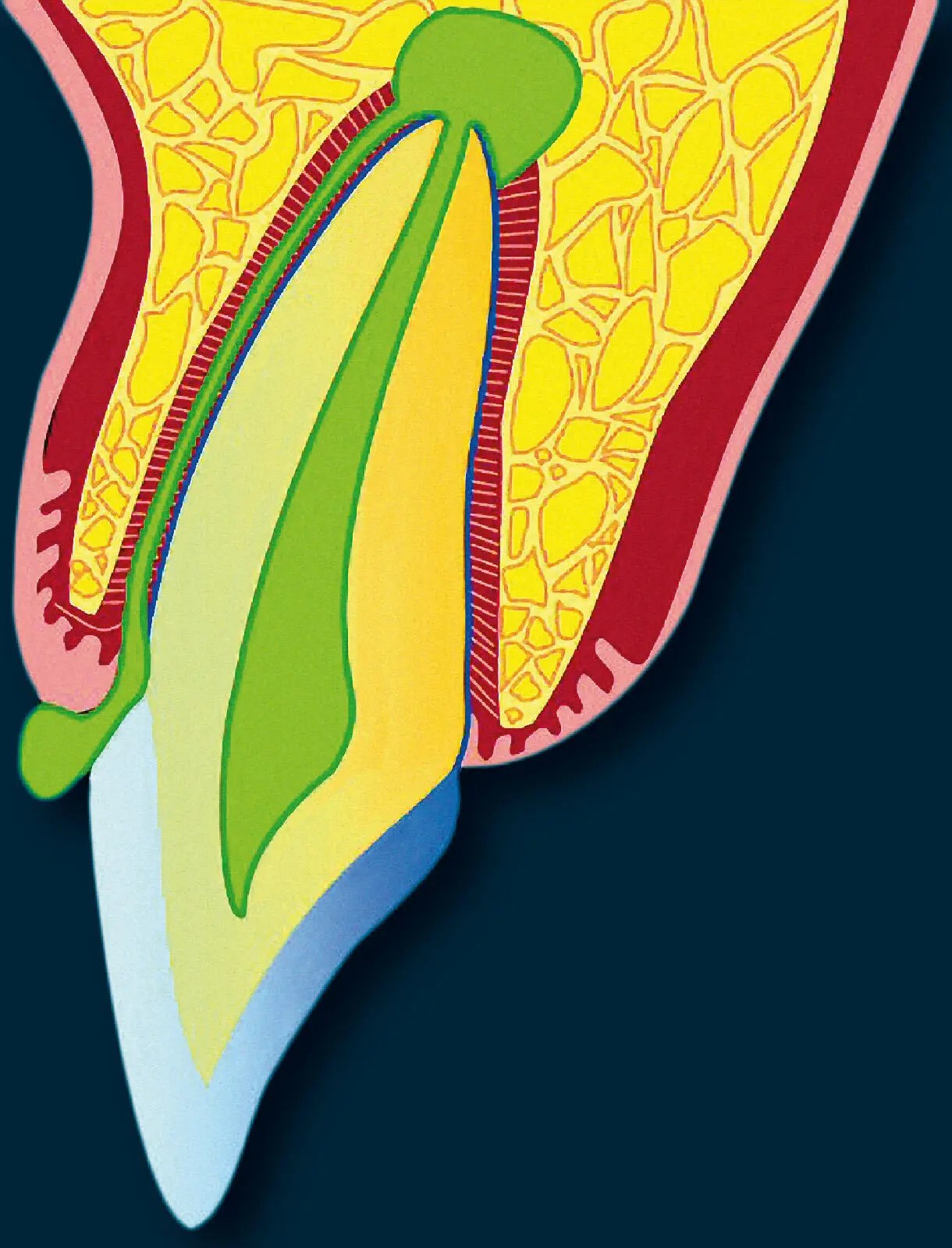
Abb. 2 Klinisch normale Gingiva: Bakterielle Plaque setzt Stoffwechselprodukte wie Fettsäuren, N-Formyl-MethionylLeucyl-Phenylalanin (FMLP) und Lipopolysaccharide (LPS) gramnegativer Bakterien frei. Diese antigenen Substanzen induzieren in den Saumepithelzellen die Produktion verschiedener Entzündungsmediatoren wie Interleukin-8 (IL-8), IL-1α, Prostaglandin E2 (PGE2), Matrix-Metalloproteinasen (MMP) und Tumornekrosefaktor-α (TNF-α). Neurale Komponenten des Epithels setzen Neuropeptide frei, die die Gefäße beeinflussen. Die bakteriellen Antigene und die epithelialen Produkte aktivieren perivaskuläre Mastzellen, die Histamin freisetzen, und Endothelzellen zur Freisetzung von IL-8, das ein Chemotaxin für neutrophile segmentkernige Granulozyten (PMN) ist (modifiziert nach Kornman et al. 4).
Initiale Läsion: akute entzündliche Reaktion
Die Umsatzrate des Saumepithels ist generell hoch und seine Zellen sind durch weniger Desmosomen verbunden als andere orale Epithelien. Eine verstärkte bakterielle Exposition erhöht diese Umsatzrate, die Interzellularräume weiten sich und ermöglichen somit einen verstärkten Ausstrom von Sulkusflüssigkeit sowie Leukozytenmigration. Die initiale Läsion zeigt bereits 24 Stunden nach Beginn der Plaqueakkumulation eine Dilatation der Gefäße des dentogingivalen Plexus. Es wird direkt benachbart zum Saumepithel vermehrt Blut in den mikrovaskulären Plexus gebracht. Der hydrostatische Druck wird erhöht und es öffnen sich Spalten zwischen den Endothelzellen der Kapillaren. Die Gefäßpermeabilität erhöht sich, sodass es zur Exsudation von Flüssigkeit und Proteinen in das Gewebe kommt ( Abb. 3). Die Folge ist eine vermehrte Exsudation von Sulkusflüssigkeit. Durch die Exsudation ins Gewebe und den Sulkus können schädigende Substanzen mikrobiellen Ursprungs verdünnt werden. Bakterien und deren Produkte werden aus dem Sulkus hinausgespült. Die Menge der exsudierten Sulkusflüssigkeit (Sulkusflüssigkeitsflussrate) ist proportional zum Schweregrad der Entzündungsreaktion. Parallel mit den Gefäßveränderungen kommt es nach 2 bis 4 Tagen zu einer vermehrten Migration von neutrophilen Granulozyten und Monozyten/Makrophagen aus dem subepithelialen Gefäßplexus durch das subepitheliale Bindegewebe (s. Abb. 3). Adhäsionsmoleküle wie das „Intercellular Adhesion Molecule-1“ (ICAM-1) und das „Endothelial Leukocyte Adhesion Molecule-1“ (ELAM-1), die durch proinflammatorische Zytokine (Interleukin-1β [IL-1β], Tumornekrosefaktor-α [TNF-α]) aktiviert wurden, ermöglichen den Leukozyten, sich an der Gefäßwand der postkapillären Venolen anzuheften, um dann hindurchzutreten (Diapedese). Die vermehrte Extravasation der Leukozyten erfordert eine erhöhte Anheftungsrate dieser Zellen an die Gefäßwände. Proinflammatorische Stimuli (Lipopolysaccharide [LPS], IL-1β, TNF-α) führen nicht nur zu erhöhter Gefäßpermeabilität und Expression von Leukozytenadhäsionsmolekülen, sondern auch zur Ausschüttung anderer proinflammatorischer Zytokine, wie IL-8, in die Blutbahn, durch die ein Rollen der Leukozyten induziert wird. Damit erhöht sich die Wahrscheinlichkeit eines Kontaktes zwischen Leukozyten-Integrinen und Endothelzelladhäsionsmolekülen (z. B. ICAM-1) ( Abb. 4).
Читать дальше


















