Source: Based on [183].
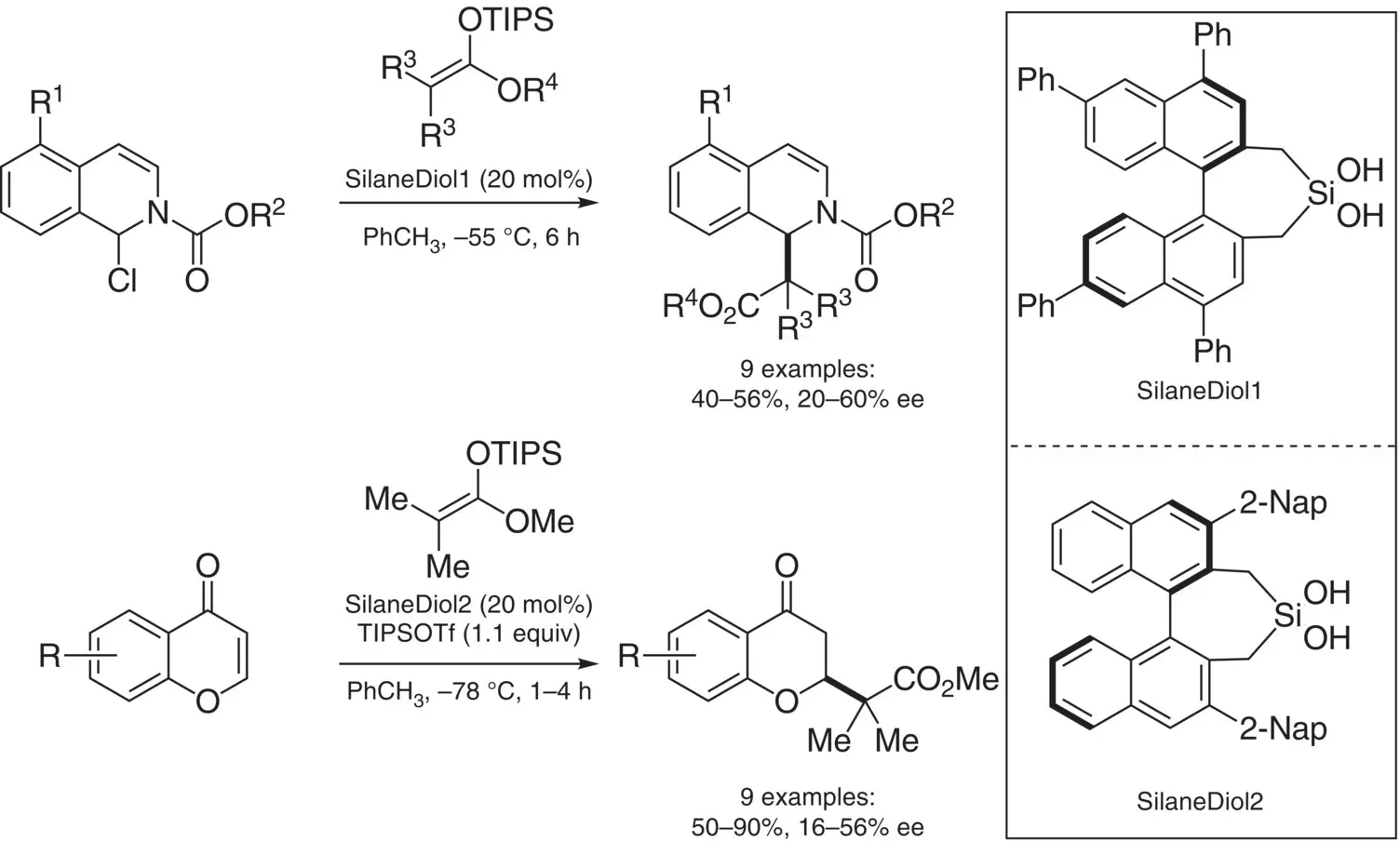
Scheme 4.56. Enantioselective transformations catalyzed by BINOL‐derived silane‐diols.
Source: Based on [191].
4.3.7.3. Asymmetric Ring Opening of Strained Heterocycles
In 2012, the Jacobsen group demonstrated that hydrogen bonding catalysts could affect the asymmetric ring opening of episulfonium cations with indoles ( Scheme 4.57) [193]. The source of the enantioselectivity was proposed to be an ensemble of electrostatic, cation‐π, and hydrogen‐bonding interactions between the anion‐bound catalyst, indole, and episulfonium. The Gouverneur lab extended this reactivity to utilizing fluoride as the nucleophile, a notoriously challenging fluorine source for asymmetric fluorination reactions [194]. Other advances in the field include an asymmetric selenocyclization through the intermediacy of a seleniranium ion‐pair [195]. It was shown that the seleniranium readily interconverts between two enantiomers via group transfer, allowing for a Curtin‐Hammett situation that determines the enantioselectivity of the reaction.
Since the initial reports of chiral cation phase‐transfer catalysis, there has been an exponential growth in the number of key strategies available for asymmetric induction of reactions involving ion‐pairing. Currently, there is a push to better understand the mechanistic interplay between the chiral ion, its achiral counterion, and the substrate. This has taken the form of utilizing traditional transition state analysis by DFT, as well as newer data‐intensive approaches that focus on linear‐regression analysis. Another major area of current focus is utilizing these interesting noncovalent effects in combination with the unique reactivity of transition‐metal catalysis, to yield novel enantioselective methodologies.
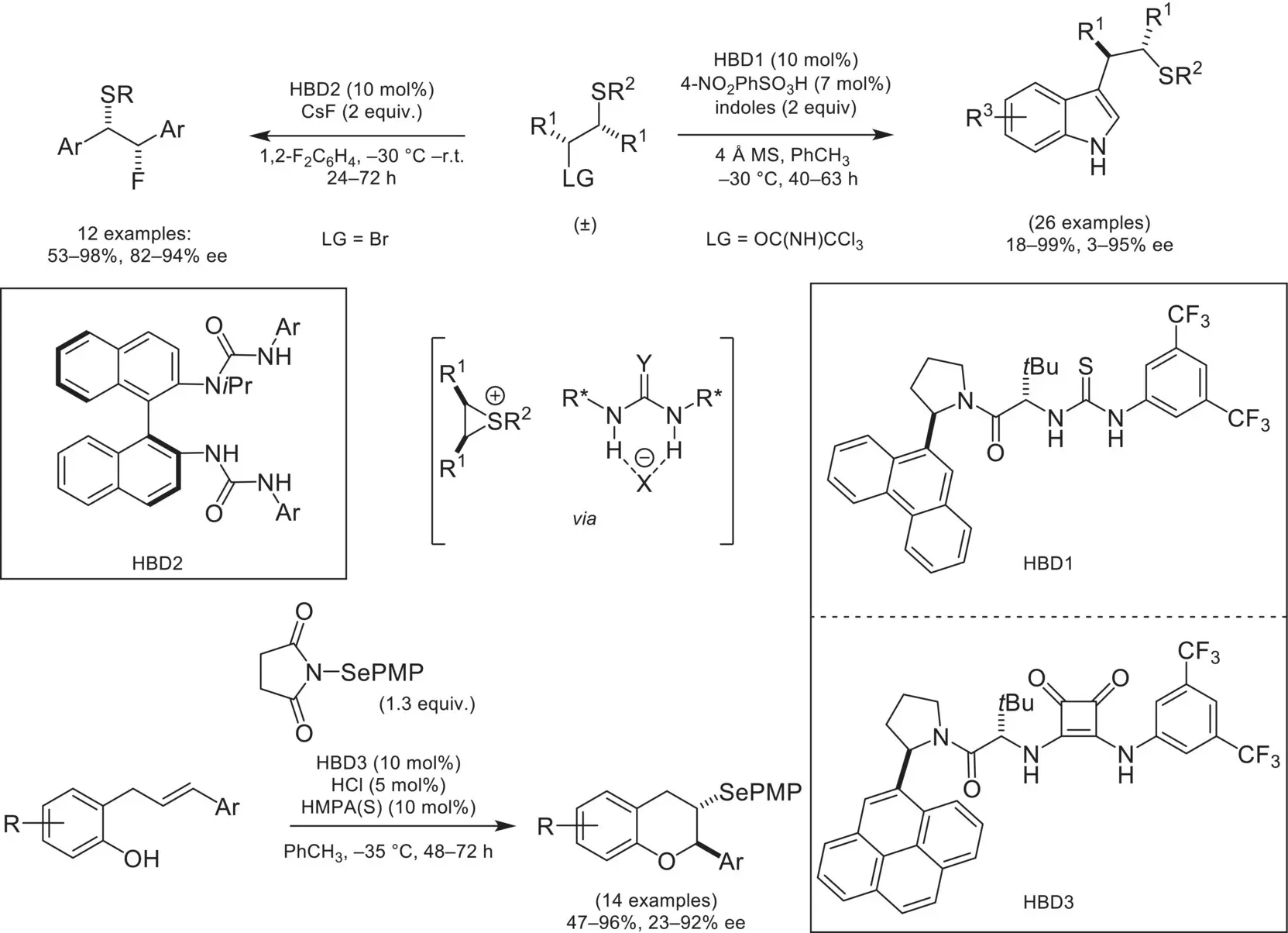
Scheme 4.57. Asymmetric ring opening of strained heterocycles by anion‐binding catalysis.
Source: Based on [193].
1 1. Dolling, U. H. ; Davis, P. ; Grabowski, E. J. J. J. Am. Chem. Soc. 1984, 106, 446–447.
2 2. Hughes, D. L. ; Dolling, U. H. ; Ryan, K. M. ; Schoenewaldt, E. F. ; Grabowski, E. J. J. J. Org. Chem. 1987, 52, 4745–4752.
3 3. O’Donnell, M. J. ; Bennett, W. D. ; Wu, S. J. Am. Chem. Soc. 1989, 111, 2353–2355.
4 4. Lygo, B. ; Wainwright, P. G. Tetrahedron Lett. 1997, 38, 8595–8598.
5 5. Lygo, B. ; Crosby, J. ; Lowdon, T. R. ; Wainwright, P. G. Tetrahedron 2001, 57, 2391–2402.
6 6. Lygo, B. ; Andrews, B. I. Acc. Chem. Res. 2004, 37, 518–525.
7 7. Corey, E. J. ; Xu, F. ; Noe, M. C. J. Am. Chem. Soc. 1997, 119, 12414–12415.
8 8. Corey, E. J. ; Bo, Y. ; Busch‐Petersen, J. J. Am. Chem. Soc. 1998, 120, 13000–13001.
9 9. Jew, S.‐S. ; Yoo, M.‐S. ; Jeong, B.‐S. ; Park, I. Y. ; Park, H.‐G. Org. Lett. 2002, 4, 4245–4248.
10 10. Jew, S.‐S. ; Jeong, B.‐S. ; Yoo, M.‐S. ; Huh, H. ; Park, H.‐G. Chem. Commun. 2001, 1244–1245.
11 11. Park, H.‐G. ; Jeong, B.‐S. ; Yoo, M.‐S. ; Park, M.‐K. ; Huh, H. ; Jew, S.‐S. Tetrahedron Lett. 2001, 42, 4645–4648.
12 12. Ooi, T. ; Kameda, M. ; Maruoka, K. J. Am. Chem. Soc. 1999, 121, 6519–6520.
13 13. Ooi, T. ; Uematsu, Y. ; Kameda, M. ; Maruoka, K. Angew. Chem. Int. Ed. 2002, 41, 1551–1554.
14 14. Lygo, B. ; Allbutt, B. ; James, S. R. Tetrahedron Lett. 2003, 44, 5629–5632.
15 15. Shibuguchi, T. ; Fukuta, Y. ; Akachi, Y. ; Sekine, A. ; Ohshima, T. ; Shibasaki, M. Tetrahedron Lett. 2002, 43, 9539–9543.
16 16. Ohshima, T. ; Gnanadesikan, V. ; Shibuguchi, T. ; Fukuta, Y. ; Nemoto, T. ; Shibasaki, M. J. Am. Chem. Soc. 2003, 125, 11206–11207.
17 17. Ohshima, T. ; Shibuguchi, T. ; Fukuta, Y. ; Shibasaki, M. Tetrahedron 2004, 60, 7743–7754.
18 18. Sasai, H. (2003). Quaternary ammonium salt having spirochirality and its utilization. Mitsubishi Chem. Corp., JP2003335780.
19 19. Kita, T. ; Georgieva, A. ; Hashimoto, Y. ; Nakata, T. ; Nagasawa, K. Angew. Chem. Int. Ed. 2002, 41, 2832–2834.
20 20. Denmark, S. E. ; Gould, N. D. ; Wolf, L. M. J. Org. Chem. 2011, 76, 4260–4336.
21 21. Wen, S. ; Li, X. ; Lu, Y. Asian J. Org. Chem. 2016, 5, 1457–1460.
22 22. O’Donnell, M. J. Tetrahedron 2019, 75, 3667–3696.
23 23. O’Donnell, M. J. ; Wu, S. Tetrahedron Asymmetry 1992, 3, 591–594.
24 24. Lygo, B. ; Crosby, J. ; Peterson, J. A. Tetrahedron Lett. 1999, 40, 8671–8674.
25 25. Jew, S.‐S. ; Jeong, B.‐S. ; Lee, J.‐H. ; Yoo, M.‐S. ; Lee, Y.‐J. ; Park, B.‐S. ; Kim, M. G. ; Park, H.‐G. J. Org. Chem. 2003, 68, 4514–4516.
26 26. Ooi, T. ; Takeuchi, M. ; Kameda, M. ; Maruoka, K. J. Am. Chem. Soc. 2000, 122, 5228–5229.
27 27. Kitamura, M. ; Shirakawa, S. ; Maruoka, K. Angew. Chem. Int. Ed. 2005, 44, 1549–1551.
28 28. Hashimoto, T. ; Maruoka, K. Chem. Rev. 2007, 107, 5656–5682.
29 29. Jolliffe, J. D. ; Armstrong, R. J. ; Smith, M. D. Nat. Chem. 2017, 9, 558–562.
30 30. Li, H. ; Fan, W. ; Hong, X. Org. Biomol. Chem. 2019, 17, 1916–1923.
31 31. Corey, E. J. ; Noe, M. C. ; Xu, F. Tetrahedron Lett. 1998, 39, 5347–5350.
32 32. Zhang, F. Y. ; Corey, E. J. Org. Lett. 2000, 2, 1097–1100.
33 33. Arai, S. ; Tsuji, R. ; Nishida, A. Tetrahedron Lett. 2002, 43, 9535–9537.
34 34. He, R. ; Shirakawa, S. ; Maruoka, K. J. Am. Chem. Soc. 2009, 131, 16620–16621.
35 35. Wang, L. ; Shirakawa, S. ; Maruoka, K. Angew. Chem. Int. Ed. 2011, 50, 5327–5330.
36 36. Shirikawa, S. ; Wang, L. ; He, R. ; Arimitsu, S. ; Maruoka, M. Chem. Asian J. 2014, 9, 1586–1593.
37 37. Shirakawa, S. ; Terao, S. J. ; He, R. ; Maruoka, K. Chem. Commun. 2011, 47, 10557–10559
38 38. Liu, S. ; Maruoka, K. ; Shirakawa, S. Angew. Chem. Int. Ed. 2017, 56, 4819–4823.
39 39. Shirakawa, S. ; Ota, K. ; Terao, S. J. ; Maruoka, K. Org. Biomol. Chem. 2012, 10, 5753–5756.
40 40. Shirakawa, S. ; Maruoka, K. Tetrahedron Lett. 2014, 55, 3833–3839.
41 41. Arai, S. ; Tsuge, H. ; Shioiri, T. Tetrahedron Lett. 1998, 39, 7563–7566.
42 42. Arai, S. ; Tsuge, H. ; Oku, M. ; Miura, M. ; Shioiri, T. Tetrahedron 2002, 58, 1623–1630.
43 43. Jew, S.‐S. ; Lee, J.‐H. ; Jeong, B.‐S. ; Yoo, M.‐S. ; Kim, M.‐J. ; Lee, Y.‐J. ; Lee, J. ; Choi, S.‐H. ; Lee, K. ; Lah, M. S. ; Park, H.‐G. Angew. Chem. Int. Ed. 2005, 44, 1383–1385.
44 44. Hori, K. ; Tamura, M. ; Tani, K. ; Nishiwaki, N. ; Ariga, M. ; Tohda, Y. Tetrahedron Lett. 2006, 47, 3115–3118.
45 45. Allingham, M. T. ; Howard‐Jones, A. ; Murphy, P. J. ; Thomas, D. A. ; Caulkett, P. W. R. Tetrahedron Lett. 2003, 44, 8677–8680.
46 46. Ooi, T. ; Ohara, D. ; Tamura, M. ; Maruoka, K. J. Am. Chem. Soc. 2004, 126, 6844–6845.
47 47. Corey, E. J. ; Zhang, F.‐Y. Org. Lett. 1999, 1, 1287–1290.
48 48. Aires‐de‐Sousa, J. ; Lobo, A. M. ; Prabhakar, S. Tetrahedron Lett. 1996, 37, 3183–3186.
49 49. Murugan, E. ; Siva, A. Synthesis 2005, 12, 2022–2028.
50 50. Mahé, O. ; Dez, I. ; Levacher, V. ; Brière, J.‐F. Angew. Chem. Int. Ed. 2010, 49, 7072–7075.
51 51. Gasparski, C. M. ; Miller, M. J. Tetrahedron 1991, 47, 5367–5378.
52 52. Mettath, S. ; Srikanth, G. S. C. ; Dangerfield, B. S. ; Castle, S. L. J. Org. Chem. 2004, 69, 6489–6492.
53 53. Ooi, T. ; Taniguchi, M. ; Kameda, M. ; Maruoka, K. Angew. Chem. Int. Ed. 2002, 41, 4542–4544.
Читать дальше









